
- •41. Аллергия (определение). Общая этиология и общий патогенез. Виды гиперчувствительности.
- •42. Формы аллергии по Джелу- Кумбсу. Принципы профилактики и терапии иммунопатологических состояний и аллергии.
- •Предупреждение аллергии. Гипосенсибилизация
- •47.Опухоль (определение). Этиология. Механизмы антибластомной резистентности организма. Понятие о предопухолевых (предраковых) состояниях.
- •48.Патогенез опухолевого процесса. Механизмы канцерогенеза. Биологические особенности опухолевого роста.
- •49. Доброкачественные и злокачественные опухоли. Виды атипий (анаплазий) Опухолевая прогрессия, ее клиническое значение.
- •50. Взаимодействие опухоли и организма. Паранеопластический синдром. Принципы профилактики и терапии опухолевого процесса.
Предупреждение аллергии. Гипосенсибилизация
Предупредить развитие аллергических заболеваний можно путем изоляции организма от потенциального антигена, воспроизведением специфической иммунной толерантности или иммунодепрессивных состояний.
Иммунная толерантность вызывается введением новорожденному или эмбриону установленного антигена. Ее воспроизведение представляет интерес для трансплантации органов, а также для предупреждения реализации наследственной способности к аллергическим реакциям на какой-нибудь антиген. У взрослых специфическую иммунную толерантность можно обеспечить введением в очень больших дозах растворимого антигена (паралич Фелтона).
Иммунодепрессивные состояния можно вызвать, подавляя способность к выработке антител ко многим антигенам. Угнетения выработки антител можно добиться тремя способами: облучением, применением иммунодепрессантов, тормозящих клеточное деление и белковый синтез, и специфических антилимфоцитарных антител (АЛС).
Если сенсибилизация уже произошла или если аллергическое заболевание начало развиваться, возможны следующие воздействия:
Подавление выработки антител указанными выше способами.
Специфическая гипосенсибилизация — снижение чувствительности организма к аллергену путем введения больному в малых дозах того аллергена, к которому имеется повышенная чувствительность. Наилучшие результаты такой специфической иммунотерапии отмечаются при лечении аллергических заболеваний реагинового типа (поллиноз, атопическая бронхиальная астма, крапивница и др.). Гипосенсибилизацию по Безредке применяют при введении чужеродных лечебных сывороток. Механизм гипосенсибилизации заключается в подборе малой дозы антигена для повторного введения, так что вырабатываемые БАВ дезактивизируются самим организмом и антитела будут связаны антигеном без аллергии. При атонических заболеваниях его связывают с образованием блокирующих антител, которые соединяются с поступающим в организм аллергеном и тем самым предупреждают его контакт с IgE.
Блокирование выделения и инактивация биологически активных соединений. С этой целью вводят препараты, увеличивающие содержание цАМФ в тучных клетках, ингибиторы протеолитических ферментов, вещества, связывающие гистамин, серотонин и другие БАВ, применяют противовоспалительные средства.
Защита клеток от действия биологически активных веществ (антигистаминные препараты блокируют Н1-гистаминные рецепторы), а также коррекция функциональных нарушений в органах и системах (наркоз способствует защите нервной системы, введение спазмолитических средств уменьшает степень сужения бронхиол и других органов).
43.
Температурные кривые — графическое изображение колебаний температуры при каждодневном измерении. Температурные кривые дают наглядное представление о характере лихорадки (см.), имеют нередко существенное диагностическое и прогностическое значение.
Виды кривых позволяют выделить следующие типы лихорадки.
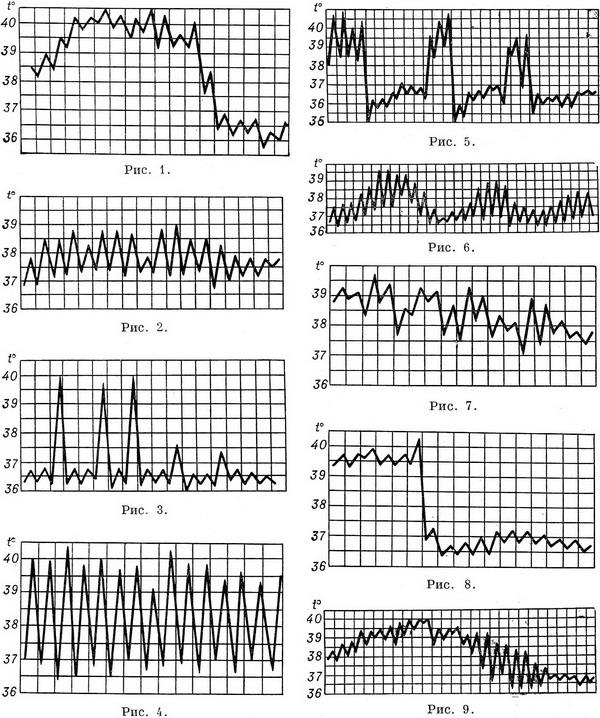
1. При постоянной лихорадке (febris continua) температура тела обычно высокая, в пределах 39°, держится в течение нескольких дней или недель с колебаниями в пределах 1°. Встречается при острых инфекционных заболеваниях: сыпной тиф, крупозная пневмония и др. (рис. 1).
2. Послабляющая, или ремиттирующая, лихорадка (febris remittens) характеризуется значительными суточными колебаниями температуры тела (до 2° и более), встречается при гнойных заболеваниях (рис. 2).
3. Перемежающаяся, или интермиттирующая, лихорадка (febris intermittens) характеризуется резким подъемом температуры тела до 39—40° и больше и спадом в короткий срок до нормальных и даже субнормальных цифр; через 1—2—3 дня такой же подъем и спад повторяются. Характерна для малярии (рис. 3).
4. Гектическая, или истощающая, лихорадка (febris hectica) характеризуется большими суточными колебаниями температуры тела (свыше 3°) и резким падением ее до нормальных и субнормальных цифр, причем колебания температуры большие, чем при ремиттирующей лихорадке; наблюдается при септических состояниях и тяжелых формах туберкулеза (рис. 4).
5. Возвратная лихорадка (febris recurrens). Температура тела повышается сразу до высоких цифр, держится на этих значениях несколько дней, снижается затем до нормы. Через некоторое время лихорадка возвращается и вновь сменяется ремиссией (лихорадочных приступов бывает несколько, до 4—5). Такой тип лихорадки характерен для некоторых спирохетозов (возвратный тиф и др.) (рис. 5).
6. Волнообразная лихорадка (febris undulans). Постепенное изо дня в день повышение температуры с аналогичным характером снижения. Может быть несколько волн подъема и снижения температуры, отличается от возвратной лихорадки постепенным нарастанием и спадением температуры. Встречается при бруцеллезе и некоторых других заболеваниях (рис. 6).
7. Извращенная лихорадка (febris in versa). Утренняя температура выше вечерней, встречается при туберкулезе, затяжном сепсисе, прогностически неблагоприятна.
8. Неправильная лихорадка встречается наиболее часто. Суточные колебания температуры тела разнообразны, длительность не определяется. Наблюдается при ревматизме, пневмониях, дизентерии, гриппе (рис. 7).
По температурным кривым различают 3 периода лихорадки.
1. Начальный период, или стадия нарастания температуры (stadium incrementi). В зависимости от характера заболевания этот период может быть очень коротким и измеряться часами, обычно сопровождаясь ознобом (например, при малярии, крупозной пневмонии), или растягиваться на продолжительный срок до нескольких дней (например, при брюшном тифе).
2. Стадия разгара лихорадки (fastigium или acme). Длится от нескольких часов до многих дней.
3. Стадия снижения температуры. Быстрое падение температуры называется кризисом (малярия, крупозное воспаление легких, сыпной тиф; рис. 8); постепенное снижение называется лизисом (брюшной тиф и др.; рис. 9).
Рис 1—9. Различные виды температурных кривых. Рис 1—7 Лихорадки: рис. 1 — постоянная; рис. 2 — послабляющая; рис. 3— перемежающаяся; рис. 4. — гектическая; рис. 5 — возвратная; рис 6 - волнообразная; риС с. 7 — неправильная. Рис. 8. Кризис. Рис. 9. Лизис.
Принципы коррекции лихорадочных реакций ( при повышении температуры выше 38 у взрослых и выше 39 у детей) – использование антипиретических препаратов:
-нестероидные противовоспалительные средства (НПВС): вольтарен, анальгин, индометацин, напроксен, амидопирин, ибупрофен, бутадион, парацетамол, аспирин.
-стероидные лекарственные средства( кортизил, кортизон, дексаметазол, преднизолон, преднизон).
44. Гипоксия (определение, виды, механизмы компенсации).Принципы профилактики и терапии гипоксии.
Гипоксия (кислородное голодание) - типовой патологический процесс, возникающий в результате недостаточности биологического окисления и обусловленной ею энергетической необеспеченности жизненных процессов.
В зависимости от причин и механизма развития гипоксии могут быть:
экзогенные (при изменениях содержания во вдыхаемом воздухе кислорода и/или общего барометрического давления, сказывающихся на системе обеспечения кислородом) — подразделяются на гипоксическую (гипо - и нормобарическую) и гипероксическую (гипер - и нормобарическую) формы гипоксии;
- дыхательная (респираторная);
- циркупяторная (ишемическая и застойная);
- гемическая (анемическая и вследствие, инактивации гемоглобина);
- тканевая (при нарушении способности тканей поглощать кислород или при разобщении процессов биологического окисления и фосфорилирования);
- субстратная (при дефиците субстратов);
- перегрузочная («гипоксия нагрузки»);
- смешанная. Различают также гипоксии:
по течению — молниеносную (длится несколько десятков секунд), острую (десятки минут), подострую (часы, десятки часов), хроническую (недели, месяцы, годы);
по распространенности — общую и регионарную;
по степени тяжести — легкую, умеренную, тяжелую, критическую (смертельную).
Проявления и исход всех форм гипоксии зависят от природы этиологического фактора, индивидуальной реактивности организма, степени тяжести, скорости развития, от продолжительности процесса.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ГИПОКСИИ ГИПОКСИЧЕСКАЯ ГИПОКСИЯ
Гипобарическая форма возникает при понижении парциального давления кислорода во вдыхаемом воздухе в условиях разреженной атмосферы. Имеет место при подъеме в горы (горная болезнь) или при полетах на летательных аппаратах (высотная болезнь, болезнь летчиков). Основными факторами, вызывающими при этом патологические сдвиги, являются: 1) понижение парциального давления кислорода во вдыхаемом воздухе (гипоксия); 2) понижение атмосферного давления (декомпрессия или дизбаризм).
Нормобарическая форма развивается в тех случаях, когда общее барометрическое давление нормальное, но парциальное давление кислорода во вдыхаемом воздухе понижено. Возникает данная форма гипоксии главным образом в производственных условиях (работа в шахтах, неполадки в системе кислородного обеспечения кабины летательного аппарата, на подводных лодках, имеет место также при нахождении в помещениях малого объема в случае большой скученности людей.)
При гипоксической гипоксии снижаются парциальное давление кислорода во вдыхаемом и альвеолярном воздухе; напряжение и содержание кислорода в артериальной крови; возникает гипокапния, сменяющаяся гиперкапнией.
ГИПЕРОКСИЧЕСКАЯ ГИПОКСИЯ
Гипербарическая форма возникает в условиях избытка кислорода («голод среди изобилия»). «Лишний» кислород не потребляется в энергетических и пластических целях; угнетает процессы биологического окисления; подавляет тканевое дыхание; является источником свободных радикалов, стимулирующих перекисное окисление липидов; вызывает накопление токсических продуктов, а также - повреждение легочного эпителия, спадение альвеол, снижение потребления кислорода и в конечном счете - нарушение обмена веществ, возникновение судорог, коматозного состояния (осложнения при гипербарической оксигенации).
Нормобарическая форма развивается как осложнение при кислородной терапии, если длительно используются высокие концентрации кислорода, особенно у пожилых людей, поскольку у них с возрастом падает активность анти-оксидантной системы.
При гипероксической гипоксии в результате увеличения парциального давления кислорода во вдыхаемом воздухе возрастает его воздушно-венозный градиент, но снижается скорость транспорта кислорода артериальной кровью и потребления кислорода тканями, накапливаются недоокисленные продукты, возникает ацидоз.
дыхательная (респираторная) гипоксия
Развивается в результате недостаточности газообмена в легких в связи с альвеолярной гиповентиляцией, нарушением вентиляционно-перфузионных отношений, с затруднением диффузии кислорода (болезни легких, трахеи, бронхов, нарушение функции дыхательного центра; пневмо -, гидро-, гемоторакс, воспаление, эмфизема, саркоидоз, асбестоз легких; механические препятствия для поступления воздуха; локальное запустевание сосудов легких, врожденные пороки сердца). При респираторной гипоксии в результате нарушения газообмена в легких снижается напряжение кислорода в артериальной крови, возникает артериальная гипоксемия, в большинстве случаев сочетающаяся с гиперкапнией.
ЦИРКУЛЯТОРНАЯ (СЕРДЕЧНО-СОСУДИСТАЯ) ГИПОКСИЯ
Возникает при нарушениях кровообращения, приводящих к недостаточному кровоснабжению органов и тканей. Важнейшим показателем и патогенетической основой ее развития является уменьшение минутного объема крови
из-за расстройства сердечной деятельности (инфаркт, кардиосклероз, перегрузка сердца, нарушения электролитного баланса, нейрогуморальной регуляции функции сердца, тампонада сердца, облитерация полости перикарда); гипово-лемии (массивная кровопотеря, уменьшение притока венозной крови к сердцу и др.). При циркуляторной гипоксии падает скорость транспорта кислорода артериальной и капиллярной кровью при нормальном или сниженном содержании его в артериальной крови и низком - в венозной, т.е. имеет место высокая артериовенозная разница по кислороду.
КРОВЯНАЯ (ГЕМИЧЕСКАЯ) ГИПОКСИЯ /
Развивается при уменьшении кислородной емкости крови. Причинами ее могут быть анемия и гидремия; нарушение способности гемоглобина связывать, транспортировать и отдавать тканям кислород при качественных изменениях гемоглобина (образование карбоксигемоглобина, метгемоглобинообразование, генетически обусловленные аномалии гемоглобина). При гемической гипоксии снижается содержание кислорода в артериальной
и венозной крови; уменьшается артериовенозная разница по кислороду.
тканевая гипоксия
Различают первичную и вторичную тканевую гипоксию.
К первичной тканевой (иеллюлярной) гипоксии относят состояния, при которых имеет место первичное поражение аппарата клеточного дыхания. Основными патогенетическими факторами первично-тканевой гипоксии являются:
- снижение активности дыхательных ферментов (цитохромоксидазы при отравлении цианидами), дегидрогеназ (действие больших доз алкоголя, уретана, эфира), снижение синтеза дыхательных ферментов (недостаток рибофлавина, никотиновой кислоты);
- активация процессов перекисного окисления липидов, ведущая к дестабилизации и декомпозиции мембран митохондрий и лизосом (ионизирующее излучение, дефицит естественных антиоксидантов - рутина, аскорбиновой кислоты, глютатиона, каталазы и др.);
- разобщение процессов биологического окисления и фосфорилирования, при котором потребление кислорода тканями может возрастать, но значительная часть энергии рассеивается в виде тепла и, несмотря на высокую интенсивность функционирования дыхательной цепи, ресинтез макроэргических соединений не покрывает потребностей тканей; в результате возникает относительная недостаточность биологического окисления и ткани оказываются в состоянии гипоксии. При тканевой гипоксии парциальное напряжение и содержание кислорода в артериальной крови могут до известного предела оставаться нормальными, а в венозной крови значительно повышаются; уменьшается артериовенозная разница по кислороду.
Вторичная тканевая гипоксия может развиться при всех других видах гипоксии.
субстратная гипоксия
Развивается в тех случаях, когда при адекватной доставке кислорода к органам и тканям, нормальном состоянии мембран и ферментных систем возникает первичный дефицит субстратов, приводящий к нарушению всех звеньев биологического окисления. В большинстве случаев такая гипоксия обусловливается дефицитом в клетках глюкозы (например, при расстройствах углеводного обмена - сахарный диабет и др.) или других субстратов (жирных кислот в миокарде), а также тяжелым голоданием.
перегрузочная гипоксия («гипоксия нагрузки»)
Возникает при напряженной деятельности органа или ткани, когда функциональных резервов систем транспорта и утилизации кислорода при отсутствии в них патологических изменений оказывается недостаточно для удовлетворения резко возросшей потребности в кислороде (чрезмерная мышечная работа, перегрузка сердца). При перегрузочной гипоксии формируется «кислородный долг» наряду с увеличением скорости доставки и потребления кислорода, а также образования и выведения углекислоты.
смешанная гипоксия
Гипоксия любого типа, достигнув определенной степени, неизбежно вызывает нарушения функции различных органов и систем, участвующих в обеспечении доставки к ним кислорода и его утилизации. Сочетание различных типов гипоксии возможно, в частности, при шоке, отравлении боевыми отравляющими веществами, заболеваниях сердца, при коматозных состояниях и др.
Первые изменения в организме при гипоксии связаны с включением реакций, направленных на сохранение гомеостаза (фаза компенсации). Если этих приспособительных реакций оказывается недостаточно, в организме происходят структурно-функциональные нарушения (фаза декомпенсации). Различают реакции, направленные на приспособление к кратковременной острой гипоксии (срочные), и реакции, обеспечивающие устойчивое приспособление к менее выраженной, но длительно существующей или многократно повторяющейся гипоксии (реакции долговременного приспособления). Срочные реакции возникают рефлекторно вследствие раздражения рецепторов сосудистой системы и ретикулярной формации ствола мозга изменившимся газовым составом крови. В результате усиливается альвеолярная вентиляция, увеличивается минутный дыхательный объем (за счет углубления дыхания, учащения дыхательных экскурсий и мобилизации резервных альвеол -компенсаторная одышка); учащаются сердечные сокращения, увеличиваются масса циркулирующей крови (за счет выброса крови из кровяных депо), венозный приток, ударный и минутный объемы сердца, скорость кровотока, кровоснабжение мозга, сердца и других жизненно важных органов, уменьшается кровоснабжение мышц, кожи и т.д. (централизация кровообращения); повышается кислородная емкость крови (за счет усиленного вымывания эритроцитов из костного мозга), а затем - активации эритропоэза, улучшаются кислородсвязывающие свойства гемоглобина (оксигемоглобин приобретает способность отдавать тканям большее количество кислорода даже при умеренном снижении рО2 в тканевой жидкости, чему способствует развивающийся в тканях ацидоз; при нем оксигемоглобин легче отдает кислород). Кроме того, ограничивается активность органов и тканей, непосредственно не участвующих в обеспечении транспорта кислорода. Повышается сопряженность процессов биологического окисления и фосфорилирования. Усиливается анаэробный синтез АТФ за счет активации гликолиза. В различных тканях возрастает интенсивность процесса продуцирования оксида азота, что ведет к расширению прекапиллярных сосудов, снижению адгезии и агрегации тромбоцитов, к активации процесса синтеза стресс-белков, защищающих клетку от повреждения. Важной приспособительной реакцией при гипоксии является активация гипоталамо-гипофизарно-надпочечниковой системы (стресс-синдром), гормоны которой (глюкокортикоиды), стабилизируя мембраны лизосом, снижают тем самым повреждающее действие гипоксического фактора и препятствуют развитию гипоксического некробиоза, повышая устойчивость тканей к недостатку кислорода.
Компенсаторные реакции при гипероксической гипоксии направлены на предупреждение возрастания напряжения кислорода в артериальной крови и в тканях — на ослабление легочной вентиляции и центрального кровообращения, снижение минутного объема дыхания и кровообращения, частоты сердечных сокращений, ударного объема сердца, уменьшение объема циркулирующей крови, ее депонирование в паренхиматозных органах; понижение артериального давления; сужение мелких артерий и артериол мозга, сетчатки глаза и почек, наиболее чувствительных как к недостатку, так и к избытку кислорода. Эти реакции в целом удовлетворяют соответствующие потребности тканей в кислороде.
Принципы устранения гипоксии
-Этиотропный:1)экзогенный тип гипоксии:нормализация pO во вдыхаемом воздухе,добавление во вдыхаемый воздух СО;2)эндогенный тип:устранение болезни или патологического процесса,причины гипоксии;
-Патогенетический:ликвидация или снижение степени ацидоза,уменьшение дисбаланса ионов в клетке и биологической жидкости,предотвращение или снижение степени повреждения мембран и ферментов клетки,оптимизация или снижение уровня функции органов и их систем;
-Симптоматический: устранение неприятных ощущений, усугубляющих состояние пациента.
45. Инфекционный процесс и инфекционная болезнь. Этиология инфекционного процесса. Понятие аутоинфекция. Взаимодействие макро- и микроорганизма. Патогенез инфекционного процесса. Сепсис. Принципы лечения инфекционного процесса.
Инфекционный процесс- выработанный в процессе эволюции типовой патологический процесс, возникающий при взаимодействии микроорганизма с макроорганизмом, особенно в неблагоприятный условиях внешней и\или внутренней среды.
Виды инфекционного процесса:
Бактериемия, вирусемия – наличие в крови бактериий или вирусов без признаков размножения.
Сепсис – тяжелая генерализованная форма ИП, обусловленная размножением микроорганизмов в крови, нередко и в других биологических жидкостях.
Септикопиемия – вид ИП, характеризующийся вторичным размножением гнойных очагов в различных органах и тканях пациентов с сепсисом.
Микстинфекция – вид ИП, вызванный одновременно двумя или более микроорганизмами.
Реинфекция- повторное (после выздоровления) возникновение у пациента ИП, вызванного тем же микроорганизмом.
Суперинфекция – повторное инфицирование организма тем же возбудителем до периода выздоровления.
Вторичная инфекция – ИП, развивающийся на фоне уже имеющейся (первичной) инфекционной болезни, вызванной другим микроорганизмом.
Аутоинфекция — заболевание, вызванное возбудителем, который находился до этого в организме в непатогенной форме.
Инфекционная болезнь — это заболевание, вызываемое проникновением в организм патогенных (болезнетворных) микроорганизмов. Для того, чтобы патогенный микроб вызвал инфекционное заболевание, он должен обладать вирулентностью (ядовитостью; лат. virus — яд), то есть способностью преодолевать сопротивляемость организма и проявлять токсическое действие.
Виды ИБ:
Здоровое носительство микроорганизма – наличие м/о в организме не сопровождается выраженными структурными и метаболическими изменениями.
Субклиническая форма инфекции – при отсутствии симптомов наблюдаются неспецифические метаболические и структурные изменения.
Клиническая форма инфекции – в разной степени выражены специфические симптомы и неспецифические реакции организма.
По клиническому течению: Острые ИБ и хронические.
По степени тяжести ИБ мб: легкой, средней, тяжелой и крайне тяжелой.
Этиология ИП:
Причиной ИП являются инфекционные возбудители: бактерии, вирусы, грибы, простейшие, прионы и др.
Характер и выраженность ИП (ИБ) зависит от следующих факторов:
Основные свойства инфекционного возбудителя;
Патогенность (способность вызывать опред. ИБ) и вирулентность (степень патогенности);
Особенность взаимодействия микро с макро;
Тропность микро к различным тканям макро;
Исходное состояние макро;
Исходное состояние внешней среды.
Взаимоотношения макро- и микроорганизма:
Паразитизм – форма антагонистического взаимоотношения макроорганизма и патогенного микроорганизма, при которой микроорганизм использует организм хозяина как источник питания и место постоянного или временного обитания; наносит тот или иной ущерб макроорганизму.
Комменсализм - форма промежуточного типа взаимодействия макроорганизма и условно патогенного микроорганима, при которой размножающиеся в обычных условиях микроорганизмы не наносят организму-хозяину вреда.
Мутуализм – форма взаимовыгодного отношения макроорганизма и непатогенных микроорганизмов.
Патогенез ИП:
В патогенезе ведущую роль играет характер и интенсивность взаимодействия возбудителя и иммунной системы макро. При снижении иммунитета – усиливается патогенное действие микробов.
В патогенезе ИП также важную роль играют выраженность и длительность воспаления, лихорадки, гипоксии и др
Этапы ИП:
Адгезия микро к эпителию и эндотелию тканей и органов макро.
Инвазия микро во внутренних средах хозяина
Пролиферация микро во внутренних средах хозяина
Продукция микробами токсинов
Формирование специфического иммунитета (АТ)
Периоды течения ИБ:
Инкубационный период – время от момента попадания микро в макро до появления первых неспецифических признаков ИБ.
Продромальный период – интервал времени от появления первых неспецифических общих признаков до полного разгара ИБ.
Период основных клинических проявлений – интервал времени от появления первых специфических симптомов ИБ до начала спада клинических проявлений.
Период завершения мб различным : а) Выздоровление – благоприятное завершение ИБ.
Б) Бациллоносительство
В) Рецидив – повторное появление признаков заболевания.
Г) Осложнения.
Принципы лечения:
Этиотропная терапия – на ликвидацию причины ИП.
Патогенетическая терапия блокирует основное, ведущее звено патогенеза.
Симптоматическая терапия направлена облегчить состояние больного.
46.Общая характеристика патологии роста тканей. Причины, механизмы, обменные и структурные проявления гипотрофии (атрофии), гипоплазии (аплазии), гипертрофии и гиперплазии, метаплазии, их значение для организма. Эмбриопатии.
Патологический рост проявляется в виде избытка, недостатка и извращения (качественного нарушения) размножения, дифференци- ровки, роста и созревания субклеточных, клеточных и межклеточных структур. Патологический рост тканей и органов сопровождается многообразными местными и общими изменениями. Он обычно возникает в части ткани или органа, но может захватывать всю ткань или орган, а также несколько или много тканей или органов. Те или иные нарушения тканевого роста могут развиваться в различные периоды онтогенеза:
в пренаталъном, или внутриутробном, периоде (у эмбриона — в эмбриональном, у плода — в фетальном периоде);
в постнатальном периоде, т.е. после рождения: у новорожденных, в препубертатном (детском), пубертатном (молодом и зрелом) и постпубертатном (пожилом и старческом) возрастах.
Следует отметить, что для каждого из перечисленных периодов онтогенеза существуют свои особенности и даже характерные варианты.
Нарушение тканевого роста в эмбриональном периоде
Нарушение эмбрионального развития с формированием пороков развития тканей, органов и систем называют тератогенезом.
Тератогенез (от греч. teras, teratos — чудовище, урод; genesis — происхождение, развитие) — возникновение порока развития ткани, органа или системы в результате как ненаследственных (различных нарушений зародышевого развития), так и наследственных изменений.
Примерами генетически обусловленных нарушений эмбрионального развития могут быть расщепление верхней губы и нёба, корот- копалость (брахидактилия), шестипалость, синдактилия, некоторые пороки сердца, нарушения развития половой системы и др.
Примерами нарушений эмбрионального развития, связанных с ненаследственными факторами, могут служить отсутствие, недоразвитие или неправильное развитие отдельных органов и др.
Факторы, вызывающие тератогенез, называют тератогенными.
Тератогенными могут быть химические (в том числе лекарственные), физические или биологические факторы, вызывающие пороки развития различных структур организма.
К основным группам тератогенных факторов относятся следующие:
ионизирующее излучение;
инфекции (преимущественно вирусные);
метаболические нарушения и вредные привычки у беременной;
лекарственные средства и химические вещества.
Нарушение тканевого роста в препубертатном и пубертатном периодах
Специфические нарушения тканевого роста в эти периоды связаны прежде всего с нарушением формирования скелета, правильных пропорциий тела, отклонениями от нормального роста. Эти нарушения могут быть также связаны с генетическими расстройствами (например, различные варианты хондродистрофии, синдром Шерешевского-Тернера и др.), но могут быть не связанными с наследственностью, например обусловлены нарушением образования и действия гормона роста, гормонов щитовидной железы.
Нарушение тканевого роста в постпубертатном (взрослом) периоде
Принципиально можно выделить два основных типа нарушения роста тканей:
L гипербиотический, или избыточный, рост тканей (гипертрофия, гиперплазия, гиперрегенерация, опухолевый рост);
• гипобиотический, гипопластический, или недостаточный, рост тканей (атрофия, гипотрофия, гипоплазия, дистрофия и дегенерация).
Эти виды нарушений тканевого роста встречают также и в другие периоды жизни (например, в пубертатном и препубертатном* а в отдельных случаях в фетальном и эмбриональном периодах развития организма).
Атрофия и гипотрофия (греч. а — отсутствие, отрицание; hypo — ^достаточно; trophe — питание) — прижизненное уменьшение объема
клеток, а также межклеточных структур тканей и органов, возникающее за счет либо гипотрофии, либо гипоплазии, либо их сочетания и сопровождающееся снижением их функций.
Различают физиологическую (например, старческая атрофия хрящей межпозвонковых дисков, костей, половых желез) и патологическую атрофию.
Патологическая атрофия как результат развития заболеваний или патологических процессов может быть общей (истощение) и местной.
Общая атрофия возникает в таких ситуациях:
алиментарное истощение;
онкологические заболевания (раковая кахексия);
эндокринная патология (гипопитуитаризм, гипокортицизм);
тяжелые и длительные инфекционные и токсические заболевания.
Местная атрофия возникает по таким причинам:
I бездействие и длительное снижение функций органа (атрофия мышцы при перерезке сухожилия, атрофия мышц у космонавтов вследствие длительного действия невесомости);
ишемия органа (атрофия и сморщивание почек при атеросклерозе почечных артерий);
длительное повреждающее действие на ткань или органы различных физических, химических и биологических патогенных факторов;
I денервация органа (см. раздел «Нейродистрофический процесс»);
длительное сдавление органа (опухолью, аневризмой соседнего органа, жидкостью, например при водянке головного мозга, яичка), приводящее к нарушению его питания и обмена
at-* веществ.
Дистрофия (dys — нарушение, расстройство; trophe — питаю) —расстройство состава клеточно-тканевых структур, обусловленное нарушением в них процессов метаболизма (характера и интенсивности обмена веществ) и сопровождающееся либо накоплением, либо уменьшением тех или иных веществ (соединений), либо появлением веществ, которые в норме не встречают.
Дисплазия - нарушение процесса развития клеток, проявляющееся изменением их структуры (количества, формы, размеров клеток, их орга- нем, мембран), функций, жизнедеятельности и продолжительности жизни. ;В патогенезе дисплазий большое значение имеют расстройства процесса дифференцировки клеток.
Гипертрофия — увеличение объема ткани или органа за счет увеличения объема их клеток и межклеточных структур.
Гипертрофия клеток может происходить за счет увеличения объема'и количества их субклеточных структур, т.е. гипертрофия клетки | обычно сочетается с гипертрофией и гиперплазией ее внутриклеточных ультраструктур.
Гиперплазия — увеличение объема ткани или органа за счет повышения количества клеток и межклеточных структур.
Виды гипертрофии и гиперплазии
По биологическому значению различают физиологическую и патологическую гипертрофию и гиперплазию.
Физиологическая возникает в физиологических условиях, например в матке — при беременности, в грудной железе — при лактации и т.д. Гипертрофию скелетной мускулатуры при интенсивной и длительной мышечной нагрузке также относят к физиологической.
Патологическая развивается при различных видах патологии, например в миокарде при пороках клапанов сердца или артериальной гипертензии.
По морфологическим особенностям выделяют следующие виды гипертрофии и гиперплазии: истинную, ложную и полых органов.
Истинная гипертрофия характеризуется пропорциональным увеличением паренхимы (от греч. parenchima — совокупность основных функционирующих элементов внутреннего органа, покрытых соединительнотканной стромой, капсулой) и других тканей. При этом отмечают увеличение объема и специфических функций ткани или органа.
Ложная гипертрофия характеризуется непропорциональным увеличением паренхимы и других тканей, проявляется избыточным ростом главным образом соединительной ткани. При этом отмечают увеличение объема и уменьшение специфических функций ткани или органа.
Гипертрофия полых органов бывает эксцентрической (когда полость органа расширяется) и концентрической (когда полость органа уменьшается).
В зависимости от механизмов возникновения выделяют следующие виды гипертрофии и гиперплазии:
рабочая гипертрофия, например гипертрофия скелетных мышц, развивающаяся при физической нагрузке, или гипертрофия миокарда — при артериальной гипертензии;
заместительная {викарная) гипертрофия (гиперплазия), возникающая в одном из парных органов при гибели или удалении части или всего другого органа (легкие, почки, надпочечники, семенники);
корреляционная (нейрогуморальная) — возникает в одном из органов, входящих в единую физиологическую систему (например, гипертрофия молочной железы — при удалении яичника или семенника, гипертрофия гипофиза — при удалении надпочеч-
ника, гипертрофия миокарда — при длительном спазме артериальных сосудов и т.д.);
регенераторно-репаративная (регенераторная, регенеративная) — возникает в оставшейся части органа при частичном повреждении другой части (например, частичная гепатэктомия, спленэк- томия, нефрэктомия);
вакатная (от лат. vacuum — пустой) гипертрофия — происходит разрастание опорной ткани (костной, хрящевой, жировой) при атрофии паренхимы органа (например, при атрофии мышц между мышечными волокнами разрастается жировая ткань, при атрофии мозга происходит утолщение костей черепа);
гипертрофические разрастания — обычно возникают в тканях и органах при хроническом воспалении, например разрастание слизистых оболочек с образованием полипов (желудок, кишечник).
Гипертрофия (как и гиперплазия) может иметь компенсаторный характер, например рабочая, заместительная или регенерационная гипертрофия, но может не иметь компенсаторного характера, например корреляционная гипертрофия или редкие случаи врожденной гипертрофии. Независимо от вида гипертрофии клетки органа находятся в невыгодных условиях, поскольку поступление кислорода, питательных веществ, регуляция клеточных процессов при гипертрофии нарушаются, что может сопровождаться активацией апоптоза клеток и замещением ткани гипертрофированного органа соединительной тканью и развитием склероза органа, например кардиосклерозом на фоне гипертрофии миокарда.
Метаплазия— стойкое замещение дифференцированных клеток одного типа дифференцированными клетками другого типа при сохранении основной видовой принадлежности ткани. Основной причиной метаплазии, в отличие от гетероплазии, являются патологические стимулы (изменения окружающей среды, воспаление и инфекционные заболевания, эндокринные нарушения и т. д.). При прекращении воздействия патологических факторов, ткань возвращает свою нормальную морфологическую структуру.
