
2015-СК-біохімія-07-Ензими-ІКТ---
.pdf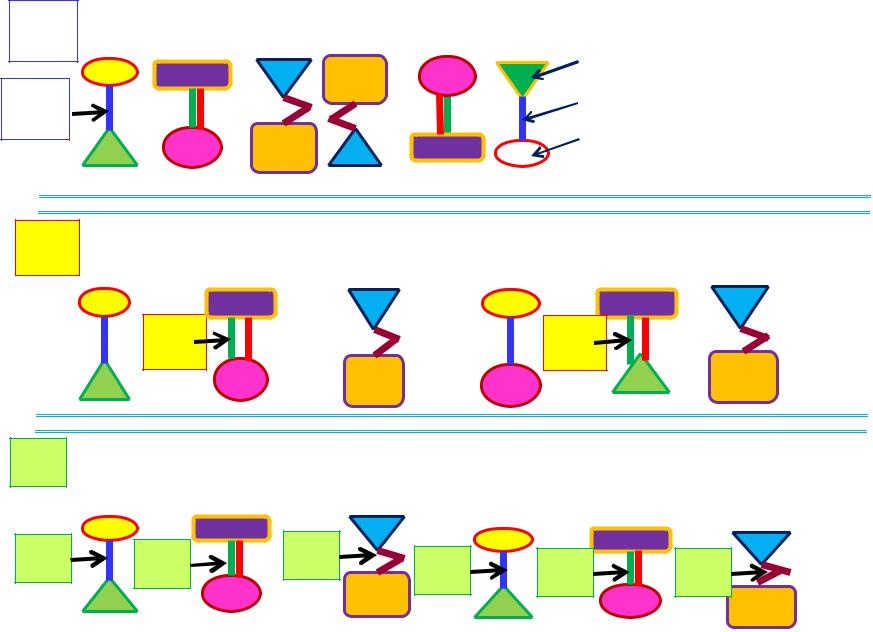
|
Ензимна реакція та субстратна специфічність |
||
Е |
(специфічність реакції - висока і субстратна специфічність - висока) |
||
1 |
|
група |
|
|
|
|
|
Е1 |
|
зв'язок |
Наприклад, |
|
уреаза |
||
|
група |
||
|
|
|
|
Е2 |
(специфічність реакції - висока і субстратна специфічність - низька) |
||
|
|
|
Наприклад, |
|
Е2 |
Е2 |
ліпаза |
|
|
||
Е3 |
(специфічність реакції - низька і субстратна специфічність - низька) |
|||||
|
|
|
|
|
|
Наприклад, |
|
|
|
|
|
|
нуклеаза |
Е |
Е3 |
Е3 |
Е3 |
Е3 |
Е3 |
|
3 |
|
11 |
||||
|
|
|
|
|
|
|

Більшість ензимів є набагато більшими за субстрат і тому вони діють тільки своєю малою частиною (біля 3–4 амінокислот) у каталітичному процесі.
Область, на якій зосереджені “активні” залишки амінокислот, зв'язує субстрат і там проходить відповідна реакція. Таку область називають активним сайтом.
Ензими також мають місця – сайти, які зв'язують кофактори (іони металів і коензими), що необхідні для каталізу.
12

Лактатдегідрогеназа (ЛДГ)
13
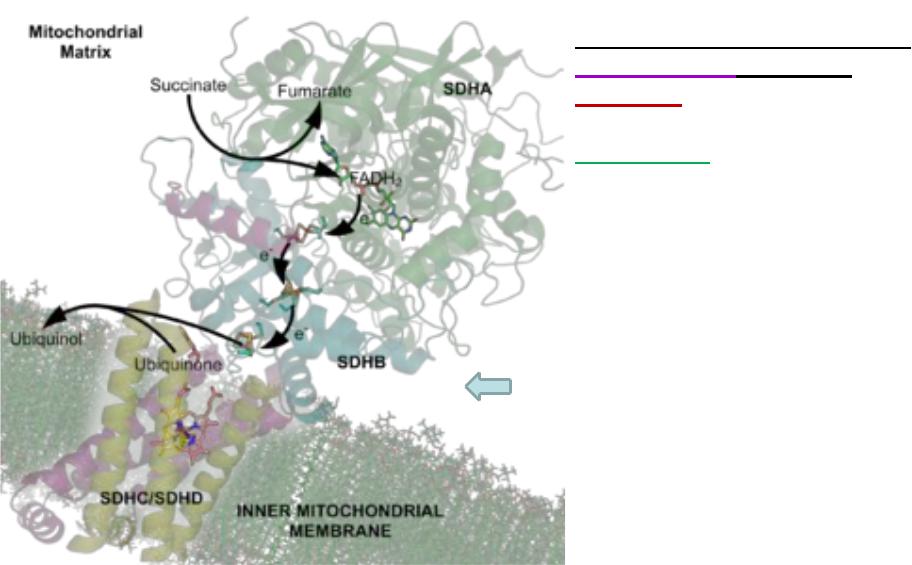
2. Кофактори. Коензими
Ензими, крім активних сайтів, мають місця – сайти, які зв'язують кофактори: іони металів (наприклад,
Mg2+, Zn2+, Мn2+, Со2+) і
коензими, що необхідні для каталізу.
Сукцинатдегідрогеназний комплекс з кількома кофакторами, включаючи флавін, Ферум-Сульфурні центри і гем.
14

Кофактори часто класифікуються як неорганічні речовини (іони металів), які необхідні для каталітичної реакції або підвищення її швидкості.
Приклади деяких ензимів, які потребують іони металів як кофакторів
Кофактор |
Ензим або протеїн |
|
Zn++ |
Карбонова ангідраза |
|
Zn++ |
алкогольдегідрогеназа |
|
Fe+++ або Fe++ |
цитохроми, гемоглобін |
|
Fe+++ або Fe++ |
феродоксин |
|
Cu++ або Cu+ |
цитохромоксидаза |
|
K+ і Mg++ |
піруватфосфокіназа |
15 |
|
|

Водорозчинні вітаміни |
коензими |
|
|
Вітамін |
Коензимна форма |
Тіамін (вітамін B1) |
тіамінпірофосфат |
Ніацин (нікотинова кислота) |
NADP+, NAD+ |
Рибофлавін (вітамін B2) |
FAD, FMN |
Пантотенова кислота |
Коензим A |
|
Піридоксаль, піридоксин, піридоксальфосфат піридоксамін (вітамін B6)
5’-дезоксиаденозилкобаламін
Кобаламін (вітамін B12) метилкобаламін
метилкобаламін
Біотин Біотин-лізинові комплекси (біоцитин -
біотин з’єднаний з ε-аміногрупою лізину в активному центрі ензимів групи карбоксилаз)
 Ліпоєва кислота
Ліпоєва кислота Ліпоїлолізинові комплекси (ліпоаміди)
Ліпоїлолізинові комплекси (ліпоаміди)
Фолієва кислота |
тетрагідрофолат |
16 |
|
||
|
|

Коензим
біоцитин
|
в |
н |
К |
і |
и |
д |
||
о |
п |
х |
е |
о |
|
н |
в |
в |
з |
і |
і |
и |
д |
т |
м |
н |
а |
и |
і |
м |
|
|
і |
і |
д |
н |
|
и |
|
|
о |
|
|
17 |
|

3. Механізм участі ензимів у біологічних реакціях (на прикладі односубстратної реакції)
Механізм для односубстратної ензимної реакції. Ензим (E) зв'язує субстрат (S) внаслідок чого утворюється продукт (P).
Зв'язування |
Каталітична |
|
стадія |
||
субстрату |
||
|
18
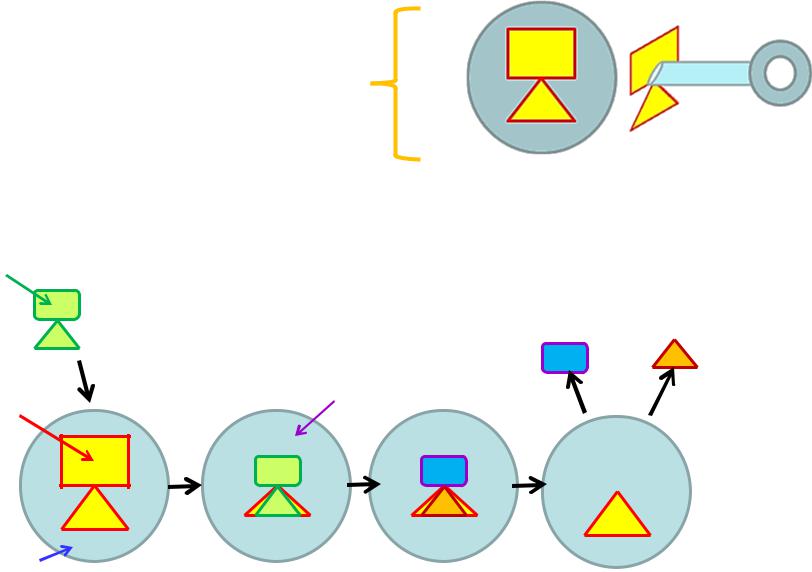
Модель |
«замок і ключ» |
|
||
(взаємодії |
ензиму |
з |
|
|
субстратом) за |
лауреатом |
|
||
Нобелівської премії, хіміком- |
|
|||
органіком |
Еміль |
Фішером |
у Замок |
Ключ |
1894. |
|
|
|
|
У1958, Даніель Кошланд запропонував
Субстрат модифікацію до моделі «замок-ключ».
Активний |
сайт |
Невеликі зміни структури |
|
Продукти |
|||||
ензиму в момент |
|
|
|
|
|||
зв'язування субстрату |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ензим |
|
|
|
|
|
Ензим- |
Комплекс |
Продукти |
|
|
субстратний |
|
||
Схема дії |
ензим-продукт |
залишають |
|
|
комплекс |
|
|||
|
активний сайт |
|
||
ензиму |
|
|
19 |
|
|
|
ензиму |
||
|
|
|
|
4. Номенклатура та класифікація ензимів
За типом реакцій, що каталізують, ензими підрозділяються на 6 класів згідно ієрархічної класифікації ферментів (КФ або EC — Enzyme Commission code).
Класифікацію було запропоновано Міжнародним союзом біохімії і молекулярної біології (International Union of Biochemistry and Molecular Biology).
Кожен клас містить підкласи (до яких входять підпідкласи, де вказані номери ензимів), так що фермент описується сукупністю чотирьох чисел,
розділених |
крапками. |
|
Наприклад, |
||
алкогольдегідрогеназа |
має |
код |
КФ |
1.1.1.1, |
|
лактатдегідрогеназа – КФ 1.1.1.27. |
|
|
|
||
Перше число описує клас реакцій, що каталізує
ензим. |
20 |
|
