
- •Работа 1. Седиментационный анализ суспензий методом непрерывного взвешивания осадка.
- •Работа 20. Применение уравнения Фрейндлиха к адсорбции органических кислот на твердых адсорбентах.
- •Работа 32. Определение электрокинетического потенциала мембран методом электроосмоса.
- •Работа 39. Очистка коллоидных растворов и суспензий от электролитов методом электродиализа.
- •Работа 40а. Исследование зон коагуляции с помощью фотоэлектроколориметра.
- •Работа 48. Исследование процесса набухания твердых полимеров.
Работа 20. Применение уравнения Фрейндлиха к адсорбции органических кислот на твердых адсорбентах.
В этой лабораторной работе исследуют адсорбцию из раствора уксусной кислоты на активированном угле. Перед началом работы споласкивают дистиллированной водой рабочие колбы, пипетки и колбу для задачи. В колбу для задачи в лаборантской получают исходный раствор уксусной кислоты. Из него следующим образом приготовляют растворы различной концентрации посредством разбавления вдвое.
В 5 колб (№№ 26) на 100 мл пипеткой наливают по 50 мл дистиллированной воды. В оставшуюся колбу (№ 1) наливают 50 мл исходного раствора. Затем снова отбирают 50 мл исходного раствора из колбы с задачей и добавляют его в колбу с водой (№ 2). Хорошо взбалтывают и споласкивают полученным раствором пипетку, набирая полученный раствор в пипетку и выливая его обратно в колбу.
Затем отбирают 50 мл полученного раствора (№ 2) этой же пипеткой и добавляют в следующую колбу с водой (№ 3). Хорошо перемешивают и моют полученным раствором пипетку как в случае предыдущего раствора. Отбирают 50 мл полученного раствора (№ 3) и так далее до тех пор, пока не получают 6 растворов, включая исходный. Объем приготовленных растворов во всех колбах должен быть 50 мл, поэтому из последней колбы (№ 6) 50 мл раствора отбирают пипеткой и выливают в раковину. Затем в каждую из шести колб добавляют по 1 г адсорбента – активированного угля; при этом необходимое количество угля отмеряют пробиркой, насыпая уголь до метки.
Колбы с углем встряхивают, перемешивая содержимое, и оставляют на 40 минут. В это время определяют концентрацию исходного раствора уксусной кислоты посредством титрования трех аликвот по 10 мл раствором NaOH в присутствии индикатора фенолфталеина. Добавлять щелочь, находящуюся в бюретках, необходимо до неисчезающего светло розового цвета раствора (концентрация щелочи различается для двух рабочих столов и указана на бутылях). Результаты титрования записывают в таблицу 20.1.
Таблица 20.1.
-
№ пробы
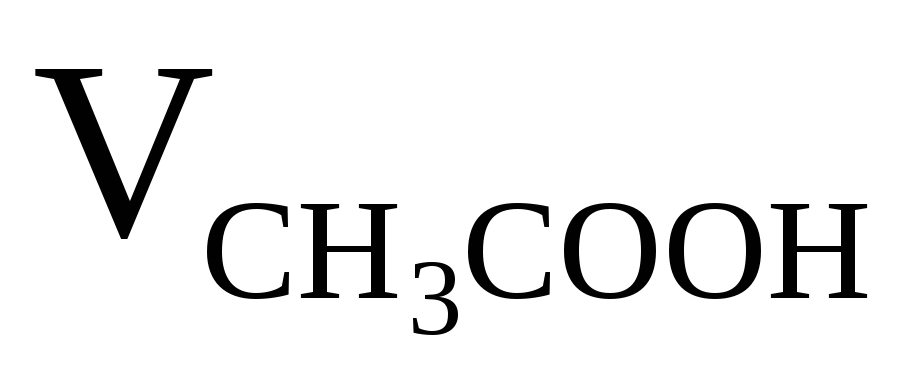 ,
мл
,
мл ,
мл
,
мл ,
М
,
М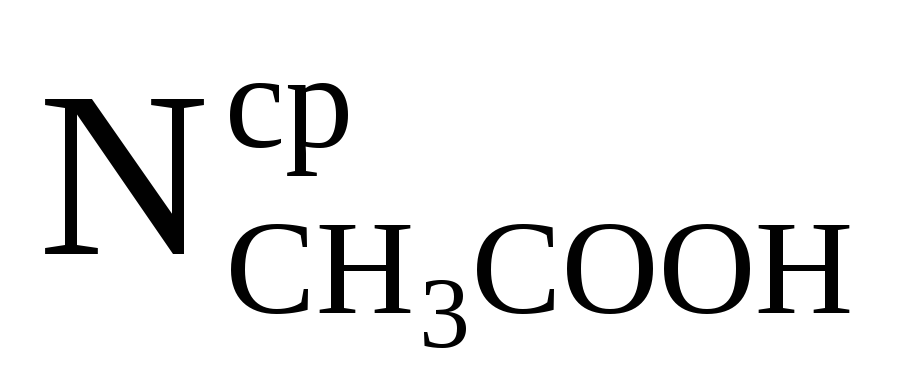 ,
М
,
М1
10
28.7
0.3157
2
10
28.8
0.3168
0.3168
3
10
28.9
0.3179
По
уравнению
![]() (в нашем случае
(в нашем случае
![]() = 0.110 М) рассчитывают концентрацию в
каждой пробе кислоты, затем вычисляют
среднюю концентрацию задачи и проверяют
ее в лаборантской.
= 0.110 М) рассчитывают концентрацию в
каждой пробе кислоты, затем вычисляют
среднюю концентрацию задачи и проверяют
ее в лаборантской.
По истечении 40 минут отфильтровывают раствор, отбрасывая первые порции фильтрата (около 10 мл), и отбирают аликвоты (по три порции каждого раствора) из оставшегося фильтрата. Можно поступить и другим способом: поочередно, начиная с самого разбавленного раствора, из колбочек с углем, не фильтруя, отбирают аликвоту 10 мл, погружая кончик пипетки вглубь раствора, но не касаясь при этом угля. Следует отметить, что для всех шести исследуемых растворов необходимо применять один и тот же способ взятия аликвот.
Для каждой из шести колб посредством титрования следует определить равновесную концентрацию уксусной кислоты после адсорбции (С). Начинать титрование лучше всего с самого разбавленного раствора (№ 6), предварительно сполоснув дистиллированной водой пипетку на 10 мл и колбы для титрования.
Закончив измерения, необходимо вылить остатки рабочих растворов вместе с углем в соответствующую емкость, сполоснуть колбы и пипетки дистиллированной водой.
Полученные
при титровании данные, так же как при
титровании исходного раствора, записывают
в протокол опыта. Затем вычисляют
количество вещества (в ммоль), находящегося
в 50 мл до (![]() )
и после (
)
и после (![]() )
адсорбции. Следует отметить, что до
адсорбции оттитровывают только исходный
раствор, и содержание вещества (C0)
в более разбавленных растворах вычисляют,
уменьшая в два раза С0
предыдущего раствора.
)
адсорбции. Следует отметить, что до
адсорбции оттитровывают только исходный
раствор, и содержание вещества (C0)
в более разбавленных растворах вычисляют,
уменьшая в два раза С0
предыдущего раствора.
Полученные данные записывают в таблицу 20.2.
Таблица 20.2.
-
№ опыта
Количество вещества
в исходном растворе
(до адсорбции)
Количество вещества
в фильтрате
(после адсорбции)
Сорбированное количество кислоты на 1 г угля, ммоль/г
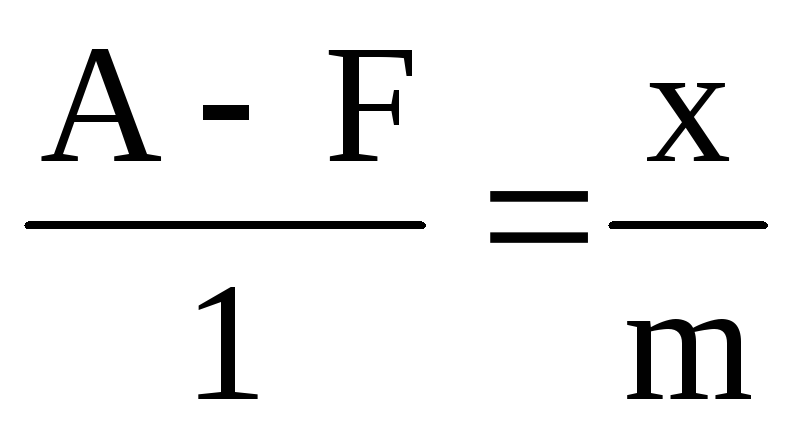
С0, М
в 50 мл, А, ммоль
С, М
в 50 мл, F, ммоль
1
0.3168
15.84
0.3028
15.14
0.7
2
0.1584
7.92
0.1463
7.315
0.605
3
0.0792
3.96
0.0715
3.575
0.385
4
0.0396
1.98
0.0352
1.76
0.22
5
0.0198
0.99
0.0187
0.935
0.055
6
0.0099
0.495
0.0093
0.45
0.045
Эти
данные используют для построения
изотермы адсорбции (рис. 20.1), откладывая
по оси абсцисс значения равновесной
концентрации С (М), а по оси ординат –
количество вещества, адсорбированное
одним граммом угля
![]() (ммоль/г).
(ммоль/г).

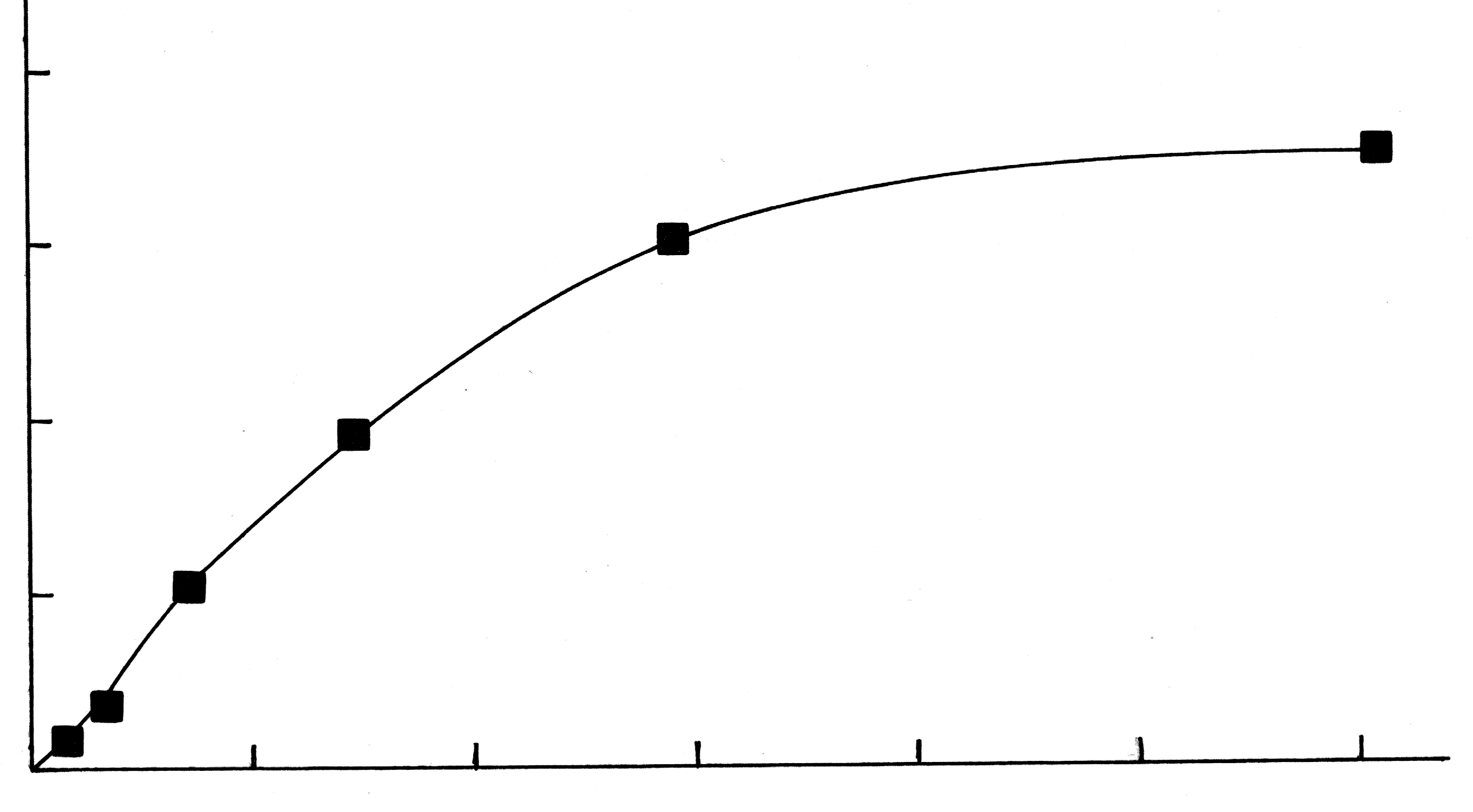
Рис. 20.1. Изотерма адсорбции.
Для
нахождения констант K
и
![]() логарифмируют уравнение Фрейндлиха:
логарифмируют уравнение Фрейндлиха:
![]() .
Выписывают в виде таблицы 20.3 значения
.
Выписывают в виде таблицы 20.3 значения
![]() и lg
C.
Нанося значения
и lg
C.
Нанося значения
![]() по оси ординат, а по оси абсцисс – lg
C,
получают прямую, не проходящую через
начало координат, подобную изображенной
на рис. 20.2. Отрезок, отсекаемый прямой
на ординате, дает, с учетом масштаба,
значение lg
K,
а тангенс угла наклона прямой к оси
абсцисс – величину
по оси ординат, а по оси абсцисс – lg
C,
получают прямую, не проходящую через
начало координат, подобную изображенной
на рис. 20.2. Отрезок, отсекаемый прямой
на ординате, дает, с учетом масштаба,
значение lg
K,
а тангенс угла наклона прямой к оси
абсцисс – величину
![]() .
В протоколе следует рассчитать и указать
значения констант K
и
.
В протоколе следует рассчитать и указать
значения констант K
и
![]() уравнения Фрейндлиха.
уравнения Фрейндлиха.
Таблица 20.3.
-
№ опыта
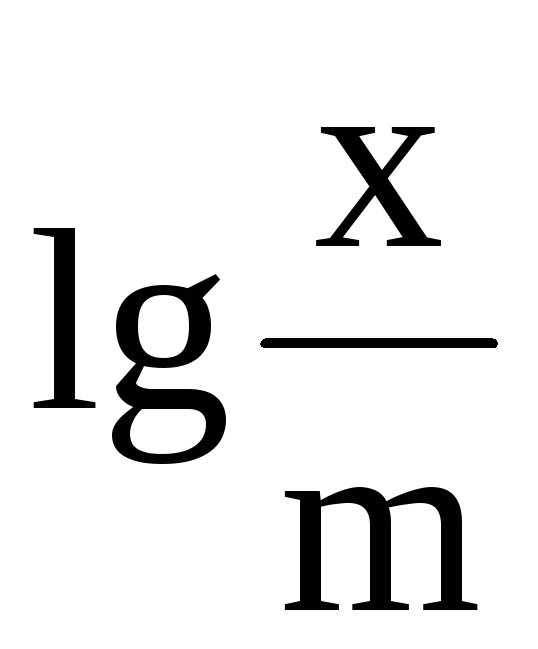
lg C
1
0.15
0.527
2
0.2182
0.835
3
0.4145
1.146
4
0.658
1.453
5
1.259
1.744
6
1.34
2.05

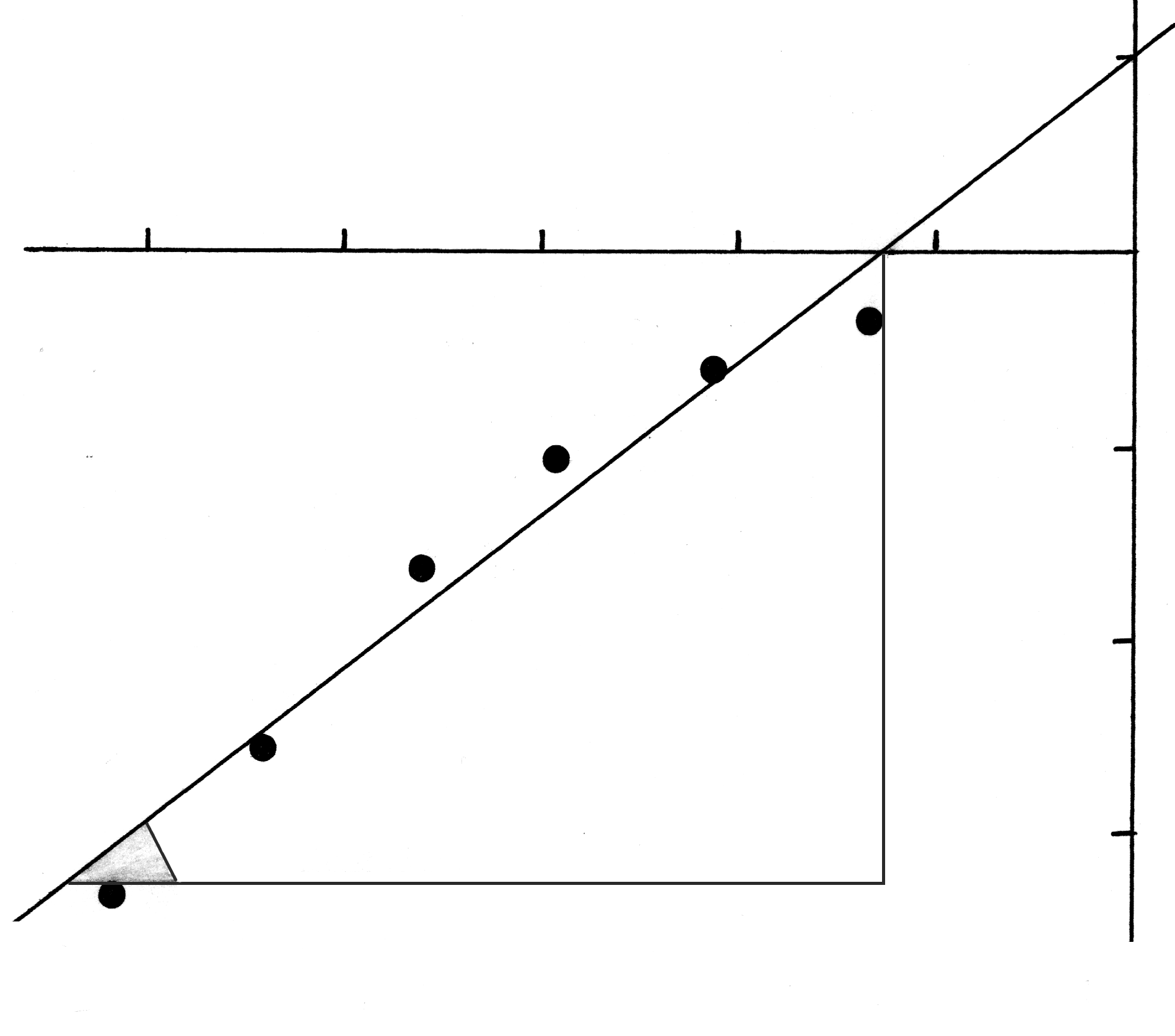
Рис.20.2. Определение констант уравнения Фрейндлиха.
В
нашем случае
![]() =
0.783 и lg
K
= 0.4; следовательно, K
= 2.51 ммоль = 2.51.103
моль, и уравнение Фрейндлиха имеет вид:
=
0.783 и lg
K
= 0.4; следовательно, K
= 2.51 ммоль = 2.51.103
моль, и уравнение Фрейндлиха имеет вид:
![]() .
.
