
- •Работа 1. Седиментационный анализ суспензий методом непрерывного взвешивания осадка.
- •Работа 20. Применение уравнения Фрейндлиха к адсорбции органических кислот на твердых адсорбентах.
- •Работа 32. Определение электрокинетического потенциала мембран методом электроосмоса.
- •Работа 39. Очистка коллоидных растворов и суспензий от электролитов методом электродиализа.
- •Работа 40а. Исследование зон коагуляции с помощью фотоэлектроколориметра.
- •Работа 48. Исследование процесса набухания твердых полимеров.
Работа 40а. Исследование зон коагуляции с помощью фотоэлектроколориметра.
Коагулированный золь обладает бóльшим светорассеянием (бóльшей мутностью) по сравнению с некоагулированным золем. Это может быть использовано для определения зон коагуляции оптическим методом с помощью фотоэлектроколориметра (ФЭКа).
Зависимость мутности золя τ от концентрации коагулирующего электролита (иона) изображена на рис. 40а.1.

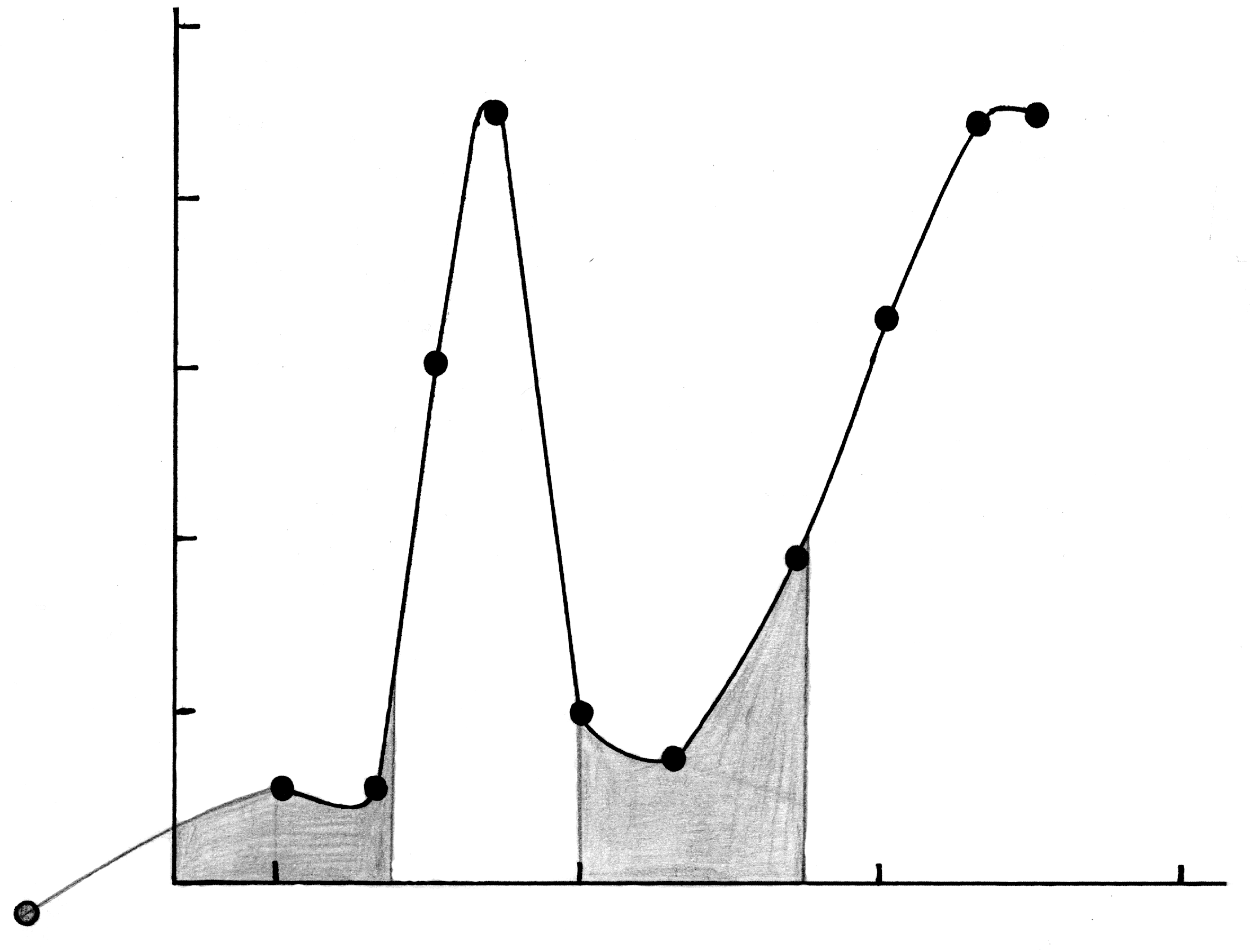
Рис.40а.1. Зависимость мутности золя от логарифма концентрации коагулирующего иона.
В зоне I золь устойчив и величина τ имеет небольшое значение. Увеличение концентрации коагулирующего иона приводит к коагуляции золя (II зона), однако дальнейший рост концентрации коагулирующего электролита приводит к перезарядке золя, и появлению новой зоны устойчивости золя (III зона). Наконец, при еще бóльших концентрациях коагулирующего иона наступает вторая зона коагуляции (IV зона), связанная со сжатием двойного электрического слоя, существующего вокруг частиц.
В данной работе исследуют зоны коагуляции или так называемые “неправильные ряды” на примере коагуляции отрицательно заряженного золя AgJ раствором Al(NO3)3 в области концентраций 106 3.104 М. Золь получают непосредственно в кювете, в которой в дальнейшем производится измерение оптической плотности D.
Золь для каждого измерения готовится заново, и объем золя в кювете всегда составляет 21 мл. При этом компоненты в кювету наливают, строго соблюдая указанный порядок: сначала в кювету наливается необходимое количество дистиллированной воды, затем добавляют раствор Al(NO3)3 из соответствующей пробирки (см. таблицу 40а.1), 10 мл раствора AgNO3 и 10 мл раствора KJ (объем получающегося золя в кювете всегда составляет 21 мл).
Растворы AgNO3 и KJ необходимой концентрации находятся на рабочем месте в бюретках, растворы Al(NO3)3 с концентрациями 2.1.104, 2.1.103, 2.1.102 М – в трех отдельных пробирках, пронумерованных по возрастанию концентрации. Общий объем воды и раствора нитрата алюминия составляет 1 мл, а соотношение между ними задано в таблице 40а.1. Требуемое количество воды и раствора Al(NO3)3 рекомендуется вливать в кювету по разности начального и конечного объемов раствора в пипетке. Для выполнения работы выдаются две пипетки: одна для воды и вторая – для Al(NO3)3, причем перед выполнением работы обе пипетки промываются.
После смешения всех четырех компонентов включают секундомер и содержимое кюветы тщательно перемешивают, осторожно продувая грушей воздух через пипетку, носик которой подносят к поверхности раствора в кювете. Затем кювета помещается в ФЭК, и оптическую плотность D5 измеряют по три раза подряд на синем светофильтре через 5 минут после смешения растворов; при этом раствором сравнения служит дистиллированная вода (21 мл воды наливают из бюретки в оставшуюся кювету, и устанавливают ее в дальний кюветодержатель ФЭКа). После проведенных измерений золь выливается, кювета тщательно ополаскивается дистиллированной водой над сливной емкостью, и аналогичные эксперименты проводятся с бóльшими количествами коагулирующего электролита.
Полученные данные заносятся в таблицу 40а.1, проверяя каждые пять последовательных измерений оптической плотности у преподавателя.
Таблица 40а.1.
|
№ про-бир-ки |
№ опы-та |
H2O, мл |
Al(NO3)3, мл |
Сисх М |
|
lg C |
D5 |
|
τ5, см1 |
|
I |
1 |
1.0 |
0.0 |
2.1∙104 |
0 |
|
0.08 0.06 0.07 |
0.08 |
0.037 |
|
|
2
|
0.9 |
0.1 |
|
1∙106 |
6 |
0.11 0.11 0.11 |
0.11 |
0.051 |
|
|
3 |
0.8 |
0.2 |
|
2∙106 |
5.7 |
0.13 0.10 0.10 |
0.11
|
0.051 |
|
|
4 |
0.7 |
0.3 |
|
3∙106 |
5.5 |
0.22 0.21 0.23 |
0.22
|
0.101 |
|
|
5 |
0.5 |
0.5 |
|
5∙106 |
5.3 |
0.27 0.28 0.28 |
0.28
|
0.129 |
|
|
6 |
0.0 |
1.0 |
|
1∙105 |
5.0 |
0.10 0.14 0.14 |
0.13
|
0.060 |
|
II |
7 |
0.8 |
0.2 |
2.1∙103 |
2∙105 |
4.7 |
0.12 0.12 0.12 |
0.12
|
0.055 |
|
|
8 |
0.5 |
0.5 |
|
5∙105 |
4.3 |
0.19 0.17 0.15 |
0.17
|
0.078 |
|
|
9 |
0.0 |
1.0 |
|
1∙104 |
4.0 |
0.25 0.25 0.20 |
0.23
|
0.106 |
|
III |
10 |
0.8 |
0.2 |
2.1∙102 |
2∙104 |
3.7 |
0.27 0.29 0.30 |
0.29
|
0.133 |
|
|
11 |
0.7 |
0.3 |
|
3∙104 |
3.5 |
0.29 0.29 0.29 |
0.29
|
0.133 |
Результаты
трех повторных измерений усредняют,
после чего из величин
![]() вычисляются значения τ5
по формуле τ5
=
вычисляются значения τ5
по формуле τ5
=
![]() ,
где l
– толщина слоя среды (в см), через который
проходит луч в кювете (в нашем случае l
= 5 см). На основании полученных результатов
строится зависимость τ5
от логарифма концентрации коагулирующего
иона (рис. 40а.1). На графике необходимо
указать зоны коагуляции и зоны устойчивости
золя.
,
где l
– толщина слоя среды (в см), через который
проходит луч в кювете (в нашем случае l
= 5 см). На основании полученных результатов
строится зависимость τ5
от логарифма концентрации коагулирующего
иона (рис. 40а.1). На графике необходимо
указать зоны коагуляции и зоны устойчивости
золя.
