
- •ТРЕТИЧНАЯ СТРУКТУРА –
- •Max Perutz и John Kendrew –
- •Третичная структура миоглобина
- •Типы взаимодействий, стабилизирующие третичную структуру
- •Примеры нековалентных взаимодействий между аминокислотными остатками в третичной структуре
- •Гидрофобные взаимодействия
- •Ленточная модель с боковыми радикалами третичной структуры поверхностного белка вируса гепатита В (HBsAg)
- •относительная гидрофобность
- •Гидрофобный кор лизоцима
- •Водородные связи между радикалами аминокислотных остатков
- •Электростатические взаимодействия
- •ЧЕТВЕРТИЧНАЯ СТРУКТУРА –
- •Первый олигомерный
- •ЛЕНТОЧНАЯ МОДЕЛЬ ГЕМОГЛОБИНА
- •3-мерная модель гомодимера поверхностного белка вируса гепатита В (HBsAg)
- •Электростатические взаимодействия между субъединицами в гемоглобине
- •Структура гема
- •Изменение конформации гемоглобина при связывании кислорода
- •Некоторые примеры свойств мультимерных белков
- •Надмолекулярные структуры – капсиды вирусов
- •Определение пространственной структуры белков
- •Крио-электронная микроскопия
- •Атомная силовая микроскопия (AFM, SFM)
- •Спектроскопия ЯМР
- •ДЕНАТУРАЦИЯ И
- •Денатурация – нарушение нековалентных взаимодействий в белках и разрушение дисульфидных связей
- •ФАКТОРЫ ДЕНАТУРАЦИИ
- •Рибонуклеаза:
- •Денатурированное
- •Формирование третичной структуры белка
- •Самопроизвольность протекания любого процесса оценивают с помощью изменения свободной энергии Гиббса
- •«спонтанная» реакция
- •Экспериментально рассчитанное изменение свободной энергии для фолдинга 7 анкириновых повторов Notch- рецептора
- •Этапы свертывания полипептидной цепи
- •Структурные домены сворачиваются отдельно
- •Внутри домена можно выделить ядро свертывания
- •Проблемы фолдинга
- •Динамическая флуоресцентная деполяризация – метод исследования фолдинга белков
- •Котрансляционный фолдинг белков
- •УЧАСТИЕ ШАПЕРОНОВ В ФОЛДИНГЕ БЕЛКОВ
- •Участие шаперонов в фолдинге белков
- •ФОЛДИНГ БЕЛКОВ С УЧАСТИЕМ ШАПЕРОНИНОВ
- •Пространственная
- •Возможные причины нарушения процесса сворачивания (фолдинга) белка
- •НАРУШЕНИЯ ФОЛДИНГА: ПРИОННЫЕ БОЛЕЗНИ
- •Модели прионного перехода

ТРЕТИЧНАЯ СТРУКТУРА –
УКЛАДКА ВТОРИЧНЫХ СТРУКТУР ОДНОЙ ПОЛИПЕПТИДНОЙ ЦЕПИ В ГЛОБУЛУ
(ПОЛНАЯ ПРОСТРАНСТВЕННАЯ СТРУКТУРА ПОЛИПЕПТИДНОЙ ЦЕПИ)
ТРЕТИЧНАЯ СТРУКТУРА СТАБИЛИЗИРУЕТСЯ
НЕКОВАЛЕНТНЫМИ
СВЯЗЯМИ

Max Perutz и John Kendrew –
рентгеноструктурный анализ миоглобина и гемоглобина (1958 - 1959)

Третичная структура миоглобина
4,5x3,5x2,5 нм
a – ленточная модель (видны вторичные стр.)
b – сетчатая (поверхность) c – поверхностный контур d – ленточная с боковыми радикалами
e – полная пространственная модель
Типы взаимодействий, стабилизирующие третичную структуру
•Гидрофобные взаимодействия между неполярными радикалами
•Водородные связи между полярными радикалами
•Электростатические взаимодействия между противоположно заряженными радикалами

Примеры нековалентных взаимодействий между аминокислотными остатками в третичной структуре
Hydrophobic interaction
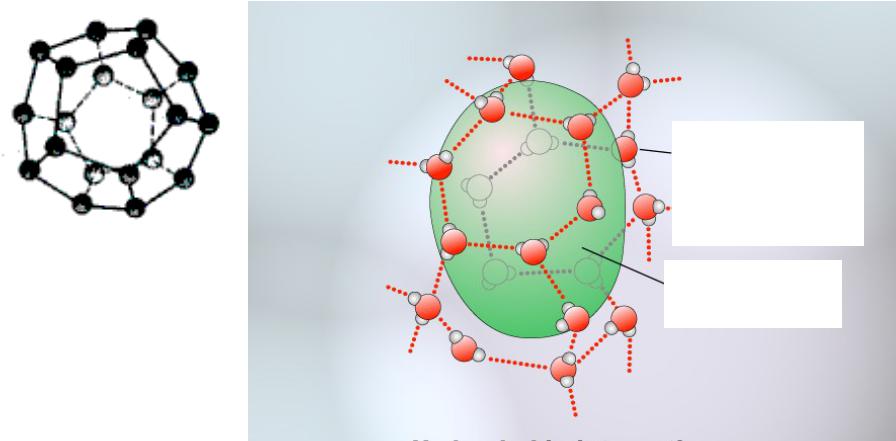
Гидрофобные взаимодействия
|
Льдоподобная |
|
|
квазикрис- |
|
|
таллическая |
|
Додекаэдр, |
структура воды |
|
Гидрофобная |
||
образованный |
||
молекулами воды, |
молекула |
|
соединенными |
|
|
водородными связями |
|
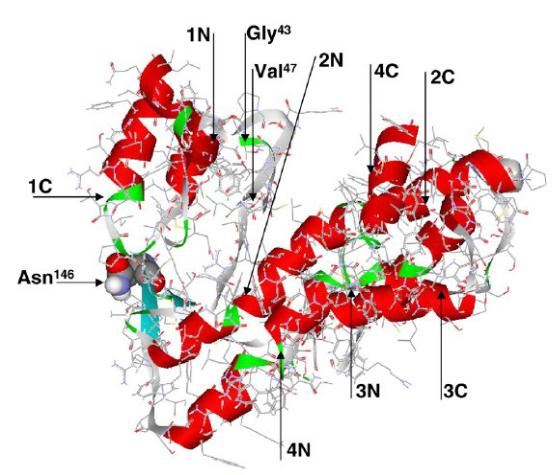
Ленточная модель с боковыми радикалами третичной структуры поверхностного белка вируса гепатита В (HBsAg)
1: Gly7–Ile28,
2: Phe80–Leu97,
3: Phe170–Trp191
4: Gly202–Trp223
Гидрофобные а.к.:
Аланин
Валин
Лейцин
Изолейцин
Метионин
Фенилаланин
Триптофан
Пролин

относительная гидрофобность
положение аминокислотного остатка
Значения выше 0.679 – гидрофобные а.к.о. (красные);
Значения ниже 0.583 - гидрофильные а.к.о. (синие);
Промежуточные – желтые
По 10 а.к.о. На N- и C-концах – вне профиля гидрофобности
(серые)
третичная структура поверхностного белка вируса гепатита В (HBsAg)

Гидрофобный кор лизоцима
 Гидрофильные а.к.о.
Гидрофильные а.к.о.
 Гидрофобные а.к.о.
Гидрофобные а.к.о.

Водородные связи между радикалами аминокислотных остатков
Тирозин
Серин
Треонин
Аспарагин
Глутамин Аспарагиновая кислота Глутаминовая кислота Гистидин
