
319_Лекции по ядерной физике 1_7
.pdfМіністерство освіти і науки, молоді та спорту України Донецький національний університет Фізико-технічний факультет
Кафедра загальної фізики і дидактики фізики
І. М. Пустинникова
ЛЕКЦІЇ З ЯДЕРНОЇ ФІЗИКИ
(Частина 1)
для студентів фізико-технічного факультету
ЗАТВЕРДЖЕНО на засіданні вченої ради
фізико-технічного факультету Протокол № 8 від 20.04.2012
Донецьк ДонНУ 2012
УДК 378. 147:53 (076.1) П 893
Рецензент:
Зуйкова З. Г. – канд. фіз.-мат. наук, доц. кафедри загальної фізики та дидактики фізики
Пустинникова І.М.
П 893 Лекції з ядерної фізики (для студентів фізико-технічного факультету) (Ч.1) / І. М. Пустинникова – Донецьк: ДонНУ, 2012. – 71 с.
Посібник містить матеріал, що викладається автором для студентів спеціальності «Фізика». Матеріал, наведений у посібнику, відповідає програмі цієї спеціальності. Викладання проводиться на посильному для студентів рівні з необхідним використанням математичного апарата.
Для викладачів, студентів і усіх, хто цікавиться ядерною фізикою.
УДК 378. 147:53 (076.1)
© Пустинникова І. М., 2012 © ДонНУ, 2012
Зміст |
|
Лекція 1 ВСТУП. ЗАГАЛЬНІ ВЛАСТИВОСТІ АТОМНИХ ЯДЕР. |
|
ОСНОВНІ ХАРАКТЕРИСТИКИ ЯДЕР.................................................................... |
4 |
Масштаби величин, характерних для світу елементарних частинок.................. |
9 |
Розміри атомних ядер ............................................................................................ |
11 |
Лекція 2 ЕНЕРГІЯ ЗВ’ЯЗКУ ЯДЕР. МОДЕЛІ АТОМНИХ ЯДЕР....................... |
13 |
Енергія зв’язку ядер............................................................................................... |
13 |
Моделі атомних ядер.............................................................................................. |
17 |
Лекція 3 ФОРМУЛА ВЕЙЦЗЕККЕРА.................................................................... |
24 |
Недоліки краплинної моделі................................................................................. |
35 |
Лекція 4 ЯДЕРНІ СИЛИ............................................................................................ |
37 |
Основні характеристики ядерних сил.................................................................. |
38 |
Фізичні обґрунтування мезонної теорії ядерних сил.......................................... |
49 |
Лекція 5 СТРУКТУРА НУКЛОНА.......................................................................... |
55 |
Лекція 6 ЕЛЕМЕНТАРНА ТЕОРІЯ ДЕЙТРОНА.................................................. |
58 |
Магнітний момент дейтрона................................................................................ |
61 |
Лекція 7 ОБОЛОНКОВА МОДЕЛЬ ЯДРА............................................................. |
62 |
3
Лекція 1
ВСТУП. ЗАГАЛЬНІ ВЛАСТИВОСТІ АТОМНИХ ЯДЕР. ОСНОВНІ ХАРАКТЕРИСТИКИ ЯДЕР
Субатомна фізика – це фізика атомних ядер і елементарних частинок. Ядерна фізика вивчає структуру атомних ядер, властивості ядерних сил, за-
кони зміни й перетворення ядер при розпаді і ядерних реакціях, взаємодію ядерного випромінювання зречовиноюй елементарні частинки. Ядерна фізика– наука про будову, властивості й перетворення атомного ядра.
У 1896 р. Анрі Беккерель відкрив природну радіоактивність солей урану, що проявляється в самодовільному випромінюванні невидимих променів, здатних викликати іонізацію повітря й почорніння фотоемульсій, той же ефект пізніше був виявлений у торію, полонію, радію.
Детальне експериментальне вивчення радіоактивних випромінювань було зроблено Резерфордом. Він показав, що радіоактивні випромінювання складаються із трьох типів променів, названих відповідно -, - і -променями. Пізніше з'я- сували, що -промені складаються із двічі іонізованих атомів гелію, -промені складаються з електронів, а -промені є електромагнітним випромінюванням.
У1904 р. Томсон запропонував першу модель атома, відповідно до якої атом являє собою позитивно заряджену кулю розміром 10–8 см зі зваженими всередині неї електронами.
Приблизно в той же час Хантаро Нагаока запропонував «модель Сатурна», відповідно до якої електрони обертаються в атомі по орбітах навколо розташованого в центрі позитивно зарядженого тіла, подібно тому як кільця обертаються навколо Сатурна або планети навколо Сонця. Але це необхідно було підтвердити експериментально.
У1909 р. у дослідах з вивчення розсіювання -частинок на тонких металевих плівках було виявлено, що поряд з розсіюванням на малі кути, що відпові-
дає розрахункам кулонівської взаємодії -частинок з атомом Томсона, у деяких випадках -частинки зазнають відхилення на дуже великі кути (більше 90º).
Наприклад,припроходженніпучкаα-частинок,щомаютьшвидкість1,8·109см/с ( 6 % від швидкості світла), через шар золота товщиною 4·10–5 см у середньому одна частинка з 20000 відхилялася (або, що те ж саме, розсіювалася) на кут порядку 90º, хоча найбільш імовірний кут, на який розсіюються α-частинки, становить 0,87º. Центральна гранична теорема (з теорії ймовірностей) дає формулу для ймовірності будь-якого значення величини, обумовленої великим числом статистично незалежних малих приростів, кожний з яких може бути як додатним, так і від’ємним. Відповідно до цієї формули, імовірність значення, що більш ніж у 100 разів (90º/0,87º >100) перевищує найбільш імовірне значення деякої вели-
4
чини (або, строго кажучи, більш ніж у 100 разів перевищує її середньоквадратичне відхилення), становить усього 3·10–2174. Резерфорд вирішив, що розсіювання на великі кути можна пояснити, припустивши, що -частинки відхиляються на великий кут в одиничному зіткненні з атомом. Розрахунки, які будуть виконані трохи пізніше (див. Розміри атомних ядер), дозволили Резерфорду оцінити, що розсіювання -частинок на великий кут було викликано зіткненнями не з об'єктами розмірами порядку розмірів самого атома, а з частинками приблизно в тисячу разів менше атома. Причому ці частинки повинні бути заряджені позитивно, оскільки негативно заряджені електрони дуже легкі, щоб настільки сильно вплинути на рух -частинки, що зіткнулася з ними.
У 1911 р. Резерфорд запропонував нову модель атома, відповідно до якої атом являє собою центральне важке позитивно заряджене ядро дуже малих розмірів (≈ 10–12 см) з розподіленими довкола нього на відносно великих відстанях (≈ 10–8 см) електронами. Оскільки маса електронів дуже мала, то вся маса атома практично зосереджена в ядрі. Електрони обертаються навколо ядра й утримуються поблизу нього електричними силами на відстанях, якими й визначається розмір усього атома. Оскільки атоми електрично нейтральні, то атомний номер Z, що визначає заряд ядра й хімічні властивості елементів, дорівнює числу електронів зовнішньоїоболонки.
Ядерна модель атома Резерфорда прекрасно пояснює результати дослідів з вивчення розсіювання -частинок. Вона за своєю будовою нагадує Сонячну систему, тому її ще називають планетарною.
Однак з погляду класичної фізики не можна пояснити існування стабільних атомів, використовуючи ядерну модель. Відповідно до законів електродинаміки будь-який заряд, що рухається прискорено (у тому числі й електрон, що рівномірно рухається навколо ядра по колу), повинен втрачати свою енергію на випромінювання. У результаті енергія системи повинна зменшуватися, електрон повинен поступово наближатися до ядра й зрештою впасти на нього. При цьому повинна безупинно змінюватися частота обігу електрона навколо ядра й, отже, частота випромінювання, що випускається атомом. Таким чином, ядерна модель атома суперечить стійкості атомів і дискретному характеру атомних спектрів. (Сталість моделі Томсона забезпечувалася рівновагою сил взаємного відштовхування електронів і притягання їх позитивно зарядженою кулею). Для усунення протиріч Н. Бор у 1913 р. запропонував квантову теорію атомних процесів. Він сформулював постулат про існування в атомі стаціонарних електронних орбіт з певним моментом імпульсу, кратним сталій Планка
meVr=nħ,
5
де me – маса електрона, V – швидкість електрона, r – радіус орбіти, n – ціле число, називане головним квантовим числом (n = 1, 2, 3, ...), ħ = 1,05·10–34 Дж·c – стала Планка. За припущенням Бора, електрони, що перебувають на цих орбітах, не втрачають енергію на випромінювання. Перехід же електрона з однієї стаціонарної орбіти на іншу (за Бором) повинен супроводжуватися поглинанням або випромінюванням порції електромагнітної енергії у вигляді кванта світла частоти v і енергії
hv = En –Em ,
де En і Em – енергії електрона на n-й і m-й стійкій орбіті.
Але й теорія Бора містила протиріччя. З одного боку, Бор припускав, що класичні принципи механіки й електродинаміки є правильні й електрон має звичайні властивості зарядженої корпускули. З іншого боку, стверджувалося, що для електрона в атомі існують деякі виключення, що нез'ясовно суперечать класичним уявленням.
Ці труднощі були переборені в 1926 р., після того як Гейзенберг і Шредингер створили нову теорію – квантову механіку. Закони квантової механіки в макросвіті зводяться до законів класичної фізики, але в мікросвіті відповідають зовсім новимвластивостям частинок.Як показуєквантова механіка, не існуєтаких станів мікрочастинки, в яких вона мала б одночасно точно визначені положення і швидкість. Наприклад, при русі електрона в атомі не можна говорити про його траєкторію. Замість цього стан частинок у мікросвіті варто описувати так називаною хвильовою функцією. Для кожної конкретної системи вона може бути знайденаяк розв’язок хвильового рівняння Шредингера. Замість старої моделі атома була запропонована нова, у якій положення електрона в атомі в деякий момент часу визначається не точно, а з деякою ймовірністю, що задається квадратом модуля хвильової функції.
Квантова механіка не тільки підтвердила теорію Бора, але й пояснила, чому атом не випромінює в стаціонарному стані, дозволила підрахувати інтенсивності спектральних ліній, дала пояснення явищу дифракції електронів тощо.
У 1919 р. Резерфорд спостерігав розщеплення ядер різних речовин при бомбардуванні їх α-частинками. При цьому з ядер вилітали позитивно заряджені частинки із зарядом +е й масою, рівною масі ядра атома легкого ізотопу водню (яка дорівнює 1836,15 me). Тим самим було доведено, що в складі різних ядер утримуються найпростіші водневі ядра, які стали називати протонами й позначати символом р.
Після відкриття протонів фізикам здавалося, що ядро побудоване зА протонів і (A – Z) електронів, а навколо ядра на відстані порядку 10–8 см обертаються Z електронів. У цій моделі одержав природне пояснення факт пропорційності мас атомів елементів масовому числу А і зарядів ядер порядковому номеру Z.
6
Однак така гіпотеза суперечила експериментальним фактам, що відносяться до спінів і магнітних моментів ядер. Крім того, присутність електронів усередині ядра виявилося неможливим поєднати із принципом невизначеності Гейзенберга.
У 1932 р. (на підставі дослідів Боте, Беккера, подружжя Жоліо-Кюрі) Чедвик довів існування електрично нейтральної частинки з масою, майже такою ж, як у протона (mn = 1838,68me). Ця частинка була названа нейтроном і позначається символом n.
Основна різниця між протоном і нейтроном полягає в тому, що протон – позитивно заряджена частинка, заряд якої е = 1,60219· 10–19 Кл. Це елементарний заряд, який чисельно дорівнює заряду електрона. Нейтрон же електрично нейтральний. Спіни протона й нейтрона однакові й рівні спіну електрона, тобто 1 2 (в одиницях ħ), – обидві частинки є ферміонами й підкоряються статистиці Фермі-Дірака, тобто для них виконується принцип Паулі, відповідно до якого в кожному квантовому стані окремої частинки в складній зв'язаній системі (ядро, атом) не може перебувати одночасно більше однієї частинки.
2 (в одиницях ħ), – обидві частинки є ферміонами й підкоряються статистиці Фермі-Дірака, тобто для них виконується принцип Паулі, відповідно до якого в кожному квантовому стані окремої частинки в складній зв'язаній системі (ядро, атом) не може перебувати одночасно більше однієї частинки.
Магнітний момент протона позитивний і в 660 разів менше магнітного моменту електрона, магнітний момент нейтрона негативний і в 1000 разів менше магнітного моменту електрона.
Маси протона mр і нейтрона mn майже однакові: mр =1836,15me, mn =1838,68mе, де me = 9,1095· 10–28 г – маса електрона.
Маса частинки пов'язана з її повною енергією співвідношенням Ейнштейна Е = mс2. Тому в субатомній фізиці масу прийнято вимірювати в одиницях енергії, причому за одиницю енергії приймають мегаелектронвольт (МеВ). У цих одиницях me = 0,511 МеВ, mр = 938,28 МеВ, mn = 939,55 МеВ. При цьому під масою розуміють масу спокою частинки. Прийнято так само масу частинки вимірювати в так званих атомних одиницях маси (а. о. м.). За атомну одиницю маси приймають 1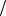 12 частину маси нейтрального атома вуглецю 12С. Легко підраху-
12 частину маси нейтрального атома вуглецю 12С. Легко підраху-
вати, що 1 а. о. м. = 931,50 МеВ (mр = 1,00759 а. о. м., mn =1,00898 а. о. м.).
Оскільки енергія спокою нейтрона більше суми енергій спокою протона й електрона, то енергетично можливий розпад нейтрона на протон і електрон. Такий розпад був виявлений у 1950 р. радянськими фізиками П.Є. Співаком і О.М. Сосновським, канадським фізиком Робсоном і американським фізиком Снеллом.
n p e ~e. |
(1.1) |
Нейтрон розпадається на протон, електрон і електронне антинейтрино. Його період піврозпаду дорівнює T1/2 12 хв.
Незабаром після відкриття нейтрона радянський фізик Д.Д. Іваненко й німецький фізик В. Гейзенберг висловили гіпотезу про протон-нейтронну будову ядра. За цією моделлю всі ядра складаються із двох видів елементарних частинок, на-
7
зиваних нуклонами, – протонів і нейтронів. Повне число нуклонів визначає масу ядра А, число одних протонів – заряд ядра Z.
Вільний протон – стабільна частинка. Однак усередині ядра протон не вільний і може розпадатися на нейтрон, позитрон і електронне нейтрино.
(1.2)
Питання про те, яка частинка – протон або нейтрон – більш елементарна, позбавлене фізичного сенсу. Обидві вони є елементарними, але взаємно перетворюються одна в одну. У вільному стані нейтрон радіоактивний, а протон стабільний,тобтойдепроцес(1.1).Усерединіж ядраможливіобидвапроцеси(1.1) і(1.2).
Кількість протонів у ядрі (зарядове число) прийнято позначати черезZ, кількість нейтронів – через N. Їхня сума A = Z + N називається масовим числом ядра; число Z збігається з порядковим номером елемента в таблиці Менделєєва. Тому число Z також називають атомним номером ядра.
Ці характеристики ядра відбиті в символічних позначеннях, які будуть використані надалі у вигляді ZA X (або Z X A ), де X – назва елемента, атому якого на-
лежить ядро, наприклад, ядро літію 3Li7. Надалі ядро, що містить А нуклонів і Z протонів, будемо позначати (A, Z), його масу Мяд(A, Z) або простоM(A, Z), а масу відповідного атома Maт(A, Z). У тих випадках, коли треба вказати хімічний символ
елемента, для маси ядра або атома будемо використовувати позначення Mяд(ZXА),
M(ZXА) і Maт(ZXА).
Протон і нейтрон досить подібні між собою. Тому їх називають загальним найменуванням – нуклон і кажуть, що нуклон може перебувати у двох станах: протон і нейтрон, що відрізняються своїм відношенням до електромагнітного поля, оскільки єдина істотна відмінність полягає в тому, що протон заряджений, а нейтрон– нейтральний. Ця подібність,що має фундаментальне значення в ядерній фізиці, з особливою виразністю проявляється у властивостях «дзеркальних» ядер. Дзеркальними називають два ядра з однаковими масовими числамиА, кожне з яких виходить із іншого заміною всіх протонів нейтронами, а всіх нейтро-
нів – протонами. Прикладом такої пари можуть бути самі протон і нейтрон. Ін-
шими прикладами є: 1Н3 і 2Не3; 4Ве7 і 3Li7; 5B11 і 6С11; 6С13 і 7N13; 7N15 і 8O15; 8O17 і
9F17; 14Si29 і 15Р29 тощо (більш важке ядро в кожній із цих пар радіоактивне). Атоми з однаковими Z (тобто атоми того самого елемента), але різними N
називають ізотопами, з однаковими А, але різними Z – ізобарами, з однаковими N, але різними Z – ізотонами. Існують радіоактивні ядра з однаковими Z і А, що відрізняються періодом піврозпаду. Їх називають ізомерами.
Поряд з терміном ядро атома використовують термін нуклід. Трьом атомам ізотопу водню 11H , 12H і 13H привласнені різні назви – відповідно водень, дейтерій і тритій, а ядрам дейтерію й тритію – дейтрон (d) і тритон (t).
8
У природі зустрічаються елементи з атомним номером Z від 1 до 92, крім технецію(Тс, Z=43) і прометію(Pm, Z= 61).Плутоній (Pu,Z =94) після одержання його штучним шляхом був виявлений у незначних кількостях у природному мінералі– смолянійобманці.Інші трансуранові (тобто зауранові) елементи (зZ від 93 до 107) були отримані штучним шляхом за допомогоюрізних ядерних реакцій.
Масштаби величин, характерних для світу елементарних частинок
Довжина Поперечникатома~10–8 см–характеризуєрадіусорбітизовнішніхелектронів.
Розміриядра–10–12 ÷10–13 см.
Відстань 10–13 см = 10–15 м = 1 фм (фемтометр) одержала назву 1 Фермі. Зараз експериментально розрізняють відстані до 0,01 (0,1) Фермі.
Різні методи визначення розмірів ядер можна розділити на дві групи. В одних методах реєструється наявність ядерної речовини – в них використовують явища, обумовлені ядерними силами. В інших використовують електромагнітні взаємодії й досліджують розподіл електричного заряду в ядрі. Розходження між результатами вимірів розмірів ядра різними методами не великі. Коли не потрібна особлива точність, можна говорити про «розміри ядра» взагалі, не уточнюючи, про яку величину йде мова.
У першому наближенні ядро можна вважати кулею, радіус якої визначається формулою
R = r0A1/3. |
(1.3) |
Для постійної r0 для важких ядер різними методами виходять результати, |
|
що трохи відрізняються, але всі вони лежать у межах r0 = (1,2 ÷ 1,5)10–13 см. |
|
Часто(1.3) записуютьувигляді |
|
R=1,3А1/3 фермі. |
(1.4) |
З (1.4) випливає, що об'єм ядра пропорційний числу нуклонів у ядрі. Таким чином, густина речовини у всіх ядрах приблизно однакова.
Площа
Площі геометричних перетинів ядер, рівні πR2, для більшості ядер близькі до величини 10–24 см2. Тому в ядерній фізиці для виміруплощ приймається одиниця
1 барн =10–24см2.
Енергія Один електронвольт (1 еВ) відповідає енергії, що набуває або втрачає час-
тинка з елементарним електричним зарядом при проходженні неюрізниці потенціаліву1В,тобто
1еВ=1,6·10–19 Кл·1В=1,6·10–19 Дж.
Більшими одиницями енергії є мегаелектронвольт– 106 еВ (МеВ) і гігаелектронвольт 109 еВ (ГеВ).
9

Швидкість
Абсолютною межею швидкостей всіх рухів є швидкість світла у вакуумі c =3·108 м/с.
Зі швидкістю світла поширюються електромагнітні хвилі й нейтрино, якщо вони не мають маси. Інші елементарні частинки, що мають масу, можуть мати швидкість, як завгодно близьку до швидкості світла, але завжди меншуза неї.
Теорія відносності дозволяє розрахувати кінетичну енергію частинки, що рухається зі швидкістю, яку можна порівняти зі швидкістю світла:
|
|
т |
с2 |
|
||
Т |
|
е |
|
|
тес2 |
, |
|
|
|
|
|||
|
|
|
||||
|
1 |
V 2 |
|
|||
|
с2 |
|
||||
|
|
|
|
|||
де те – маса спокою електрона.
При енергії 1 МеВ швидкість електрона становить 94 % швидкості світла. Швидкість світла й вибирають як величину, що характеризує масштаб швидкостей у мікросвіті.
Час Якщо оцінити час, за який частинка, рухаючись зі швидкістю світла
(3 ·108 м/с), перетне ядро по діаметру(10–14 м),то
31010148 3 10 23с.
Час10–23сприйнятоназиватиядернимчасом.
Маса За одиницю маси елементарних частинок приймають масу спокою елект-
рона me = 9,1095· 10–31 кг. Якщо її виразити в енергетичних одиницях, то масі спокою електрона відповідає власна енергія, що дорівнює
mec2 9,1095 10 31 (2,9979 108 )2 0,511 МеВ. 1,60219 10 19 106
Маса ядра й атома в ядерній фізиці вимірюється в атомних одиницях маси. Щоб виразити значення атомної одиниці маси в грамах, треба взяти обернену величину від числа Авогадро
|
1 |
|
1 |
–24 |
1 а. о. м. = |
|
|
|
=1,66056· 10 габо931,502МеВ. |
NА |
6,023 1023 |
Якщо вимірювати масу ядра в атомних одиницях маси, то вона близька до маси протона, помноженої на масове число А (похибка результату – 0,1÷1 %).
10
