
- •Министерство транспорта Российской Федерации
- •Подписано в печать . Формат 60х90 1/16.
- •Введение
- •1. Эквивалент. Закон эквивалентов
- •Примеры решения задач
- •2. Строение атомов
- •3. Периодическая система химических элементов
- •4. Химическая связь
- •Примеры решения задач
- •5. Энергетика химических процессов
- •Примеры решения задач
- •6. Химическое сродство Примеры решения типовых задач
- •Поскольку rН0, rS0 и rG0 реакции связаны друг с другом уравнением:
- •7. Скорость химических реакций Примеры решения типовых задач
- •8. Химическое равновесие Примеры решения типовых задач
- •9. Коллигативные свойства растворов Примеры решения типовых задач
- •10. Ионно-молекулярные реакции обмена Примеры решения задач
- •Решение. В насыщенном растворе сульфата свинца существует гетерогенное равновесие:
- •Решение.
- •Решение.
- •12. Окислительно – восстановительные реакции
- •Примеры решения задач
- •Основные типы окислительно-восстановительных реакций (овр)
- •13. Электродные процессы и гальванические элементы
- •Примеры решения задач
- •14. Электролиз Примеры решения задач
- •15. Коррозия металлов Примеры решения задач
- •16. Комплексные соединения Примеры решений типовых задач
- •Взаимодействие металлов со щелочами
- •Взаимодействие металлов с кислотами
- •18. Полимеры
- •Примеры решения задач
- •19. Дисперсные системы Примеры решений задач
- •20. Количественный анализ
- •Примеры решения задач
- •Константы нестойкости ряда комплексных ионов
9. Коллигативные свойства растворов Примеры решения типовых задач
Пример 1. Для определения относительной молекулярной массы вещества, являющегося незлектролитом, его навеска массой 1,764 г была растворена в воде, и объем раствора доведен до 100 мл. Измеренное осмотическое давление раствора оказалось равным 2,38∙10 Па при 20оС. Рассчитайте молярную массу указанного вещества.
Решение. В растворе объемом 1 м3 масса вещества составляет 17640 г. Из уравнения Вант-Гоффа, подставляя в это выражение экспериментальные данные, получим:
![]()
![]() г/моль
г/моль
Пример 2. Навеска вещества массой 12,42 г растворена в воде объемом 500 мл. Давление пара полученного раствора при 25 0С равно 3297,8 Па. Как по этим данным найти молярную массу растворенного вещества?
Решение. Для определения молярной массы растворенного вещества М1 надо вычислить количество молей растворенного вещества ν1, пользуясь законом Рауля:
![]() ,
,
где : р- давление пара над раствором;
р0 – давление пара над чистой водой, его значение при 250С согласно табл 14 []
равно 3306 Па;
ν2
=
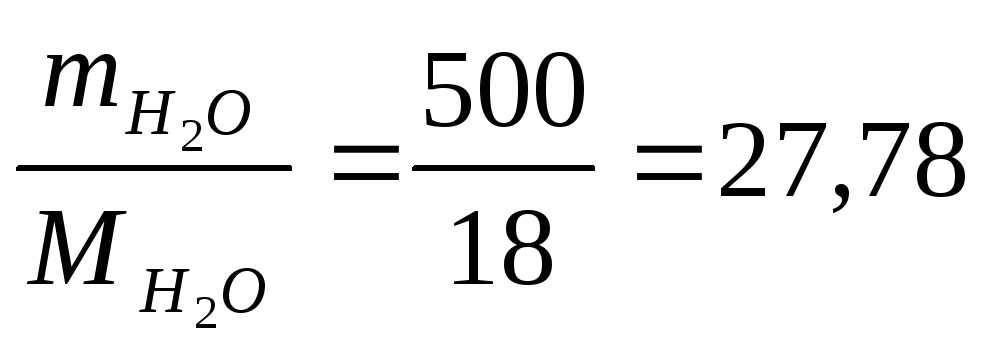 моль, после подстановки в закон Рауля
получим:
моль, после подстановки в закон Рауля
получим:
![]() ;
отсюда ν1 =
ν(вещества)
= 0,069 моль;
;
отсюда ν1 =
ν(вещества)
= 0,069 моль;
М1
=
![]() г/моль
г/моль
Пример 3. Раствор, содержащий 0,85 г хлористого цинка ZnС12 в 125 г воды, замерзает при —0,23 °С. Определите кажущуюся степень диссоциации хлористого цинка в этом растворе.
Решение. Выразим прежде всего моляльную концентрацию раствора в молях на 1000 г воды. Так как молярная масса хлористого цинка равна 136 г/моль, то
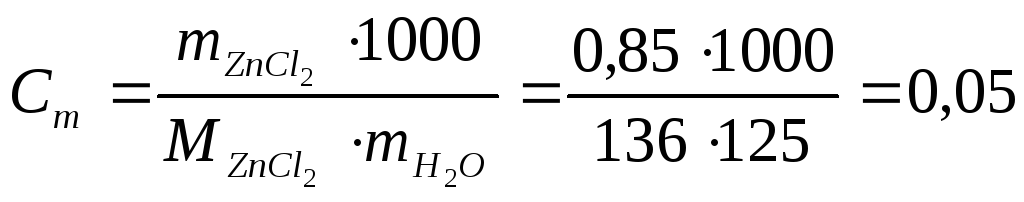 моль/кг
моль/кг
Для растворов электролитов величина понижения точки замерзания рассчитывается по формуле
∆tзам. = i∙ К∙Ст
Криоскопическая постоянная К для воды из табл.14[] равна 1,86, следовательно, изотонический коэффициент данного раствора составит:
![]()
Степень диссоциации связана с величиной изотонического коэффициента соотношением:
![]() или
73,5%
или
73,5%
Здесь п – количество ионов, образующихся при диссоциации молекулы ZnCl2.
10. Ионно-молекулярные реакции обмена Примеры решения задач
Пример 1. ПР(РbSО4) = 2,2.10-8. Чему равна концентрация ионов Рb2+иSО42-в насыщенном растворе сульфата свинца и его растворимость, выраженная молярной и массовой концентрациями?
Решение. В насыщенном растворе сульфата свинца существует гетерогенное равновесие:
РbSО4 (т)↔ Рb2+(р-р) + SО42-(р-р)
х х х
ПР(РbSО4)=
![]()
Растворимость
бинарного электролита равна молярной
концентрации каждого из его ионов: s=х
=
![]() =
=![]() 1,5
10-4
моль/л. Растворимость соли, выраженная
массовой концентрацией, равна
s∙М=
1,5 ·10-4
моль/л ·303 г/моль = 0,0455 г/л.
1,5
10-4
моль/л. Растворимость соли, выраженная
массовой концентрацией, равна
s∙М=
1,5 ·10-4
моль/л ·303 г/моль = 0,0455 г/л.
Пример 2. Составьте уравнения реакций, протекающих в водных растворах, в молекулярной, ионной и сокращенной ионной формах: 1) между сульфидом натрия и сульфатом меди (II), 2) между гидроксидом железа (III) и соляной кислотой.
