
3_1_Alkiny
.pdf
АЛКИНЫ
Л Е К Ц И Я 3

АЛКИНЫ
•К алкинам или ацетиленовым углеводородам относятся соединения, содержащие тройную углерод– углеродную связь.
•Общая формула
СnН2n-2
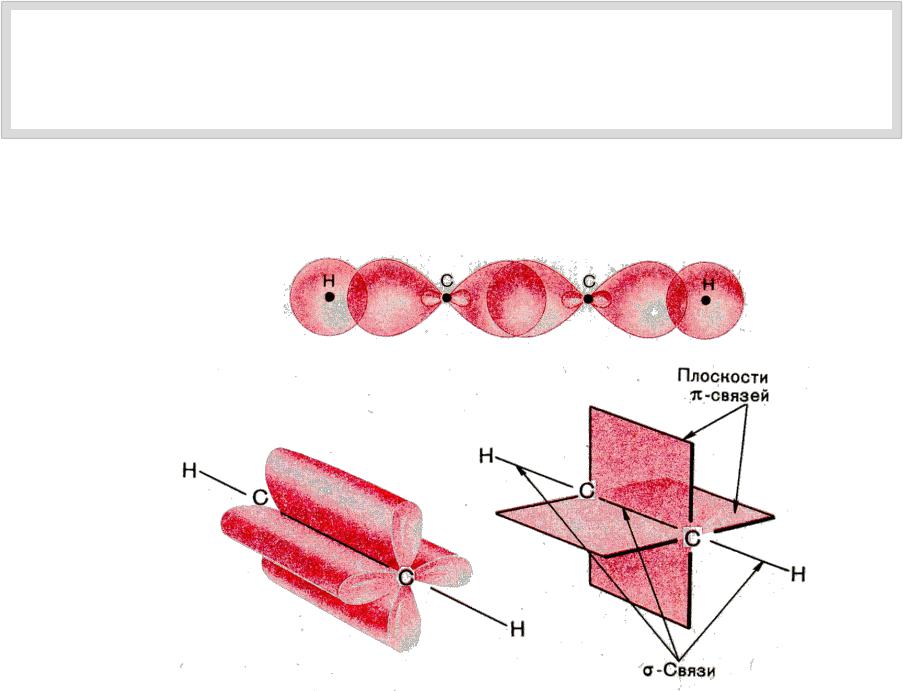
СТРОЕНИЕ
Тройная углеродная связь построена из
одной –связи и двух –связей
–связь
–связи

СТРОЕНИЕ
•Атомы углерода находятся в состоянии spгибридизации
•π-Электроны тройной связи втянуты внутрь молекулы, поэтому атомы углерода меньше экранированы с внешней стороны, поэтому присоединение протекает труднее, чем у алкенов

ПОЛУЧЕНИЕ АЦЕТИЛЕНА
• Из карбида кальция (Вёлер, 1862 г.)
CaC2  H2O
H2O  HC
HC CH
CH  Ca(OH)2
Ca(OH)2
• Пиролизом метана и этана
1500-1600 oC
2CH4  HC
HC CH
CH  3H2
3H2
C2H6 |
1200 oC |
HC CH 2H2 |

СПОСОБЫ ПОЛУЧЕНИЯ
• Из дигалогенпроизводных
H H
R C C R
Hal Hal
вицинальный
|
|
|
|
|
|
|
|
|
|
|
2KOH |
R |
|
C |
|
C |
|
R |
|
|
|
2KHal |
|
|
|
2H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
H |
Hal |
|
спирт |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
C |
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
H Hal
геминальный
СПОСОБЫ ПОЛУЧЕНИЯ
• Из тетрагалогенпроизводных
|
|
Hal |
Hal |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
2Zn |
R |
|
|
|
|
|
R |
|
|
|
2ZnHal2 |
R |
|
C |
|
C |
|
R |
|
C |
|
C |
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Hal Hal |
|
|
|
|
|
|
|
|
|
|
|
||||||
• Алкилирование ацетилена
HC CH
CH  NaNH2
NaNH2  HC
HC C Na
C Na  NH3
NH3
HC |
|
C |
|
Na |
|
|
|
R |
|
al |
HC |
|
C |
|
R |
|
|
|
NaHal |
|
|||||||||||||||||||
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|||||||||||||||||||
|
|
|
|||||||||||||||||
|
|
|
|
|

ФИЗИЧЕСКИЕ СВОЙСТВА
•Гомологи С2–С4 (за исключением 1- бутина) – газы, С5–С15 – жидкости, С15 и более – твердые вещества.
•Алкины обладают низкой полярностью и хорошо растворяются в органических растворителях.

ХИМИЧЕСКИЕ СВОЙСТВА
•Характерны реакции присоединения, полимеризации, окисления и замещения атома водорода у тройной связи.
•Реакции присоединения протекают ступенчато с образованием алкенов или их производных, затем алканов (или их производных).

ХИМИЧЕСКИЕ СВОЙСТВА
• Присоединение водорода, галогенов
СН3 С |
|
СН |
+H2 |
СН3 СН СН2 |
|
+ H2 |
|
|
СН2 |
|
СН3 |
|
|
|
|
|
|||||||
|
Pt |
|
Pt |
СН3 |
|
||||||
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
Br2 |
Br |
H Br2 |
|
|
|
||
HC |
|
CH |
C |
|
C |
CHBr2 |
|
CHBr2 |
||
|
|
|
|
|
||||||
|
|
|
|
|||||||
|
|
|
|
|
||||||
|
|
|
||||||||
|
|
|
|
H |
Br |
|
|
|
||
