
- •Введение
- •Предельные углеводороды (алканы и циклоалканы)
- •Способы получения
- •Углеводороды с двойными связями алкены
- •Диеновые углеводороды
- •Понятие об ароматичности
- •Функциональные производные
- •Галогенопроизводные
- •Физические свойства
- •Кислородсодержащие функциональные производные
- •Одноатомные спирты
- •Физические свойства
- •Применение.
- •Многоатомные спирты
- •Физические свойства
- •Применение.
- •Фенолы, нафтолы
- •Физические свойства
- •Оксосоединения. Альдегиды и кетоны.
- •Физические свойства
- •Применение.
- •Карбоновые кислоты
- •Одноосновные кислоты (насыщенные и ароматические)
- •Способы получения
- •Одноосновные ненасыщенные кислоты
- •Физические свойства.
- •Применение.
- •Двухосновные кислоты
- •Применение.
- •Функциональные производные карбоновых кислот
- •Гидроксикислоты
- •Углеводы. Определение, строение, нахождение в природе.
- •Физические свойства
- •Физические свойства
- •Азотсодержащие соединения
- •Нитросоединения
- •Физические свойства
- •Применение.
- •Диазо- и азосоединения
- •Физические свойства
- •Применение.
- •Аминокислоты
- •Классификация, изомерия
- •Химические свойства
- •Значение аминокислот
- •Пептиды
- •Гетероциклические соединения
Функциональные производные
К функциональным производным относятся органические соединения, в углеводородной цепочке которых один или несколько атомов водорода замещены на функциональные группы.
По виду и количеству функциональных групп бывают монофункциональные (одна группа), гомополифункциональные (несколько одинаковых групп) и соединения со смешанными функциями (когда группы разные).
Галогенопроизводные
Если один или несколько атомов водорода в углеводородной цепочке замещены на атом галогена, то такие функциональные производные называются галогенопроизводными.
Изомерия галогенопроизводных включает все виды изомерии углеводородов, которые связаны с галогенами, а также дополнительный вид изомерии – по положению галогена.
Галогенопроизводные классифицируются:
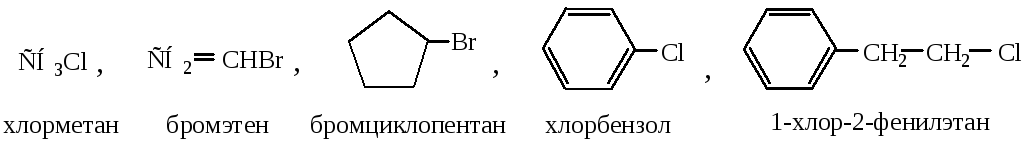
1) по типу галогена: фтор-, хлор-, бром- или йодпроизводные;
2) по типу углеводородной цепочки: насыщенные (алифатические и циклические), ненасыщенные (ациклические и циклические), ароматические (с галогенами в ядре и боковой цепочке);
1-хлорпропан (З.Н.)
пропилхлорид (Р.Ф.Н.)
1-бромэтен
винилбромид
3) по количеству
галогенов: моно-, ди- и полигалогенопроизводные.
1,2-дихлорпропан
Электронное строение галогенопроизводных.
Атом галогена обладает большей электроотрицательностью, чем углерод, поэтому связь Сδ+ → Halδ- сильно полярна из-за индуктивного эффекта (–J). Электронная плотность смещена к атому галогена:

На атоме углерода, связанном с галогеном, создается положительный заряд δ+, и на соседнем с ним атоме углерода δδ+, а также атоме водорода, с ним соединенным δδ+ (δδ+ < δ+). Поэтому этот водород (в α-положении к галогену) способен отщепляться в виде протона Н+, т.е. проявляются кислотные свойства, а галогенопроизводные легко вступают в реакции нуклеофильного замещения. Для галогенопроизводных характерны реакции, протекающие по механизмам: SN1, SN2, EN1, EN2.
СПОСОБЫ ПОЛУЧЕНИЯ
Практически все способы получения галогенопроизводных были рассмотрены при изучении химических свойств углеводородов. К ним относятся:
замещение водорода в алканах, циклоалканах, алкенах, бензоле;
присоединение галогенов к алкенам, алкинам, бензолу;
присоединение галогеноводородов к алкенам, алкинам.
К ранее неизученным методам получения галогенопроизводных относятся следующие:
1. Замена галогена на галоген:

![]()
2. Получение галогенопроизводных из спиртов действием на последние PCl3, PCl5 или SOCl2, а также сухого HCl или HBr.
2.1 Действие галогеноводородов:

Реакция может происходить также с солями в присутствии сильных минеральных кислот.
![]()
2.2 Действие галогенидов фосфора PCl3, PCl5:

2.3 Действием галогенидов тионила SOX2:
![]()
3. Геминальные дигалогенопроизводные можно получить действием PCl5 на карбонильные соединения:


