
- •«Биологическая химия» для бакалавров направления 111100.62 «Зоотехния»
- •Содержание Введение
- •Цели и задачи дисциплины
- •2. Объем дисциплины и виды учебной работы
- •3. Формы и содержание текущего и итогового контроля
- •Система рейтинговой оценки
- •Система итоговой оценки знаний
- •4. Рекомендуемая литература
- •Организация работы студента
- •II. Работа с веществами и растворами
- •III. Обращение с нагревательными приборами
- •Занятие № 1. «Основы физической и коллоидной химии»
- •Экспериментальная работа.
- •Занятие № 2. «Углеводы и липиды как биогенные соединения»
- •Экспериментальная работа.
- •Занятие № 3. «Строение и физико-химические свойства аминокислот и белков»
- •Экспериментальная работа.
- •Занятие № 4. «Ферментный катализ»
- •Вопросы к контрольной работе:
- •Экспериментальная работа.
- •Занятие № 5. «Роль витаминов в метаболизме»
- •Вопросы к контрольной работе:
- •Экспериментальная работа.
- •Занятие № 6. «Гормональная регуляция обмена веществ»
- •Экспериментальная работа.
- •Занятие № 7. Коллоквиум I: «Уровни организации биогенных соединений. Ферменты. Витамины. Гормоны»
- •Занятие № 8. «Обмен веществ и энергии»
- •Экспериментальная работа.
- •Занятие № 9. «Цикл трикарбоновых кислот»
- •Экспериментальная работа.
- •Занятие № 10. «Обмен углеводов (часть 1)»
- •Экспериментальная работа.
- •Занятие № 11. «Обмен углеводов (часть 2)»
- •Экспериментальная работа.
- •Занятие № 12. «Обмен липидов»
- •Экспериментальная работа.
- •Занятие № 13. «Липиды и биологические свойства клеточных мембран»
- •Экспериментальная работа.
- •X - содержание холестерина в калибровочном растворе, ммоль/л
- •Занятие № 14. «Белковый обмен»
- •Экспериментальная работа.
- •Расчетные методы определения биологической ценности белка.
- •Содержание незаменимых (для человека) аминокислот в некоторых видах продуктов, г на 100 г белка
- •Занятие № 15. «Биохимическая детоксикация»
- •Экспериментальная работа.
- •Занятие № 16. Коллоквиум II: «Обмен веществ и энергии»
- •Физиологические показатели обмена веществ у домашних и сельскохозяйственных животных.
- •Контрольные вопросы по курсу «Биологическая химия»
- •Биологическая химия
Занятие № 14. «Белковый обмен»
Цель занятия: изучить методы количественного определения белков; освоить расчетные методы определения биологической ценности белков.
ВОПРОСЫ К КОНТРОЛЬНОЙ РАБОТЕ:
Переваривание белков. Протеазы пищеварительного тракта, механизм их активации.
Дайте определение понятию «азотистый обмен» и расскажите, как определяется азотистый обмен. Чем вызваны различия в питательной ценности большинства белков растительной природы с одной стороны и животного происхождения с другой?
Механизм реакций трансаминирования. Биологическая роль данного процесса.
Пути декарбоксилирования аминокислот. Биологическое значение конечных продуктов этих реакций.
Дезаминирование аминокислот. Биологическое значение конечных продуктов этих реакций.
Роль ароматических аминокислот в метаболизме.
Дата выполнения ________ Балл ____ Подпись преподавателя ____________
Экспериментальная работа.
Опыт 1. Количественное определение общего белка в сыворотке крови.
В плазме крови содержится до 200 различных белковых компонентов. Большая часть выполняемой функции крови, так или иначе, связана с белками плазмы: поддержание онкотического давления, участие в процессах свертывания крови, регуляции рН крови, выполнение транспортной и защитной функции, функции «белкового резерва» и др. Качественное и количественное постоянство белкового состава крови четко поддерживается организмом, и любые изменения в этой системе, как правило, являются отражением нарушенного функционирования тех или органов и тканей.
Приборы. 1. Штатив с пробирками.
2. Набор пипеток.
3. Центрифуга.
4.Центрифужные пробирки.
5. Водяная баня.
6. ФЭК.
7. Кюветы, 10 мм.
Реактивы. 1. Сыворотка крови.
2. Трихлоруксусная кислота, 3%-ный раствор в этаноле.
3. Биуретовый реактив.
4. Хлорид натрия, 0,85%-ный раствор.
а) Определение концентрации альбуминов.
В центрифужную пробирку поместите 1,5 мл 3%-ной трихлоруксусной кислоты в этаноле.
Добавьте 0,5 мл сыворотки крови, тщательно перемешайте и через 10 мин центрифугируйте.
0,2 мл центрифугата перенесите в пробирку, содержащую 2,3 мл 0,85%-ного раствора хлорида натрия и добавьте 2,5 мл биуретового реактива.
Тщательно перемешайте и выдержите 20 мин в термостате при 37С.
Измерьте оптическую плотность при зеленом светофильтре (540-560 нм) в кювете с толщиной слоя 10 мм.
б) Определение концентрации общего белка.
0,1 мл сыворотки крови внесите в пробирку, содержащую 2,4 мл 0,85% раствора хлористого натрия.
Прибавьте 2,5 мл биуретового реактива.
Перемешайте, термостатируйте 30 мин при 37оС, измерьте оптическую плотность так же, как и при определении альбуминов.
Калибровочный
график для определения белка биуретовым
методом.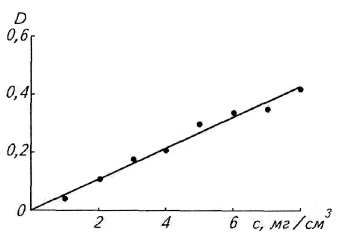 К
К
Для определения концентрации альбуминов полученные по стандартному графику значения следует умножить на 2, т.к. в ходе подготовки реакции сыворотка крови была разбавлена в два раза больше, чем при определении общего белка.
Сравните полученные значения с нормальными величинами. О чем свидетельствует снижение (повышение) уровня белка в сыворотке крови у животных? К каким последствия может привести недостаточность альбумина в крови?
Опыт 3. Количественное определение активности аланинаминотрансферазы (АлАТ) в сыворотке крови.
В две пробирки внесите реактивы согласно следующей таблице:
|
|
Контрольная проба |
Опытная проба |
|
Реагент 1 (АлАТ, субстрат), мл |
0,25 |
0,25 |
|
Дистиллированная вода, мл |
0,05 |
– |
|
Сыворотка, мл |
– |
0,05 |
|
Перемешать и инкубировать 30 мин | ||
|
Реагент 2 (динитрофенилгидразин), мл |
0,25 |
0,25 |
|
Перемешать и оставить при комнатной температуре на 20 мин | ||
|
NaOH (С = 0,4 моль/л), мл |
2,5 |
2,5 |
Перемешайте и через 10 минут измерьте оптическую плотность пробы против контрольной пробы при длине волны 540 нм, кювета с толщиной слоя 5 мм.
Активность АлАТ в опытной пробе определите по калибровочному графику в нмоль/сл.
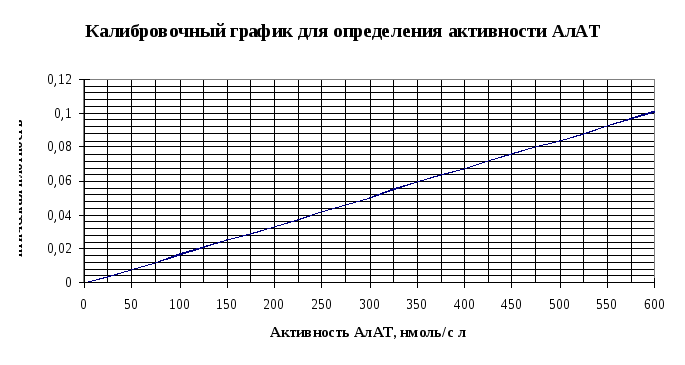
Сравните полученный результат с физиологическими величинами и сделайте вывод. Опишите механизм работы кофермента трансаминаз.
Опыт 2. Белки как противоядие от ионов тяжелых металлов.
Взаимодействие ионов металлов с белками лежит в основе использования молока как противоядия при отравлении тяжелыми металлами.
Приборы. 1. Штатив с пробирками.
2. Набор пипеток.
3. Водяная баня.
Реактивы. 1. Амилаза, раствор.
2. Крахмал, 1%-ный раствор.
3. Ацетат свинца, 1%-ный раствор.
4. Молоко.
5. Дистиллированная вода.
6. Йод, 1%-ный раствор.
В опытную пробирку налейте по 1 мл раствора амилазы, 1%-ного раствора крахмала, 1%-ного раствора ацетата свинца (II) и молока.
В контрольную пробирку налейте по 1 мл растворов амилазы, крахмала, ацетата свинца (II) и воды.
Пробирки встряхните и выдержите 20 минут при температуре 30°С.
Добавьте в обе пробирки по 1 капле 1%-ного раствора йода.
Объясните полученные результаты.
