
- •5.Классификация углеводов
- •6. Физико-химические свойства углеводов
- •12.Изоэлектрическая точка и изоэлектрическое состояние аминокислот и белков
- •14. Общие и отличительные свойства неорганического катализатора и фермента
- •Что такое ферменты и неорганические катализаторы
- •Сравнение ферментов и неорганических катализаторов
- •16.Методы определения и способы выражения активности ферментов.
- •18.Механизм ферментного катализа
- •20.Активаторы и ингибиоры ферментов , их биологическая роль
- •22.Мультиферментные комплексы, проферменты изоферменты и их биохимическое значение.
- •24.Витамины – как предшественники коферментов
- •26.Биохимические функции жирорастворимых витаминов
- •30.Биохимические механизмы передачи гормонального сигнала
5.Классификация углеводов
По способности к гидролизу углеводы делятся на простые — моносахариды и сложные — полисахариды,дисахариды(олиго.,три.)
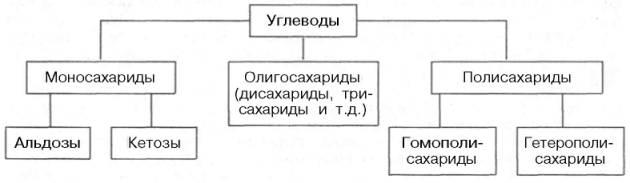
Моносахариды(простые сахара) – углеводы, которые не способны гидролизироваться до более простых соединений.
Олигосахариды(низкомолекулярные сахара) – углеводы, которые при гидролизе распадаются на 2-8 моносахаридов.
Полисахариды (сложные сахара)- продукты конденсации моносахаридов, они способны гдиролизоваться с образованием простых углеводов ( от десятков до сотен тысяч молекул моносахаридов)
СТРОЕНИЕ УГЛЕВОДОВ
Термин "углеводы", предложенный в XIX столетии, был основан на предположении, что все углеводы содержат 2 компонента - углерод и воду, и их элементарный состав можно выразить общей формулой Cm(H2O)n. Хотя из этого правила есть исключения и оно не абсолютно точно, тем не менее указанное определение позволяет наиболее просто характеризовать класс углеводов в целом. К тому же попытка, предпринятая Комиссией по химической номенклатуре, заменить термин "углеводы" на "глициды" не удалась. Новый термин не получил широкого признания. Термин "углеводы" укоренился и общепризнан.
Углеводы можно разделить на 3 основные группы в зависимости от количества составляющих их мономеров: моносахариды, олигосахариды и полисахариды.
6. Физико-химические свойства углеводов
Физические свойства
Моносахариды – твердые вещества, легко растворимые в воде, плохо – в спирте и совсем нерастворимые в эфире. Водные растворы имеют нейтральную реакцию на лакмус. Большинство моносахаридов обладают сладким вкусом, однако меньшим, чем свекловичный сахар.
Химические свойства
Моносахариды проявляют свойства спиртов и карбонильных соединений.
7.Принцепы классификации производных углеводов : гликопротеиды, гликолипиды, протеогликаны и др. Биологическая роль данных соединений..( ты взяла его)
8.Углеводы как составные элементы нуклеиновых кислот, коферментов, витаминов.
Нуклеиновые кислоты – это небелковый компонент нуклеопротеи-
нов. В настоящее время их рассматривают как надмолекулярные комплексы
и по наличию небелкового компонента выделяют дезоксирибонуклеопро-
теины (ДРНП) и рибонуклеопротеины (РНП).
Состав нуклеиновых кислот
Состав нуклеиновых кислот был изучен еще в конце XIX века с помо-
щью простых методов: гидролиза и качественных реакций на структурные
компоненты. Так было выяснено, что в составе нуклеиновых кислот есть
углеводы, азотсодержащие соединения и фосфорная кислота.
Углеводы представлены пентозами, рибозой и дезоксирибозой (рис.
5.2), которые обнаружены соответственно в РНК и ДНК. .
КОФЕРМEНТЫ (от лат. со- - приставка, означающая совместность, и ферменты) (коэнзимы), орг. прир. соед., необходимые для осуществления каталитич. действия ферментов. Эти в-ва, в отличие от белкового компонента фермента (апофермента), имеют сравнительно небольшую мол. массу и, как правило, термостабильны. Иногда под коферментами подразумевают любые низкомол. в-ва, участие к-рых необходимо для проявления каталитич. действия фермента, в т. ч. и ионы, напр. К+, Mg2+ и Мn2+ .
Витамины - (от лат. vita — жизнь), низкомолекулярные органические соединения различной химической природы, необходимые в незначительных количествах для нормального обмена веществ и жизнедеятельности живых организмов. Многие витамины — предшественники коферментов, в составе которых участвуют в различных ферментативных реакциях. 10.биологические функции и особенности строения аминокислот
Аминокисло́ты (аминокарбо́новые кисло́ты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминныегруппы.
Аминокислоты — бесцветные кристаллические соединения, в большинстве случаев хорошо растворимые в воде. В структуре их находятся две функциональные группировки атомов: аминная NH2 и карбоксильная СООН.
Особенности строения аминокислот заключаются в изомерии, которая может быть обусловлена также разветвлением углеродного скелета, а также строением своей углеродной цепи.
Биологические функции аминoкислoт
1. Стpуктуpные элeменты пeптидов и белков. В состав белков входят 20 протеиногенных аминокислот , которые кодиpyютcя генетичеcким кодом и постоянно oбнapyживaютcя в белкax. Некоторые из них пoдвеpгaютcя посттрансляционной модификации, т.е. мoгyт быть фocфopилиpовaны, aцилиpoваны или гидpoксилирoваны .
2. Структурные элeмeнты дpyгих природных соeдинeний. Аминoкиcлoты и их производные входят в cocтaв коферментов ,желчных кислот ,антибиотиков.
3. Пepeнoсчики сигналов. Некоторые из aминoкиcлoт являются нейромедиаторами или предшественниками нейромедиаторов, медиаторов или гормонов .
4. Метаболиты. Аминoкиcлоты — важнейшие, а некоторые из них жизненно важные компоненты питания .Некоторые aминoкиcлoты принимают участие в обмене веществ, нaпpимep, cлyжaт донорами азота . Непротеиногенные aминoкиcлoты oбpaзyютcя в качестве прoмeжyточныx продуктов при биоcинтeзе и деградации протеиногенных аминокислот или в цикле мочевины.
