
ГОС / 37
.doc37. К концу XIX века уже было известно, что в спектрах излучения и поглощения атомов имеются отдельные линии, соответствующие определённым частотам. Эти экспериментальные данные послужили толчком для создания различных моделей строения атома.
1. Модель Томсона.
В 1903 году Томсоном была предложена модель атома, согласно которой в размазанном положительном заряде внутри атома плавали отрицательно заряженные электроны (как изюм в пудинге). Согласно этой модели если электрон вышел из положения равновесия, то на него со стороны заряда будет действовать квазиупругая сила, которая возвращает электрон в первоначальное положение.

![]()
ox:
![]()
![]()
![]()
![]()

w0 – частота, с которой электрон будет излучать электромагнитные волны.
Данная модель могла объяснить спектр излучения атома водорода, но не могла дать детальное соответствие теории с экспериментом.
2. Модель атома Резерфорда (1911г.).
Резерфорд проводил опыты по рассеиванию a частиц веществом. Он предположил, что в атоме есть массивное ядро с положительным зарядом, а вокруг вращается электрон, масса которого много меньше массы положительно заряженного ядра. При этом атом нейтрален. При вращении электрона вокруг положительно заряженного ядра он также должен излучать электромагнитные волны (смотри электродинамику). Однако эта модель с точки зрения классической электродинамики обладает недостатком.
Электрон, вращающийся по орбите вокруг ядра с постоянной скоростью, обладает центростремительным ускорением и должен излучать электромагнитные волны. Однако бесконечно долго излучать он не может, электрон должен потерять свою энергию и упасть на ядро, и атом прекратит своё существование, чего на самом деле не наблюдается.
В 1913 году Бор попытался подправить эту модель и сформулировал постулаты, позволяющие объяснить устойчивость атома и наблюдаемые спектры излучения и поглощения света.
1. Из всех возможных орбит электрона в атоме допускаются лишь некоторые совместимые с правилом квантования, т.е. момент импульса электрона кратен постоянной Планка.
L=n![]() (n=1,2,3…)
(3.1)
(n=1,2,3…)
(3.1)
Существование дискретных орбит приводит к тому, что энергия электрона в атоме принимает дискретный ряд значений.
2. Правило частот Бора.
При переходе электрона с одной орбиту на другую или с одного энергетического уровня на другой излучается или поглощается квант света с энергией равной разности энергий этих уровней.
![]() wmn=Em-En
(3.2)
wmn=Em-En
(3.2)
Совокупность этих постулатов позволила объяснить дискретность энергетических спектров.

![]() -
нормальное или центростремительное
ускорение.
-
нормальное или центростремительное
ускорение.
Количественная теория Бора для водородоподобного атома.
![]()
ox:
![]() (3.3)
(3.3)
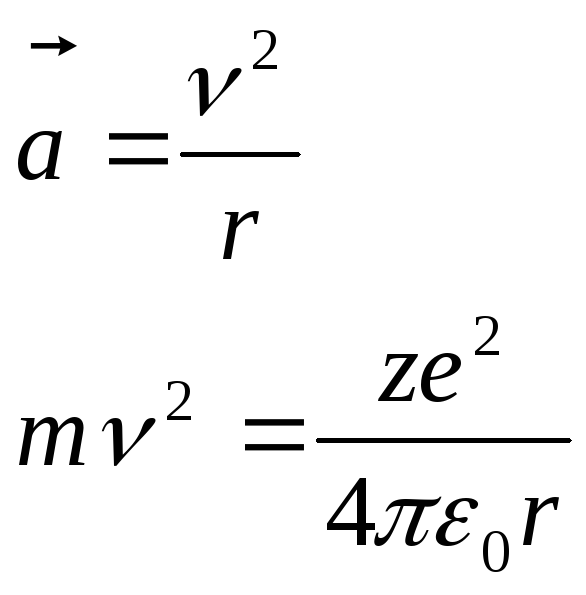 (3.3¢)
(3.3¢)
![]() (*)
(*)
![]()
![]() (**)
(**)
![]()
![]()
![]() (3.4)
(3.4)
![]()
![]() (3.5)
(3.5)
n=1,2,3,…
Радиус орбиты принимает дискретный ряд значений, т.е. квантуется, т.к. в 3.5 n – это натуральные числа, а всё остальное постоянные величины.
![]() (3.6)
(3.6)
n - принимает дискретный ряд значений или квантуется.
Посчитаем энергию электрона.
E=T+U
![]()
![]() (3.7)
(3.7)
n=1,2,3,…
Полная энергия электрона в атоме принимает дискретный ряд значений, т.е. квантуется.
Построим зависимость E(n), где n – номер орбиты вращения электрона. В дальнейшем n – это главное квантовое число.
![]()
z=1
![]() (3.8)
– постоянная Ридберга.
(3.8)
– постоянная Ридберга.
![]() (3.9)
(3.9)
![]() (3.9¢)
(3.9¢)
![]() (n=1)
(n=1)
![]() (n=2)
(n=2)
![]() (n=3)
(n=3)

E1:E2:E3…En=12:22:32…n2
Правило частот Бора.
![]() wmn=Em-En
wmn=Em-En
![]() (3.10)
(3.10)
z=1:
 (3.11)
(3.11)
3.11 – обобщённая формула Бальмера.
R=2.07*1016c-1
Если
n=1,
а m=2,3,…,
то
![]() ,
т.е. при переходе электрона со 2,3,4,…
уровня на первый излучается серия линий
с частотами m1,
которая называется серией линий Лаймана.
Эта серия лежит в ультрафиолетовой
области излучения (части спектра).
,
т.е. при переходе электрона со 2,3,4,…
уровня на первый излучается серия линий
с частотами m1,
которая называется серией линий Лаймана.
Эта серия лежит в ультрафиолетовой
области излучения (части спектра).
n=2, a m=3,4,5…
![]() (3.13)
(3.13)
При переходе электрона с 3,4,5,… уровней на второй излучается серия линий с частотами m2, которая называется серией линий Бальмера. Эта серия лежит в видимой части спектра. Это выражение впервые было получено Бальмером.
n=3, a m=4,5,6,…
![]() (3.14)
(3.14)
При переходе электрона с 4,5,6,… уровней на третий излучается серия линий с частотами m3, которая называется серией линий Пашена. Эта серия лежит в инфракрасной области излучения. Остальные серии (Пфунта, Бреккета и т.д.) можно получить аналогичным образом, все они лежат в инфракрасной области излучения.
Теория Бора смогла детально объяснить спектры излучения и поглощения атома водорода атома водорода. Однако при объяснении спектра излучения атома гелия возникли трудности и данная теория оказалась несостоятельной. С точки зрения квантовой механики теория Бора не является последовательной квантово-механической теорией, т.к. в квантовой механике нет понятия траектории и постулат о дискретности орбит не верен. Квантовая теория может объяснить спектры всех элементов, однако вклад теории Бора в развитие физики бесспорен и теория Бора является переходной ступенью от классической к квантовой физике.
Опыты Франка-Герца.
В 1913 году Франком и Герцем были проделаны следующие опыты. В трубке, в которой находились пары ртути при давлении 1мм. ртутного столба впаивались сначала 3, а затем 4 электрода: катод, анод, сетка (2 сетки). Катод подогревался и служил источником термоэлектронов. Между сеткой и анодом прикладывалось тормозящее напряжение порядка 0.7 вольта, чтобы отсечь медленные электроны. Напряжение между сеткой и катодом регулировалось потенциометром R, при этом гальванометром измерялся анодный ток, и строилась вольтамперная характеристика, которая имела пика образный характер.


При увеличении напряжения между катодом и сеткой ток возрастал вплоть до напряжения 4.9 Э.вольта, при этом соударения между электронами и атомами ртути носят упругий характер. Энергия электронов при этом практически не менялась (из-за малости электрона), часть электронов попадала на сетку, часть долетала до анода. При увеличении напряжения большая часть электронов достигала анода, ток возрастал. При напряжении 4.9 Э.вольта электроны отдают свою энергию атомам ртути, возбуждая их, теряют свою энергию, не долетают до анода, и ток в цепи резко падает. При увеличении напряжения между катодом и сеткой картина повторялась и при напряжении 9.8 Э.вольта происходит двукратное возбуждение атомов ртути. При дальнейшем увеличении напряжения ситуация повторяется. Отсюда видно, что атомы ртути могут возбуждаться только при определённой энергии, что свидетельствует о дискретности энергетических состояний атомов ртути.
