
Химия
.pdf
растворимое основание, это щелочь. Гидроксиды галлия (III) и индия (III) - амфотерны, поэтому все соли этих металлов (III) подвержены гидролизу.
Поскольку значения стандартных электродных потенциалов Ga, In, Tl отрицательные, они растворяются в кислотах с выделением водорода.
Задачи
213. Напишите электронные формулы Al, Ga, In, Tl в нормальном и возбужденном состояниях, распределите валентные электроны по энергетическим ячейкам и определите возможные степени окисления этих металлов в их соединениях. Почему для Tl характерной степенью окисления является +1
214.Как получаются гидроксиды Al(OH)3 ,Ga(OH)3 , In(OH)3 Какие они имеют свойства
Какие они имеют свойства Как диссоциируют? Напишите уравнения взаимодействия этих гидроксидов с HCl и NaOH.
Как диссоциируют? Напишите уравнения взаимодействия этих гидроксидов с HCl и NaOH.
215.С какими из перечисленных ниже соединений взаимодействует Al, Tl :
H2O, HCl, H2SO4 (разб.), H2SO4 (конц.), HNO3 (разб.), HNO3 (конц.)? Напишите уравнения реакций.
216.Как взаимодействует Al с водным раствором щелочи Какие стадии этого процесса можно выделить Запишите соответствующие реакции.
Какие стадии этого процесса можно выделить Запишите соответствующие реакции.
217.Составьте уравнения реакций, которые нужно провести для осуществления следующих превращений:
|
|
Al AlCl3 |
Al(OH)3 |
Na[Al(OH)4] |
|
|
||||
218. |
Что |
такое алюмотермия |
Можно |
ли алюмотермическим способом |
||||||
получить из оксида железа (III) железо и из оксида кальция кальций при |
||||||||||
1500 К |
Подтвердите |
ответ |
расчетом |
энергии |
Гиббса |
соответствующих |
||||
реакций, если |
|
|
|
|
|
|
|
|
|
|
|
|
Fe2O3(т) CaO (т) Al2O3 (т) Fe(т) Al(т) Ca(т) |
||||||||
H298 кДж/ моль |
-823 |
|
-636 |
-1677 |
0 |
0 |
0 |
|||
S 298 Дж/ (моль*град) |
87,9 |
|
39,8 |
|
51 |
27,3 28,3 |
41,8 |
|||
219. Осуществите превращения и определите неизвестные вещества: |
||||||||||
|
t |
электролиз |
|
|
|
|
|
|
|
|
Al(OH)3 |
Х |
Y |
Al(NO3)3 |
Na[Al(OH)4] |
|
|
||||
220.Почему Al относится к металлам, а бор – к неметаллам, хотя эти элементы являются полными электронными аналогами?
221.Осуществите превращения:
B H3BO3 Na2B4O7 H3BO3
222. Составьте, где возможно, молекулярные и электронные уравнения реакций:
а) борного ангридида с водой ; б) бора с концентрированными азотной и серной кислотами ; в) борной кислоты с магнием ;
г) буры с сильной кислотой.
XX . Элементы IVа подгруппы
На внешнем уровне элементов этой подгруппы по 4 электрона. Общая формула валентных электронов nS2p2 . Характерные степени окисления +2 и +4. Соединения углерода и кремния со степенью окисления +2 немногочисленны и сравнительно малостойки.
При переходе от углерода к свинцу закономерно ослабевают неметаллические и нарастают металлические свойства элементов. Углерод и кремний являются неметаллами, олово и свинец - металлы.
Углерод в свободном состоянии наиболее известен в виде двух модификаций - алмаза и графита.
Углерод при взаимодействии с водородом образует метан:
С+2H2 CH4
Метан - простейший представитель водородных соединений углерода - углеводородов, представляющих собой самый многочисленный класс химических веществ и являющихся объектом изучения органической химии.
Углерод и кремний - типичные восстановители. При нагревании с избытком воздуха графит и кремний образуют диоксиды (СO2 и SiO2), при недостатке кислорода можно получить монооксиды (CO и SiO), которые образуются также при нагревании простых веществ с их диоксидами:
C + CO2 = 2CO, |
Si + SiO2 = 2SiO |
Уже при обычной температуре С |
и Si реагирует с фтором, при нагревании |
- с хлором, образуя соответственно тетрафториды и тетрахлориды; при более сильном нагревании - с серой (продукты - CS2 и SiS2) и даже между собой, образуя карборунд – вещество, по твердости близкое к алмазу:
Si + C = SiC
Углерод окисляется концентрированными H2SO4 и HNO3:
C + 4HNO3 = CO2 + 2H2O + 4NO2 
Кремний растворяется в смеси концентрированных азотной и плавиковой кислот:
3Si + 4HNO3 + 12HF = 3SiF4 + 4NO + 8H2O
Кроме того, Si растворяется в водных растворах щелочей:
Si + 2NаOН + H2О=Na2SiO 3+ 2H2 
Графит часто используют для восстановления малоактивных металлов из их оксидов:
CuO + C = Cu + CO
При нагревании же с оксидами активных металлов C u Si диспропорционируют, образуя карбиды:
CaO + 3C = CaC2 + CO
2Al2O3 + 9C = Al4C3 + 6CO
или силициды:
2MgO + 3Si = Mg2Si + 2SiO2.
Активные металлы - более сильные восстановители, чем С и Si, поэтому последние при непосредственном взаимодействии с ними выступают в качестве окислителей:
Ca + 2С = CaC2 , 2Mg + Si = Mg2Si
Оксиды углерода (II) и кремния (II) не реагируют при обычных условиях ни с кислотами, ни со щелочами. SiO малодоступен и используется редко, в отличие от СО - угарного газа.
СО принято считать несолеобразующим, однако он реагирует с расплавом щелочи при высоком давлении с образованием соли муравьиной кислоты HCOОH, поэтому формально его можно считать ее ангидридом, что подтверждается выделением СО при обезвоживании HCOOH:
|
H2SO4(конц.) |
HCOOH |
CO + H2O |
На воздухе СО горит, образуя СО2 . Он восстанавливает металлы из их оксидов:
FeO + CO = Fe + CO2 
Вприсутствии катализатора СО окисляется хлором, образуя ядовитый газ
-фосген:
CO + Cl2 = COCl2
Со многими металлами СО образует летучие карбонилы:
Fe + 5CO = Fe(CO)5, Ni + 4CO = Ni(CO)4 .
Диоксид углерода СО2 постоянно образуется в природе при окислении органических веществ. В лабораториях его обычно получают в аппарате Киппа:
CaCO3 + 2HCl = CaCl2 + H2O + CO2 ,
в промышленности - обжигом известняка: CaCO3 = СаО + СО2
Кислый по своей природе, СО2 реагирует с сильными основаниями, например,
Ca (OH)2 +CO2 = CaCO3 +H2O
Взаимодействием диоксида углерода с аммиаком под давлением получается важное в практическом отношении соединение - карбамид или мочевина:
CO2 +2NH3 = CO(NH2)2 + H2O
Раствор СО2 в воде обладает слабокислотной реакцией, обусловленной присутствием в растворе небольших количеств угольной кислоты:
СО2 +Н2О = Н2СО3 Угольная кислота может существовать только в водном растворе. По
способности к диссоциации она относится к очень слабым; в растворе имеют место равновесия:
Н2СО3 Н++НСО-3 2Н+ +СО32-

Будучи двухосновной, угольная кислота образует два ряда солей - средние (карбонаты) и кислые (гидрокарбонаты), которые могут быть получены действием СО2 на щелочи (см. выше) или обменными реакциями:
Ba(NO3)2 + Na2CO3 = BaCO3 + 2NaNO3
NaHCO3 + NaOH = Na2CO3 + H2O
Со слабыми основаниями угольная кислота обычно дает основные соли, например, (CuOH)2CO3 - карбонат гидроксомеди (природный минерал - малахит).
При нагревании все карбонаты (кроме солей щелочных металлов) разлагаются:
t
MgCO3 = MgO+CO2 ,
а гидрокарбонаты щелочных металлов переходят в карбонаты: t
2NaHCO3 = Na2CO3+CO2 + H2O
Растворы карбонатов имеют вследствие гидролиза кислот сильнощелочную реакцию:
CO32- +HOH HCO3- +OH-
Карбонаты менее растворимы, чем гидрокарбонаты.
Из солей угольной кислоты в природе широко распространен CaCO3 (известняк, мел, мрамор), а также MgCO3 . Одним из главных продуктов
основной химической промышленности является сода (Na2CO3 |
10H2O- |
кальцинированная сода, NaHCO3 - питьевая сода), в значительных объемах карбонаты являются ценными рудами и используются для получения металлов (FeCO3 - шпатовый железняк, ZnCO3 – галмей).
Из соединений углерода с серой и азотом большое практическое значение имеют сероуглерод CS2 и синильная кислота HCN.
Кислотному оксиду SiO2 соотвествуют малорастворимые в воде орто – и метакремниевые кислоты (H4SiO4 и H2SiO3). Соли кремниевых кислот – силикаты – в большинстве своем также нерастворимы в воде; растворимы лишь Na2SiO3 и K2SiO3. Растворы вследствие гидролиза имеют щелочную реакцию.
Силикаты натрия и кальция составляют основу обычного стекла, состав котрого выражается приблизительной формулой Na2O CaO 6SiO2.
Силикаты чрезвычайно распространены в природе.
Врамках IVа группы германий, олово и свинец выделяют в отдельную подгруппу, поскольку эти элементы, особенно олово и свинец, являются металлами. На воздухе эти металлы покрыты тонкой оксидной пленкой, предохраняющей их от дальнейшего разрушения.
Вода сама по себе не действует на эти металлы, но в присутствии воздуха свинец постепенно разрушается с образованием гидроксида.
Pb +O2 +2H2O = Pb(ОН)2
Вжесткой воде процесс тормозится образованием нерастворимых солей - сульфата и основного карбоната.

Разбавленные соляная и серная кислоты почти не действуют на эти металлы. В концентрированной серной, особенно при нагревании, свинец и олово растворяются с образованием соответственно Pb(HSO4)2 и Sn(SO4)2. В концентрированной соляной кислоте олово растворяется, вытесняя водород. С азотной кислотой интенсивность взаимодействия свинца растет с понижением концентрации кислоты; олово же интенсивнее реагирует с концентрированной
HNO3:
4Sn + 10HNO3(р.) = 4Sn(NO3)2 + NH4NO3 + 3H2O
Sn + 4HNO3(к.) = H2SnO3 + 4NO2 |
+ H2O |
(оловянная кислота) |
|
Оба этих металла растворяются в |
щелочах, причем олово - в |
концентрированных с образованием станнитов - солей оловянистой кислоты
(H2SnO2):
Sn + 2NaOH = Na2SnO2 + H2 ,
которые в растворах существуют в гидратированной форме (например, Na2[Sn(OH)4] - тетрагидроксостаннит натрия); свинец же лучше реагирует в разбавленных горячих растворах с образованием гидроксоплюмбитов:
Pb + 4KOH +2H2O = K4[Pb(OH)6] + H2 
Олово образует два ряда соединений, соответствующих устойчивым степеням окисления +2 и +4, у свинца значительно более устойчивы и многочисленны соединения со степенью окисления +2.
Гидроксиды Sn(OH)2 и Pb(OH)2 получаются при действии щелочей на растворимые соли этих металлов
Me2+ + 2OH- = Me(OH)2 .
Они амфотерны и реагируют как с кислотами, так и сильными основаниями:
Sn(OH)2 |
+2NaOH |
= Na2[Sn(OH)4] |
Pb(OH)2 |
+ 4KOH |
= K4 [Pb(OH)6] |
Гидроксиды олова (IV) называются оловянными кислотами и извесны в двух модификациях: -оловянной и -оловянной кислот.
Состав этих кислот довольно неопределенный; формула H2SnO3 является лишь простейшей из возможных, а правильнее состав выражает формула
mSnO2* nH2O.
-Оловянная кислота лекго растворяется в щелочах, образуя гидроксостаннаты:
H2SnO3 + 2NaOH + H2O = Na2[Sn(OH)6],
выделяющиеся из растворов в виде кристаллогидратов, например,
Na2SnO3*3H2O
Кислоты также растворяют -оловянную кислоту:
Н2SnO3 +4HCl = SnCl4 + 3H2O
В избытке соляной кислоты образуется комплексная гексахлороловянная кислота:
SnCl4 +2НCl = Н2[SnCl6]

В отличие от -формы -оловянная кислота не растворяется ни в растворах кислот, ни в растворах щелочей, реагируя лишь с расплавами щелочей.
-Кислота при хранении в растворе, в котором ее получили, постепенно превращается в -кислоту.
Среди содинений свинца (IV) большое значение имеет PbO2. Это амфотерный оксид с преобладанием кислотных свойств. При сплавлении с основными оксидами образуются плюмбаты - соли несуществующей в свободном состоянии свинцовой кислоты (H2PbO3):
CaO + PbO2 = CaPbO3
Плюмбаты большинства металлов (кроме натрия и калия) нерастворимы в
воде.
Диоксид свинца, как и другие его соединения в высшей степени окисления (+4), - очень сильный окислитель. Он, например, окисляет соляную кислоту до свободного хлора:
PbO2 + 4HCl = PbCl2 + Cl2 + 2H2O
Диоксид свинца используют в свинцовом аккумуляторе в качестве катода
(заряжен положительно): |
|
|
|
|
PbO2 +SO42- + 4H+ +2e = PbSO4 + 2H2O |
восстановление |
|
||
Анодом (заряжен отрицательно) служит металлический свинец: |
|
|||
Pb + SO42- -2e = PbSO4 |
окисление |
|
|
|
В качестве электролита используется 35-40 % раствор H2SO4 . |
|
|||
Суммарное |
уравнение |
окислительно-восстановительной |
реакции, |
|
протекающей при работе (разрядке) свинцового аккумулятора:
Pb + PbO2 + 4H+ + 2SO42- = 2PbSO4 +2H2O
Для зарядки аккумулятора его подключают к внешнему источнику тока (плюсом к плюсу и минусом к минусу). При этом на электродах протекают процессы, противоположные тем, которые идут при его разрядке, и вновь получаются вещества, необходимые для его работы.
Из средних солей данных металлов наиболее известны хлориды и сульфиды олова (II и IV) и свинца (II), а также хлорид, иодид, сульфат, гидросульфат, ацетат свинца (II). Последние две соли, в отличие от большинства других солей свинца, хорошо растворимы в воде. Растворы солей Sn и Pb имеют кислую реакцию вследствие гидролиза.
Задачи
223. Запишите электронные формулы углерода, олова и свинца в нормальном и возбужденном состояниях. Какие степени окисления наиболее характерны для этих элементов
224. Приведите уравнения реакций, характеризующих окислительные и восстановительные свойства углерода
225.В чем различие химических свойств оксидов углерода (II) и (IV) Чем это вызвано Приведите соответствующие уравнения реакций.
Чем это вызвано Приведите соответствующие уравнения реакций.
226.Какие соединения называются карбидами и силицидами Напишите уравнения реакций их получения. Как взаимодействует с водой карбид
Напишите уравнения реакций их получения. Как взаимодействует с водой карбид
алюминия; силицид магния с соляной кислотой 227. Осуществите превращения и определите неизвестные вещества:
227. Осуществите превращения и определите неизвестные вещества:
|
Ca(OH)2 CO2 Ca(OH)2 |
|
|||
C |
CO2 |
Х |
Y |
Z |
CO2 |
228.Смесь кремния и угля массой 5,0 г обработали избытком концентрированной щелочи при нагревании. В результате реакции выделилось 2,8 л газа (н.у.). Вычислите массовую долю углерода в смеси.
229.Из чего состоит обычное стекло Приведите реакции, лежащие в основе его получения.
Приведите реакции, лежащие в основе его получения.
230.Осуществите превращения и определите неизвестные вещества
Mg |
O2 K2CO3 |
SiO2 Si |
Х SiH4 Y Z |
231.Как ведут себя углерод и кремний с кислотами, щелочами Приведите соответствующие уравнения реакций.
Приведите соответствующие уравнения реакций.
232.Как можно получить карбонаты, гидрокарбонаты Как они ведут себя
Как они ведут себя
при нагревании Запишите соотвествующие уравнения реакций.
233.Кремниевая кислота слабее угольной. Запишите уравнения гидролиза карбоната и силиката натрия и возможные значения pH среды при равных исходных концентрациях солей и одинаковой температуре растворов.
234.С какими из следующих соединений, находящихся в водных растворах
HCl, H2SO4 (разб.), HNO3 (разб.), H2SO4 (конц.), HNO3 (конц.),
взаимодействует олово? Напишите уравнения реакций.
235.Какие свойства имеют оксиды и гидроксиды олова и свинца Напишите уравнения реакций взаимодействия их со щелочами и кислотами.
Напишите уравнения реакций взаимодействия их со щелочами и кислотами.
236.Напишите уравнения реакций взаимодействия свинца с HNO3 (разб.),
HNO3 (конц.), H2SO4 (разб.), H2SO4 (конц.), CH3COOH, HCl.
237.Чем можно объяснить окислительные свойства оксида свинца (IV) Закончите уравнения окислительно-восстановительных реакций и расставьте коэффициенты:
Закончите уравнения окислительно-восстановительных реакций и расставьте коэффициенты:
PbO2 + Mn(NO3)2 + HNO3 = HMnO4 + ………
PbO2 + HCl = Cl2 + ………
238.Составьте уравнения реакций свинца и олова с едким натрием; свинца с водой при доступе кислорода.
239.Составьте уравнения реакций, протекающих при зарядке и разрядке свинцового аккумулятора.
240.Как получить соду, имея металлический натрий, соляную кислоту,
мрамор и воду Составьте уравнения реакций.

XXI. Элементы Vа подгруппы
Азот, фосфор, мышьяк, сурьма и висмут имеют на внешнем энергетическом уровне по 5 электронов; соответственно их высшая степень окисления +5, низшая -3.
В целом они характеризуются как неметаллы, уступающие по этому признаку элементам VIa и VIIa подгрупп. Неметаллические свойства закономерно убывают сверху вниз по подгруппе, и у висмута уже преобладают металлические свойства.
Широкий диапазон изменения степени окисления обусловливает большое
разнообразие соединений этих элементов; особенно азота. Так, известны оксиды азота N2+1O, N+2O, N2+3O3, N+4O2, N2+5O5 . Все они могут быть получены
из азотной кислоты и ее солей.
Минимальную степень окисления – 3 азот имеет в аммиаке и его производных.
N2O устойчив при комнатной температуре. Химически инертен и ни с водой, ни с кислотами, ни со щелочью не реагирует. В этом отношении с ним схож оксид NO (N2O и NO относятся к безраличным или несолеобразующим оксидам).
Для оксида азота (II) характерна окислительно-восстановительная двойственность. Например, он легко окисляется кислородом воздуха до диоксида:
2NO + O2 = 2NO2,
с другой стороны, энергично окисляет водород в смеси их равных объемов при нагревании:
2NO + 2H2 = N2 + 2H2O
Диоксид азота NO2 – бурый ядовитый газ с характерным запахом.
При t -11 С существует в виде димера N2O4, при t = 140 С – в виде NO2, частично распадающегося при более высокой температуре на NO и O2 ; в интервале температур -11 140 С имеет место равновесие
140 С имеет место равновесие
N2O4 2NO2 – Q
Оксиды азота II и IV являются промежуточными продуктами промышленного способа получения азотной кислоты HNO3:
kat
4NH3 + 5O2 = 4NO + 6H2O
(горение аммиака при обычных условиях приводит к образованию молекуляр-
ного азота и воды). |
. |
|
2NO + O2 = 2NO2 |
|
4NO2 + O2 + 2H2O = 4HNO3 |
Если растворять диоксид азота в щелочах, то образуется смесь солей
азотной и азотистой кислот (нитритов и нитратов), например:
2N+4O2 + 2NaOH = NaN+5O3 + NaN+3O2 + H2O
Ангидридом азотистой кислоты HN+3O2 является неустойчивый оксид азота +3: N2O3.
Ангидрид азотной кислоты – N2+5O5 – белый кристаллический, уже при комнатной температуре постепенно разлагающийся на NO2 и O2.
Оксид азота +5 – очень сильный окислитель, многие органические вещества при соприкосновении с ним воспламеняются.
Азотистая кислота HNO2 принадлежит к числу слабых и известна только в очень разбавленных растворах. Степень окисления +3 является промежуточной для азота, поэтому HNO2 проявляет окислительно  восстановительную двойственность: под действием восстановителей она восстанавливается обычно до NO, а в реакциях с окислителями – окисляется до
восстановительную двойственность: под действием восстановителей она восстанавливается обычно до NO, а в реакциях с окислителями – окисляется до
HNO3.
Азотная кислота также не отличается прочностью: уже под влиянием света она постепенно разлагается:
4HNO3 = 4NO2 + O2 + 2H2O
Принадлежит к числу наиболее сильных.
HNO3 за счет азота в максимальной степени окисления обладает ярко выраженной окислительной способностью.
При этом чем более она разбавлена и чем активнее восстановитель, тем
глужбе она восстанавливается: |
|
||
Cu + HNO3(к.) |
Cu(NO3)2 |
+ N+4O2 |
+ H2O |
Cu + HNO3(р.) |
Cu(NO3)2 |
+ N+2O |
+ H2O |
Zn + HNO3(очень разб.) |
Zn(NO3)2 + N-3H4 NO3 + H2O |
||
S + HNO3(к.) |
H2SO4 + N+4O2 + H2O |
||
Водород при окислении азотной кислотой, как правило, не выделяется. Смесь, состоящая из 1 объема азотной и 3-4 объемов соляной кислот,
называется «царской водкой». Она растворяет некоторые металлы, не взаимодействующие с азотной кислотой (Au, Pt, Pd, Os, Ru):
Au + HNO3 + 4HCl = H [AuCl4] + NO + 2H2O
Соли азотной кислоты – нитраты – термически нестабильны, разлагаются с выделением кислорода. При этом нитраты щелочных и щелочноземельных металлов переходят в нитриты:
t
2NaNO3 = 2NaNO2 + O2 
Нитраты металлов, расположенных в ряду напряжений между Mg и Cu включительно, дают оксид металла, азота и кислород:
t
2Pb(NO3)2 = 2PbO + 4NO2 + O2;
нитраты наименее активных металлов разлагаются до свободного металла:
t
2AgNO3 = 2Ag + 2NO2 + O2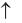
Все нитраты хорошо растворяются в воде.
Наиболее важное значение имеют нитраты натрия, калия, аммония и кальция, которые на практике называются селитрами.

С водородом азот образует несколько соединений, из которых наибольшее значение имеет аммиак NH3 – газ с характерным резким запахом.
В лаборатории он легко получается по реакции:
2NH4Cl + Ca(OH)2 = CaCl2 + 2H2O +2NH3 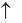
Аммиак очень хорошо растворим в воде, раствор имеет щелочную реакцию
NH3 + H2O NH4+ + OH-
и обычно выражается формулой NH4OH.
За счет неподеленной пары азота аммиак обладает слабыми основными свойствами и обратимо реагирует с кислотами.
NH3 + HCl NH4Cl
Фосфор в виде простого вещества существует в трех формах (аллотропных модификациях) - белый, красный, черный. Белый фосфор химически очень активен, легко взаимодействует с кислородом, галогенами, многими металлами. С кислородом фосфор образует оксиды P2+5O5, P2+3O3 . Им соответствуют орто– и метафосфорная кислоты (H3P+5O4 и HP+5O3) и фосфористая кислота HР+3O2. Наиболее важной является ортофосфорная. По способности к диссоциации она относится к кислотам средней силы.
Будучи трехосновной, образует три ряда солей: средние - фосфаты и кислые – гидро – и дигидрофосфаты. Растворы средних солей вследствие гидролиза имеют сильнощелочную реакцию.
Соли фосфорной кислоты широко используются в качестве минеральных удобрений.
Из природных соединений фосфора самое важное – ортофосфат кальция Ca3(PO4)2, составляющий основу минералов – фосфорита и апатита, являющихся сырьем для получения фосфора и его соединений.
Для получения фосфора смесь фосфорита или апатита с песком и углем прокаливают без доступа кислорода:
Ca3(PO4)2 + 3SiO2 + 5C = 3CaSiO3 + 2P + 5CO
У сурьмы, и особенно у висмута, металлические свойства уже преобладают над неметаллическими.
Оксид сурьмы (III) – типичный амфотерный оксид с некоторым преобладанием основных свойств, растворяется в кислотах и щелочах.
Гидроксид сурьмы, или сурьмянистая кислота, получается при действии щелочей на соли сурьмы в виде белого осадка. Осадок растворяется как в избытке щелочи, так и в кислотах.
Соли сурьмы (III), как соли слабого основания, в водном растворе гидролизуются с образованием основных солей:
SbCl3 + 2H2O Sb(OH)2Cl + 2HCl,
неустойчивых и разлагающихся с отщеплением молекул воды:
Sb(OH)2Cl = SbOCl + H2O
