
ХИМИЯ:Metodichka_organika
.pdfДонецкий национальный медицинский университет им. М.Горького.
Кафедра медицинской химии.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ к практическим занятиям по биоорганической химии
(для студентов первого курса медицинского факультета).
Донецк - 2011
Методические указания подготовили:
-зав. кафедрой доцент Рождественский Е.Ю. -доценты: Сидун М.С., Селезнева Е. В.
-ст. преподаватель Павленко В.И.
-ассистенты кафедры: Бусурина З.А., Сидоренко Л.М., Игнатьева В.В., Бойцова В.Е.
- 2 -
Вступление.
Целью развития отечественного образования в настоящее время является его конкурентноспособность по отношению к европейской системе образования. В 1999 года в европейской школе высшего образования был принят Болонский процесс. Основным принципом, которого является создания единого общеобразовательного пространства. Поскольку Украина - участник этого процесса, это влечет за собою изменение образовательных программ в высших учебных заведениях, а так же дает возможность нашим студентам получать высшее образование на уровне европейских стандартов.
Методические указания, которые предлагаются Вашему вниманию, должны помочь в освоении курса биоорганической химии и формированию умений, необходимых в учебной и будущей профессиональной деятельности. В связи с этим методические указания имеют определенную структуру. Каждый раздел начинается с обоснования актуальности и значения темы в медицине и биологии. Затем формулируются цели изучения конкретного раздела, отображающие умения, которые необходимо приобрести, и обеспечивают управление внеаудиторной подготовкой к практическим занятиям. Теоретические вопросы к темам помогут овладеть содержанием, без знания которого невозможно выполнения целевых видов деятельности. В списках литературы указаны источники для изучения конкретных тем. Освоению материала оказывают содействие структурно-логические схемы содержания (графы).
Методические указания содержат ситуационные задачи, сформулированные соответственно целям освоения учебного материала. Задания предлагается выполнить самостоятельно. Решения этих заданий способствует проверке степени готовности к занятиям. Краткие методические указания, которые завершают каждую тему, дают возможность определить последовательность, этапы, их продолжительность и обеспечение занятий. Эти методические рекомендации помогут осуществить качественную подготовку студентов соответственно требованиям кафедры.
Изучение разделов предмета и коррекция знаний помогут будущим медикам освоить биоорганическую химию как теоретическую базу для изучения таких фундаментальных дисциплин как биохимия, фармацевтическая химия. Мы надеемся, что самостоятельная работа студентов и контроль ее обеспечит приобретения знаний на качественно более высоком уровне, помогут использовать полученные знания при решении конкретных задач, которые будут встречаться в их врачебной практике. Участие в Болонской системе предоставляет возможность достойно проявить себя не только в профессиональной деятельности, но и на рынке труда. В конце хотелось отметить только знания химических, физических биологических законов поможет будущим врачам оценить значение важнейшей проблемы, стоящей сейчас перед человечеством – сохранение здоровья людей.
- 3 -
«СТРОЕНИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЬДЕГИДОВ И КЕТОНОВ»
АКТУАЛЬНОСТЬ ТЕМЫ:
Альдегиды и кетоны являются одним из важнейших классов органических соединений. Карбонильная группа входит в состав биологически важных соединений: ретиналь, витамин В6, глюкоза, фруктоза и др. Многие вещества, которые содержат карбонильную группу, используются в медицине в качестве лекарственных препаратов.
Например, хлоральгидрат – лечебное средство седативного действия. Формальдегид используется в анатомической и гистологической практике, а так же в производстве лекарственного вещества уротропина. Вещество ацетон, имеющее в составе карбонильную группу, образуется в процессе обмена и выделяется с мочой больных сахарным диабетом. Пробы мочи на кетоновые (ацетоновые) тела используются в клинических лабораториях для диагностики сахарного диабета.
Превращение соединений, которые в своём составе имеют карбонильную группу, их участие в процессах обмена обусловлено химическим составом и свойствами этих соединений.
Знание строения и свойств соединений, которые содержат карбонильную группу, умение найти их в растворах при помощи реакций, необходимы для дальнейшего обучения студента-медика, а также для профессиональной деятельности врача.
ЦЕЛИ ОБУЧЕНИЯ:
ОБЩАЯ ЦЕЛЬ:
Уметь интерпретировать строение и химические свойства карбонильных соединений для объяснения их реакций в организме человека.
Достижение этой цели обеспечивается выполнением конкретних целей.
КОНКРЕТНЫЕ ЦЕЛИ:
УМЕТЬ:
1.Идентифицировать карбонильные соединения.
2.Прогнозировать и идентифицировать свойства альдегидов и кетонов на основе электронного строения их молекул.
3.Объяснить общие и отличительные особенности карбонильных соединений на основе состава и структуры функциональных групп.
4.Интерпретировать медико-биологическое значение карбонильных соединений.
5.Идентифицировать биологически важные производные карбонильных соединений.
- 4 -
СОДЕРЖАНИЕ ОБУЧЕНИЯ:
Содержание обучения должно обеспечивать достижение целей обучения. ТЕОРЕТИЧЕСКИЕ ВОПРОСЫ:
1.Классификация и номенклатура карбонильных соединений. Электронное представление о строении карбонильной группы.
2.Реакции нуклеофильного присоединения альдегидов и кетонов: присоединение синильной кислоты, спиртов. Реакции присоединенияотщепления: взаимодействие с аммиаком и аминами. Реакции конденсации.
Механизм реакций.
3.Реакции восстановления и окисления альдегидов и кетонов. Реакции замещения в радикале (галогенирование).
4.Различная реакционная способность альдегидов и кетонов. 5.Медико-биологическое значение альдегидов и кетонов и их производных.
ИСТОЧНИКИ ИНФОРМАЦИИ: Обязательные:
1.Тюкавкина Н.А., Бауков Ю.М. «Биоорганическая химия». Москва.
Медицина, 1991г. с.181-194, с. 211, с.218-219, с. 226.
2.«Руководство к лабораторным занятиям по биоорганической химии» под. ред.
Н.А. Тюкавкиной. Москва. Медицина, 1995 г. с. 92-95, 103-106.
«Задачи для самостоятельного решения».См. там же с. 95, 11, с.103 4.1, 4.2. 3.Граф логической структуры темы.
4.Конспект лекций.
Дополнительные:
1.Черных В.П. и др. «Органическая химия», Книга 2. Харьков «Основа», 1995 г., с. 318-340.
- 5 -
Классиф. по строению радикала
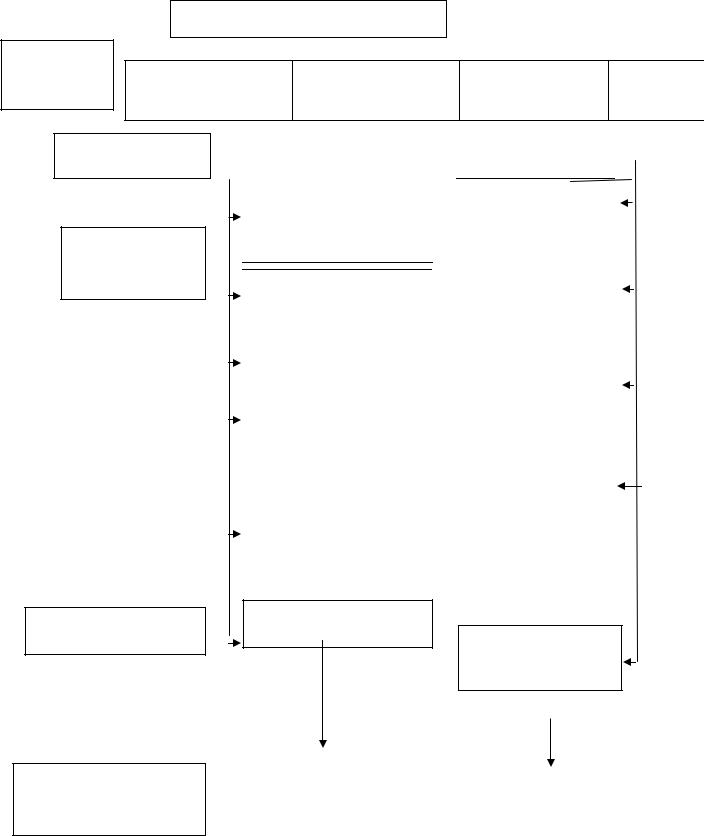
ГРАФ ЛОГИЧЕС КОЙ СТРУКТУРЫ ТЕМЫ:
«Строение и свойства альдегидов и кетонов».
Карбонильные соединения
Алифатические Ароматические Насыщенные Ненасы
Структура
Химические
свойства
Идентификация
Медико-биологическое значение
|
|
|
|
Электронное строение |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Альдегиды |
|
|
|
|
|
|
Кетоны |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Реакции |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
нуклеофильного |
|
|
|
||||||
|
|
|
Реакции |
|
|
|
|
||||||||
|
|
|
нуклеофильного |
|
|
присоединения |
|
|
|
||||||
|
|
|
замещения |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
Реакции |
|
|
|
|
Реакции |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
окисления |
|
|
восстановления |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Реакции |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
восстановления |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
Реакция |
|
|
|
|||||
|
|
|
|
|
|
|
|
альдольной |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
конденсации |
|
|
|
||||||
|
|
|
Реакции |
|
|
|
|
||||||||
|
|
|
альдольной |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
конденсации |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Реакция |
|
|
|
|
|
|
|
Реакции |
|
|
|
|
замещения |
в |
|
|
||||
|
|
|
замещения |
в |
|
|
|
радикале |
|
|
|
||||
|
|
|
радикале |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Реакция серебряного зеркала Реакция с
нитропрусидом
натрия
Формальдегид, |
|
Ацетон |
уксусный |
|
|
|
|
|
альдегид |
|
|
- 6 -

ОРИЕНТИРОВАННАЯ ОСНОВА ДЕЯТЕЛЬНОСТИ:
Инструкция к лабораторно-практическому занятию.
Окисление формальдегида гидроксидом меди (II) в щелочном растворе.
Принцип метода: метод основан на реакции окисления альдегидов. Материальное обеспечение: пробирки, пипетки, 2Н раствор NaOH, 0,2H
раствор CuSO4 , 40% раствор формальдегида, дистиллированная вода.
Ход работы:
1.Поместите в пробирку 6 капель 2Н NaOH, разбавьте его 6 каплями воды и добавьте 1 каплю 0,2H CuSO4.
2.К выпавшему осадку добавьте 2-3 капли 40% раствора формалина и взболтайте раствор.
3.Нагрейте до кипения только верхнюю часть раствора так, чтобы нижняя часть раствора осталась для контроля холодной. В нагретой части пробирки выделится осадок, сначала жёлтый, затем красный.
O |
O |
|
HC + Cu(OH) |
|
HC + CuOH +H2O |
2 |
||
H |
OH |
|
Жёлтый осадок гидроксида меди (I) при нагревании легко теряет воду и превращается в оксид меди (I) красного цвета:
2CuOH → H2O + Cu2O
Это очень важная качественная реакция восстановительную способность. Она широко медицине как проба Троммера. В химии количественного определения.
на альдегидную группу, её применяется в биохимии и сахаров применяется для
Осаждение белковых тел формалином.
Принцип метода: метод основан на осаждении белковых тел формалином. Материальное обеспечение: Пробирки, раствор куриного белка, 40%
раствор формалина. Ход работы:
1.Налейте в пробирку 0.5 мл раствора куриного белка и добавьте несколько капель формалина.
2.Перемешайте – происходит свёртывание белка под действием формалина.
Цветная реакция на ацетон с нитропруссидом натрия.
Принцип метода: метод основан на открытии ацетона цветной реакцией с нитропруссидом.
Материальное обеспечение: пробирки, дистиллированная вода, раствор 2Н NaOH, раствор 0,5Н нитропруссида натрия. Na2[Fe(CN)5NO], водный раствор ацетона, раствор 2Н CH3COOH.
Ход работы:
1.Налейте в пробирку 1 каплю 0.5Н раствора нитропруссида натрия, 5 капель дистиллированной воды и 1 каплю водного раствора ацетона.
2.Добавьте 1 каплю 2Н раствора NaOH. Что вы наблюдаете?
3.Разлейте раствор в две пробирки и в одну пробирку добавьте 1 каплю 2Н раствора CH3COOH. Сравните окраску растворов в обеих пробирках.
4.Цветная реакция с нитропруссидом натрия (проба Легаля) широко применяется в клинической практике для открытия ацетона в моче при сахарном диабете.
НАБОР ЗАДАНИЙ ДЛЯ ПРОВЕРКИ ДОСТИЖЕНИЯ КОНКРЕТНЫХ ЦЕЛЕЙ ОБУЧЕНИЯ.
Задание №1.
Формалин используют как консервант для хранения биологических тканей. Среди приведенных формул найдите это соединение:
О
A.Н – С |
D. СН3 – О – СН3 |
|
Н |
|
О |
В. СН3ОН |
Е. Н – С |
|
ОН |
|
О |
С. СН3 |
СН3 |
|
Задание №2.
Состояние атома углевода карбонильной группы определяет характер и тип реакции соединений, которые её содержат.
Какое состояние гибридизации характерно для этого атома?
A.Sp-гибридизация с отрицательным зарядом.
B.Sp-гибридизация с положительным зарядом.
C.Sp²-гибридизация с отрицательным зарядом.
D.Sp²-гибридизация с положительным зарядом.
E.Sp²-гибридизация без электрического заряда.
Задание №3.
Реакции нуклеофильного присоединения характерны для альдегидов и кетонов. Укажите, чем обусловлен механизм этих реакций.
A.Эффектом ароматичности.
B.Отрицательным зарядом на атоме углерода карбонильной группы.
C.Отсутствием заряда на атоме углерода карбонильной группы
D.Положительным зарядом на атоме углерода карбонильной группы.
E.Эффектом сопряжения.
8
Задание №4.
Ацетон образуется в организме при различных нарушениях метаболизма. Укажите вещество, которое образуется в результате реакции восстановления этого соединения.
A.Пропан-1.
B.Пропан-2.
C.Пропановая кислота.
D.Пропаналь-1.
E.Пропаналь-2.
Задание №5.
Хлорирование пропионового альдегида обусловлено подвижностью одного из атомов водорода в радикале.
Укажите продукт этой реакции:
A.β-хлорпропионовый альдегид.
B.ά-хлорпропионовый альдегид.
C.ά-хлорпропионовая кислота.
D.Хлорацетон.
E.2-хлорпропан.
Задание №6.
Кетоны обладают более низкой реакционной способностью, чем альдегиды. Каким электронным эффектом это можно объяснить?
A.–M- эффектом заместителей.
B.+ M- эффектом заместителей.
C.– Ǐ- эффектом заместителей.
D.+ Ǐ - эффектом заместителей.
E.Эффектом сопряжения.
Задание №7.
В медицинской практике широко применяется формалин. Укажите 35-40% раствор этого вещества
A.Этаналя в воде.
B.Метаналя в воде.
C.Этанола в воде.
D.Метанола в воде.
E.2,3-диметилпропаналя в воде.
Приложение.
Задачи для достижения конкретных целей.
Задача №1.
Формальдегид применяется в производстве лекарственного средства уротропина.
Какие химические преобразования могут произойти при взаимодействии формальдегида с синильной кислотой?
9
Эталон ответа:
О
Формальдегид Н – С вступает в большое количество реакций, пред-
Н
ставляет собой одну из наиболее реакционных групп в соединениях.
Этап 1:
Взаимодействия метаналя с синильной кислотой, которая приводит к получению оксинитрила, осуществляется по механизму нуклеофильного присоединения.
Для повышения реакционной способности карбонильной группы применяется кислотный катализ, который приводит к увеличению положительного заряда на атоме углерода (повышение электро-
отрицательности): |
ОН+ |
|
О |
ОН |
|
Н – С + Н+ → Н – С |
→ Н – С+ |
|
Н |
Н |
Н |
Этап 2:
Протонированный метаналь присоединяет нуклеофильную часть молекулы
HCN.
Присоединение сопровождается выбросом протона и образованием оксинитрила:
OH |
OH |
H – C + |
+ CN ¯ → H – C ––– CN |
H |
H |
Вывод: При взаимодействии метаналя с синильной кислотой образуется оксинитрил по механизму нуклеофильного присоединения.
Задача №2.
Реакция получения полуацеталей лежит в основе образования циклических форм глюкозы. Какое химическое преобразование произойдёт с 5- гидроксигексаналем в кислой среде?
Эталон ответа:
5-гидроксигексаналь – гетерофункциональное соединение, которое содержит две функциональные группы: спиртовую и альдегидную, то есть оно сочетает в себе свойства спиртов и альдегидов.
О
CH3 – CH – CH 2 – CH 2 – CH 2 – C
| |
H |
OH
Все атомы углерода в углеводородном радикале находятся в Sp²гибридизованном состоянии, поэтому углеродная цепь может принимать
10
