
- •Примеры типовых экзаменационных задач
- •Раздел 1. Термохимия
- •1.1. Примеры задач с решениями
- •1.2. Вопросы для самоподготовки
- •Раздел 2. Энтропия и энергия Гиббса
- •2.1. Примеры задач с решениями
- •2.2. Вопросы для самоподготовки
- •Раздел 3. Химическая кинетика
- •3.1. Примеры задач с решениями
- •3.2. Вопросы для самоподготовки
- •Раздел 4. Химическое равновесие
- •Вопросы для самоподготовки
- •Раздел 5. Способы выражения концентрации растворов
- •Раздел 6. Ионное произведение воды. Водородный показатель
Вопросы для самоподготовки
Запишите выражения для Кс и Кр системы: 2Fe2O3(т) + 3С(т)
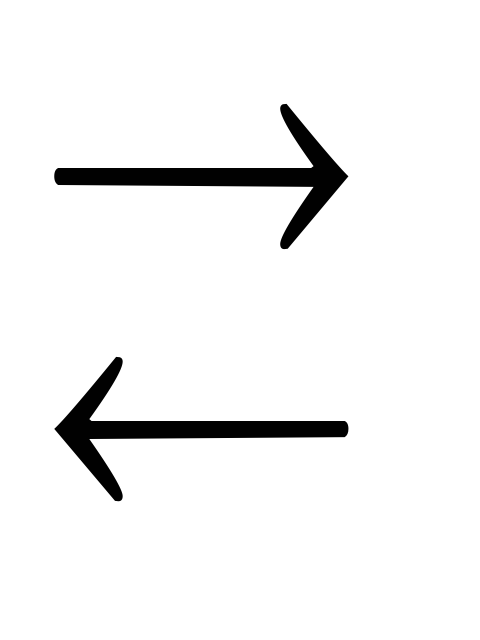 4Fe(т)
+
3CO2(г),
поясните смысл величин, входящих в эти
выражения, укажите их размерность.
Определите направление смещения
равновесия при повышении давления и
укажите, как при этом изменится
концентрация СО2.
4Fe(т)
+
3CO2(г),
поясните смысл величин, входящих в эти
выражения, укажите их размерность.
Определите направление смещения
равновесия при повышении давления и
укажите, как при этом изменится
концентрация СО2.Определите направление смещения равновесия в системе
H2O(г)
+ CO(г)
![]() H2(г)
+ CO2(г),
DH0
= -
41 кДж
H2(г)
+ CO2(г),
DH0
= -
41 кДж
а) при повышении концентрации СО; б) при понижении температуры. Ответ мотивируйте.
Определите направление смещения равновесия в системе
MnO2(т)
+
2C(т)
![]() Mn(т)
+
2CO(г)
Mn(т)
+
2CO(г)
при увеличении давления и укажите, как при этом изменяется концентрация CO.
Укажите, какое вещество будет накапливаться при повышении температуры в равновесной системе
C(т)
+
CO2(г)
![]() 2CO(г),
H0.
2CO(г),
H0.
Определите направление смещения равновесия
2ZnS(т)
+
3O2(г)
![]() 2ZnO(т)
+
2SO2(г)
2ZnO(т)
+
2SO2(г)
при увеличении давления.
Раздел 5. Способы выражения концентрации растворов
Рассчитайте, сколько граммов Na2SO3 требуется для приготовления 5 л 8% - го раствора ( = 1,075 г/мл).
Рассчитайте, какой объем 15 % - го раствора карбоната натрия ( = 1,16 г/мл) требуется для приготовления 5 л 2% - го раствора ( = 1,02 г/мл).
Рассчитайте процентное содержание гидроксида натрия в растворе, полученном добавлением к 1 л 30% - го раствора гидроксида натрия ( = 1,3 г/мл) трех литров воды.
Рассчитайте процентную концентрацию раствора соли, полученного смешением 400 г 10% - го раствора и 200 г 5% - го раствора этой соли.
Рассчитайте, какой объем 30% - го раствора КОН ( = 1,28 г/мл) необходим для приготовления 10 л 6% - го раствора ( = 1,04 г/мл).
Рассчитайте, в каком объеме 0,1 М раствора сульфата меди (II) содержится 8 г растворенного вещества.
Рассчитайте, сколько граммов K2SO4 требуется для приготовления 300 мл 0,5М раствора.
Рассчитайте молярную концентрацию раствора сульфата калия, 200 мл которого содержат 1,74 г растворенного вещества.
Раздел 6. Ионное произведение воды. Водородный показатель
Рассчитайте концентрации ионов Н+, ОН и рН в 0,001 М растворе HCl.
Рассчитайте концентрации ионов ОН, Н+ и рН в 0,01 М растворе NaОН.
Рассчитайте концентрацию Н+ и ОН - ионов (моль/л) в растворе с рН = 3.
Рассчитайте концентрацию ионов водорода (моль/л) и рН раствора с концентрацией гидроксид-ионов 105 моль/л.
Рассчитайте концентрацию гидроксид-ионов (моль/л) и рН раствора с концентрацией ионов водорода 108 моль/л.
