
химия
.docДейтерий и тритий также имеют орто- и парамодификации: p-D2, o-D2, p-T2, o-T2. Гетероизотопный водород (HD, HT, DT) не имеют орто- и парамодификаций.
[править]Свойства изотопов
Свойства изотопов водорода представлены в таблице[4][6].
|
Изотоп |
Z |
N |
Масса, а. е. м. |
Период полураспада |
Спин |
Содержание в природе, % |
Тип и энергия распада |
|
|
1H |
1 |
0 |
1,007 825 032 07(10) |
стабилен |
1⁄2+ |
99,9885(70) |
|
|
|
2H |
1 |
1 |
2,014 101 777 8(4) |
стабилен |
1+ |
0,0115(70) |
|
|
|
3H |
1 |
2 |
3,016 049 277 7(25) |
12,32(2) года |
1⁄2+ |
|
β− |
18,591(1) кэВ |
|
4H |
1 |
3 |
4,027 81(11) |
1,39(10)·10−22 с |
2− |
|
-n |
23,48(10) МэВ |
|
5H |
1 |
4 |
5,035 31(11) |
более 9,1·10−22 с |
(1⁄2+) |
|
-nn |
21,51(11) МэВ |
|
6H |
1 |
5 |
6,044 94(28) |
2,90(70)·10−22 с |
2− |
|
−3n |
24,27(26) МэВ |
|
7H |
1 |
6 |
7,052 75(108) |
2,3(6)·10−23 с |
1⁄2+ |
|
-nn |
23,03(101) МэВ |
В круглых скобках приведено среднеквадратическое отклонение значения в единицах последнего разряда соответствующего числа.
Свойства ядра 1H позволяют широко использовать ЯМР-спектроскопию в анализе органических веществ.
[править]Химические свойства
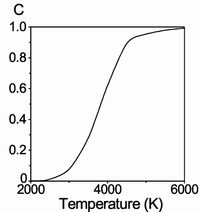
![]()
Доля диссоциировавших молекул водорода
Молекулы водорода достаточно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия:
![]()
Поэтому при обычных температурах водород реагирует только с очень активными металлами, например с кальцием, образуя гидрид кальция:
![]()
и с единственным неметаллом — фтором, образуя фтороводород:
![]()
С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии, например при освещении:
![]()
Он может «отнимать» кислород от некоторых оксидов, например:
![]()
Записанное уравнение отражает восстановительные свойства водорода.
![]()
С галогенами образует галогеноводороды:
![]() ,
реакция протекает со взрывом в темноте
и при любой температуре,
,
реакция протекает со взрывом в темноте
и при любой температуре,
![]() ,
реакция протекает со взрывом, только
на свету.
,
реакция протекает со взрывом, только
на свету.
С сажей взаимодействует при сильном нагревании:
![]()
[править]Взаимодействие со щелочными и щёлочноземельными металлами
При взаимодействии с активными металлами водород образует гидриды:
![]()
![]()
![]()
Гидриды — солеобразные, твёрдые вещества, легко гидролизуются:
![]()
[править]Взаимодействие с оксидами металлов (как правило, d-элементов)
Оксиды восстанавливаются до металлов:
![]()
![]()
![]()
[править]Гидрирование органических соединений
Молекулярный водород широко применяется в органическом синтезе для восстановления органических соединений. Эти процессы называют реакциями гидрирования. Эти реакции проводят в присутствии катализатора при повышенных давлении и температуре. Катализатор может быть как гомогенным (напр. Катализатор Уилкинсона), так и гетерогенным (напр.никель Ренея, палладий на угле).
Так, в частности, при каталитическом гидрировании ненасыщенных соединений, таких как алкены и алкины, образуются насыщенные соединения — алканы.
![]()
[править]Геохимия водорода
На Земле содержание водорода понижено по сравнению с Солнцем, планетами-гигантами и первичными метеоритами, из чего следует, что во время образования Земля была значительно дегазирована и водород вместе с другими летучими элементами покинул планету во время аккреции или вскоре после неё.
Свободный водород H2 относительно редко встречается в земных газах, но в виде воды он принимает исключительно важное участие в геохимических процессах.
В состав минералов водород может входить в виде иона аммония, гидроксил-иона и кристаллической воды.
В атмосфере водород непрерывно образуется в результате разложения воды солнечным излучением[7]. Имея малую массу, молекулы водорода обладают высокой скоростью диффузионного движения (она близка ко второй космической скорости) и, попадая в верхние слои атмосферы, могут улететь в космическое пространство.
[править]Меры предосторожности

Водород при смеси с воздухом образует взрывоопасную смесь — так называемый гремучий газ. Наибольшую взрывоопасность этот газ имеет при объёмном отношении водорода и кислорода 2:1, или водорода и воздуха приближённо 2:5, так как в воздухе кислорода содержится примерно 21 %. Также водород пожароопасен. Жидкий водород при попадании на кожу может вызвать сильное обморожение.
Считается, что взрывоопасные концентрации водорода с кислородом возникают от 4 % до 96 % объёмных. При смеси с воздухом от 4 % до 75 (74) % по объему. Такие цифры фигурируют сейчас в большинстве справочников, и ими вполне можно пользоваться для ориентировочных оценок. Однако, следует иметь в виду, что более поздние исследования (примерно конец 80-х) выявили, что водород в больших объёмах может быть взрывоопасен и при меньшей концентрации. Чем больше объём, тем меньшая концентрация водорода опасна.
Источник этой широко растиражированной ошибки в том, что взрывоопасность исследовалась в лабораториях на малых объёмах. Поскольку реакция водорода с кислородом — это цепная химическая реакция, которая проходит по свободнорадикальному механизму, «гибель» свободных радикалов на стенках (или, скажем, поверхности пылинок) критична для продолжения цепочки. В случаях, когда возможно создание «пограничных» концентраций в больших объёмах (помещения, ангары, цеха), следует иметь в виду, что реально взрывоопасная концентрация может отличаться от 4 % как в большую, так и в меньшую стороны.
[править]Экономика
Стоимость водорода при крупнооптовых поставках колеблется в диапазоне 2-5$ за кг[8]. В небольших количествах перевозится в стальных баллонах зелёного или тёмно-зелёного цвета.
[править]Применение
Атомарный водород используется для атомно-водородной сварки.
[править]Химическая промышленность
-
При производстве аммиака, метанола, мыла и пластмасс
[править]Пищевая промышленность
-
При производстве маргарина из жидких растительных масел.
-
Зарегистрирован в качестве пищевой добавки E949 (упаковочный газ, класс «Прочие»). Входит в список пищевых добавок, допустимых к применению в пищевой промышленности Российской Федерации в качестве вспомогательного средства для производства пищевой продукции.[источник не указан 725 дней]
[править]Авиационная промышленность
Водород очень лёгок и в воздухе всегда поднимается вверх. Когда-то дирижабли и воздушные шары наполняли водородом. Но в 30-х гг. XX в. произошло несколько катастроф, в ходе которых дирижабли взрывались и сгорали. В наше время дирижабли наполняют гелием, несмотря на его существенно более высокую стоимость.
[править]Топливо
Водород используют в качестве ракетного топлива.
Ведутся исследования по применению водорода как топлива для легковых и грузовых автомобилей. Водород в ДВС меньше загрязняет окружающую среду локально (из-за низкого КПД получения водорода и сопряжённых дополнительных расходов на его сжатие, транспортировку, водород как энергоноситель для ДВС совершенно неперспективен), но также как и бензиновые/дизельные аналоги, потребляет и деградирует моторное масло и все остальные неэкологичные материалы, присущие двигателям внутреннего сгорания. В смысле экологии электромобили значительно лучше, перспективен также двигатель Стирлинга.[источник не указан 60 дней]
В водородно-кислородных топливных элементах используется водород для непосредственного преобразования энергии химической реакции в электрическую.
[править]Интересные факты
-
Хорватское название водорода — Vodik, ввёл в употребление филолог Богослав Шулек.
Азот
[править]
Материал из Википедии — свободной энциклопедии
У этого термина существуют и другие значения, см. Азот (значения).
|
7
|
|||||
|
Внешний вид простого вещества |
|||||
|
|
|||||
|
Свойства атома |
|||||
|
Имя, символ, номер |
Азот / Nitrogenium (N), 7 |
||||
|
Атомная масса (молярная масса) |
14,00674 а. е. м. (г/моль) |
||||
|
Электронная конфигурация |
[He] 2s2 2p3 |
||||
|
Радиус атома |
92 пм |
||||
|
Химические свойства |
|||||
|
Ковалентный радиус |
75 пм |
||||
|
Радиус иона |
13 (+5e) 171 (-3e) пм |
||||
|
Электроотрицательность |
3,04[1] (шкала Полинга) |
||||
|
Степени окисления |
5, 4, 3, 2, 1, 0, −1, −3 |
||||
|
Энергия ионизации (первый электрон) |
1401,5 (14,53) кДж/моль (эВ) |
||||
|
Термодинамические свойства простого вещества |
|||||
|
Плотность (при н. у.) |
0,808 г/см³ (−195,8 °C); при н.у. 0,001251 г/см³ |
||||
|
Температура плавления |
63,29 К (-209,86 °C) |
||||
|
Температура кипения |
77,4 К (-195,75 °C) |
||||
|
Теплота плавления |
(N2) 0,720 кДж/моль |
||||
|
Теплота испарения |
(N2) 5,57 кДж/моль |
||||
|
Молярная теплоёмкость |
29,125[2] (газ N2) Дж/(K·моль) |
||||
|
Молярный объём |
17,3 см³/моль |
||||
|
Кристаллическая решётка простого вещества |
|||||
|
Структура решётки |
кубическая |
||||
|
Параметры решётки |
5,661 Å |
||||
|
Прочие характеристики |
|||||
|
Теплопроводность |
(300 K) 0,026 Вт/(м·К) |
||||
|
7 |
Азот |
|
N 14,007 |
|
|
2s22p3 |
|
Азо́т — элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) второго периодапериодической системы химических элементов Д. И. Менделеева, с атомным номером 7. Обозначается символом N(лат. Nitrogenium). Простое вещество азот (CAS-номер: 7727-37-9) — достаточно инертный при нормальных условиях двухатомный газ без цвета, вкуса и запаха (формула N2), из которого на три четверти состоит земная атмосфера.
|
Содержание [убрать]
|
[править]История открытия
В 1772 году Генри Кавендиш провёл следующий опыт: он многократно пропускал воздух над раскалённым углём, затем обрабатывал его щёлочью, в результате получался остаток, который Кавендиш назвал удушливым (или мефитическим) воздухом. С позиций современной химии ясно, что в реакции с раскалённым углём кислород воздуха связывался вуглекислый газ, который затем поглощался щёлочью. При этом остаток газа представлял собой по большей части азот. Таким образом, Кавендиш выделил азот, но не сумел понять, что это новое простое вещество (химический элемент). В том же году Кавендиш сообщил об этом опыте Джозефу Пристли.
Пристли в это время проводил серию экспериментов, в которых также связывал кислород воздуха и удалял полученный углекислый газ, то есть также получал азот, однако, будучи сторонником господствующей в те времена теории флогистона, совершенно неверно истолковал полученные результаты (по его мнению, процесс был противоположным — не кислород удалялся из газовой смеси, а наоборот, в результате обжига воздух насыщался флогистоном; оставшийся воздух (азот) он и назвал насыщенным флогистоном, то есть флогистированным). Очевидно, что и Пристли, хотя и смог выделить азот, не сумел понять сути своего открытия, поэтому и не считается первооткрывателем азота.
Одновременно схожие эксперименты с тем же результатом проводил и Карл Шееле.
В 1772 году азот (под названием «испорченного воздуха») как простое вещество описал Даниэль Резерфорд, он опубликовал магистерскую диссертацию, где указал основные свойства азота (не реагирует со щелочами, не поддерживает горения, непригоден для дыхания). Именно Даниэль Резерфорд и считается первооткрывателем азота. Однако и Резерфорд был сторонником флогистонной теории, поэтому также не смог понять, что же он выделил. Таким образом, чётко определить первооткрывателя азота невозможно.
В дальнейшем азот был изучен Генри Кавендишем (интересен тот факт, что он сумел связать азот с кислородом при помощи разрядов электрического тока, а после поглощения оксидов азота в остатке получил небольшое количество газа, абсолютно инертного, хотя, как и в случае с азотом, не смог понять, что выделил новый химический элемент — инертный газ аргон).
[править]Происхождение названия
Азо́т (от др.-греч. ἄζωτος — безжизненный, лат. nitrogenium), вместо предыдущих названий («флогистированный», «мефитический» и «испорченный» воздух) предложил в 1787 годуАнтуан Лавуазье, который в то время в составе группы других французских учёных разрабатывал принципы химической номенклатуры. Как показано выше, в то время уже было известно, что азот не поддерживает ни горения, ни дыхания. Это свойство и сочли наиболее важным. Хотя впоследствии выяснилось, что азот, наоборот, крайне необходим для всех живых существ, название сохранилось во французском и русском языках.
Существует и иная версия[3]. Слово «азот» придумано не Лавуазье и не его коллегами по номенклатурной комиссии; оно вошло в алхимическую литературу уже в раннемсредневековье и употреблялось для обозначения «первичной материи металлов», которую считали «альфой и омегой» всего сущего. Это выражение заимствовано из Апокалипсиса: «Я есмь Альфа и Омега, начало и конец» (Откр.1:8-10). Слово составлено из начальных и конечных букв алфавитов трёх языков — латинского, греческого и древнееврейского, — считавшихся «священными», поскольку, согласно Евангелиям, надпись на кресте при распятии Христа была сделана на этих языках (а, альфа, алеф и зет, омега, тав — AAAZOTH). Составители новой химической номенклатуры хорошо знали о существовании этого слова; инициатор её создания Гитон де Морво отмечал в своей «Методической энциклопедии» (1786) алхимическое значение термина.
Возможно, слово «азот» произошло от одного из двух арабских слов — либо от слова «аз-зат» («сущность» или «внутреннюю реальность»), либо от слова «зибак» («ртуть»)..
На латыни азот называется «nitrogenium», то есть «рождающий селитру»; английское название производится от латинского. В немецком языке используется название Stickstoff, что означает «удушающее вещество».
[править]Азот в природе
[править]Изотопы
Основная статья: Изотопы азота
Природный азот состоит из двух стабильных изотопов 14N — 99,635 % и 15N — 0,365 %.
Искусственно получены четырнадцать радиоактивных изотопов азота с массовыми числами от 10 до 13 и от 16 до 25. Все они являются очень короткоживущими изотопами. Самый стабильный из них 13N имеет период полураспада 10 мин.
Спин ядер стабильных изотопов азота: 14N — 1; 15N — 1/2.
[править]Распространённость
Вне пределов Земли азот обнаружен в газовых туманностях, солнечной атмосфере, на Уране, Нептуне, межзвёздном пространстве и др. Азот — четвёртый по распространённости элемент Солнечной системы (после водорода, гелия и кислорода).
Азот, в форме двухатомных молекул N2 составляет большую часть атмосферы, где его содержание составляет 75,6 % (по массе) или 78,084 % (по объёму), то есть около 3,87·1015 т.
Содержание азота в земной коре, по данным разных авторов, составляет (0,7—1,5)·1015 т (причём в гумусе — порядка 6·1010 т), а в мантии Земли — 1,3·1016 т. Такое соотношение масс заставляет предположить, что главным источником азота служит верхняя часть мантии, откуда он поступает в другие оболочки Земли с извержениями вулканов.
Масса растворённого в гидросфере азота, учитывая, что одновременно происходят процессы растворения азота атмосферы в воде и выделения его в атмосферу, составляет около 2·1013 т, кроме того примерно 7·1011 т азота содержатся в гидросфере в виде соединений.
[править]Биологическая роль
Азот является элементом, необходимым для существования животных и растений, он входит в состав белков (16—18 % по массе), аминокислот, нуклеиновых кислот, нуклеопротеидов,хлорофилла, гемоглобина и др. В составе живых клеток по числу атомов азота около 2 %, по массовой доле — около 2,5 % (четвёртое место после водорода, углерода и кислорода). В связи с этим значительное количество связанного азота содержится в живых организмах, «мёртвой органике» и дисперсном веществе морей и океанов. Это количество оценивается примерно в 1,9·1011 т. В результате процессов гниения и разложения азотсодержащей органики, при условии благоприятных факторов окружающей среды, могут образоваться природные залежи полезных ископаемых, содержащие азот, например, «чилийская селитра» (нитрат натрия с примесями других соединений), норвежская, индийская селитры.
[править]Круговорот азота в природе
Основная статья: Круговорот азота
Фиксация атмосферного азота в природе происходит по двум основным направлениям — абиогенному и биогенному. Первый путь включает главным образом реакции азота с кислородом. Так как азот химически весьма инертен, для окисления требуются большие количества энергии (высокие температуры). Эти условия достигаются при разрядах молний, когда температура достигает 25000 °C и более. При этом происходит образование различных оксидов азота. Существует также вероятность, что абиотическая фиксация происходит в результате фотокаталитических реакций на поверхности полупроводников или широкополосных диэлектриков (песок пустынь).

 Жидкий
азот. При н.у. — газ без
цвета, вкуса и запаха.
Жидкий
азот. При н.у. — газ без
цвета, вкуса и запаха.