
- •Часть 1 учебное пособие
- •Часть 1
- •1. Обшие сведения об атмосфере и загрязняющих веществах
- •1.1. Структура и состав атмосферы
- •1.2. Классификация загрязнений атмосферы
- •1.3. Загрязнение атмосферы в результате хозяйственной деятельности человека
- •1.4. Основные загрязняющие вещества атмосферного воздуха
- •1.5. Химические превращения загрязняющих веществ в атмосфере
- •1.5.1.Свободные радикалы в атмосфере
- •1.5.2.Химические превращения соединений серы
- •1.5.3. Химические превращения соединений азота
- •1.5.5.Фотохимический смог в городской атмосфере
- •1.6. Химические основы воздействия загрязняющих веществ на окружающую
- •1.6.3.2. Воздействие оксидов азота на материалы
- •1.6.3.4.Влияние аэрозолей на материалы
- •2. Общие сведения о литосфере
- •2.1.Структура и состав литосферы. Формирование почвы, ее значение
- •2.2.Составные части почвы
- •2.3.Свойства почвы
- •2.4. Загрязнение почв
- •Часть 1
1.5.2.Химические превращения соединений серы
Основные поступления соединений серы в тропосферу связаны с антропогенными источниками. Как было отмечено выше, в атмосфере происходят процессы окисления соединений серы при участии свободных радикалов. В частности, сероводород окисляется последовательно в несколько ступеней до диоксида серы:
H2S + OH HS + H2O, HS + O2ОН+SO, SO + HO2 SO2 + OH.
Диоксид серы, образующийся при окислении сероводорода, также, как и диоксид серы, поступающий их антропогенных источников, подвергается дальнейшему окислению.
Окисление диоксида серы связывают с переходом его в возбужденное состояние и последующее взаимодействие с молекулярным кислородом:
SO2 + h SO2*, SO2* + 2O2 SO3 + O3, SO3 + H2O H2SO4
Окисление диоксида серы значительно ускоряется в присутствии оксидов азота или углеводородов; в этом случае возможно протекание процессов с участием атомарного кислорода :
SO2 + O + M SO3 + M, где М - третье тело, которому передается энергия.
Однако, как показали исследования, этот процесс становится значительным только на высоте более 10 км при концентрации диоксида серы около 1 мкгм-3. Поэтому реакция окисления диоксида серы атомарным кислородом не играет существенной роли для процессов трансформации соединений серы в тропосфере. Ведущую роль здесь играют свободные радикалы:
SO2 + OH + M HSO3 + M, HSO3 + HO2 SO3 + 2 OH, SO2 + HO2 SO3 + OH.
Триоксид серы легко взаимодействует с атмосферной влагой с образованием раствора серной кислоты : SO3 + H2O H2SO4 .
Реагируя с аммиаком или ионами металлов, присутствующими в каплях атмосферной влаги, серна кислота частично переходит в сульфаты (сульфаты аммония, натрия, кальция). Образование сульфатов происходит и в процессе окисления на поверхности твердых аэрозолей:
SO2 + CaO CaSO3, SO2 + MgO MgSO3.
В дальнейшем, при взаимодействии с молекулярным кислородом, сульфиты переходят в соответствующие сульфаты. Оксиды железа, алюминия, хрома и других металлов существенно ускоряют реакции окисления диоксида серы, выступая в роли катализатора.
В дождливую погоду и при высокой влажности атмосферного воздуха окислению основного количества диоксида серы предшествует стадия растворения и гидролиза в каплях атмосферной влаги. В растворах, образующихся при этом, устанавливается динамическое равновесие между растворенным в воде диоксидом серы и ионами бисульфита и сульфита. Соотношение концентраций SO2, HSO3, SO3 в растворе определяется, в основном, величиной активности ионов водорода. При рН раствора менее 3.5 в воде практически отсутствуют ионы бисульфита и нет сульфит -ионов, а доля диоксида серы близка к единице. С увеличением рН до 7 и выше доля соединений серы в форме диоксида серы снижается до нуля. В этих растворах преобладают бисульфит - и сульфит -ионы, которые легко окисляются в присутствии растворенного кислорода или озона.
Установлено, что при окислении диоксида серы в жидкой фазе активное участие принимают и свободные радикалы, в частности, ОН и НОО. Конечным продуктом окисления диоксида серы в растворе, как и в случае окисления в газовой фазе, является серная кислота. Она образуется, главным образом, в виде жидкого аэрозоля и обладает малой скоростью оседания.
Сернокислотный аэрозоль и диоксид серы могут вымываться из атмосферы с осадками и адсорбироваться почвой.
На рис. 1.5. представлена схема атмосферного цикла соединений серы, которая наглядно иллюстрирует основные химические превращения сероводорода и диоксида серы в атмосфере.





 SO2 H2SO4
SO2 H2SO4

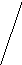




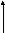 в жидкой фазе, О2,
ОН, НОО
в жидкой фазе, О2,
ОН, НОО
OH,HOO к7
антропогенные в твер- NH4 к8
 выбросы
дой фазе
выбросы
дой фазе


 H2S
к2
H2S
к2
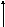 MeSO4
MeSO4
к
3 к4
к4
Природные поступления
с оединений
серы к6
к1
к5
к6
оединений
серы к6
к1
к5
к6



Вывод из атмосферы
Рис. 5. Атмосферный цикл соединений серы
к1- к6 - константы скоростей процессов сухого осаждения и вымывания из атмосферы
диоксида серы, сульфатов металлов, серной кислоты; к7 -константа химического превращения диоксида серы в серную кислоту; к8 -константа скорости процесса образования сульфатов в атмосфере.
Для среднеевропейских условий константы имеют следующие значения: к1=к4 =к6=к8= =0.03 ч-1; к2=0.025 ч-1; к3=к5 =0.01 ч-1; к7=0.1 ч-1.
