
- •Часть 1 учебное пособие
- •Часть 1
- •1. Обшие сведения об атмосфере и загрязняющих веществах
- •1.1. Структура и состав атмосферы
- •1.2. Классификация загрязнений атмосферы
- •1.3. Загрязнение атмосферы в результате хозяйственной деятельности человека
- •1.4. Основные загрязняющие вещества атмосферного воздуха
- •1.5. Химические превращения загрязняющих веществ в атмосфере
- •1.5.1.Свободные радикалы в атмосфере
- •1.5.2.Химические превращения соединений серы
- •1.5.3. Химические превращения соединений азота
- •1.5.5.Фотохимический смог в городской атмосфере
- •1.6. Химические основы воздействия загрязняющих веществ на окружающую
- •1.6.3.2. Воздействие оксидов азота на материалы
- •1.6.3.4.Влияние аэрозолей на материалы
- •2. Общие сведения о литосфере
- •2.1.Структура и состав литосферы. Формирование почвы, ее значение
- •2.2.Составные части почвы
- •2.3.Свойства почвы
- •2.4. Загрязнение почв
- •Часть 1
1.5.3. Химические превращения соединений азота
Соединения азота в тропосфере представлены в основном оксидами азота, аммиаком и солями аммония, а также азотной кислотой и нитратами. Среди оксидов азота следует выделить гемиоксид (N2O), монооксид и диоксид азота; другие оксиды азота в условиях тропосферы неустойчивы.
Основные процессы вывода гемиоксида азота из атмосферы связывают с протеканием фотодиссоциации: N2O + h N2 + O или взаимодействием : N2O + O N2 + O2, N2O + O 2 NO.
Поскольку в тропосфере концентрация О является низкой и практически отсутствует излучение с длиной волны около 250 нм, молекулы N2O являются устойчивыми; в стратосфере концентрация О увеличивается, изменяется спектр солнечного излучения, что и приводит к увеличению скорости разрушения молекул гемиоксида азота. Так, концентрация N2O на высоте 35 км примерно в 10 раз меньше, чем в тропосфере.
Монооксид и диоксид азота в атмосфере подвергаются взаимным превращениям; NO, взаимодействуя с НОО или с озоном, переходит в диоксид азота (константы скоростей реакций при 298 К равны, соответственно 8.410-12 и 1.810-14 млмоль-1с-1.
В реакциях, в которых участвует диоксид азота, поглощение ультрафиолетового излучения ( = 410 нм) приводит к разрыву одной связи между атомами азота и кислорода с образованием молекулярного кислорода и монооксида азота. Последующие реакции приводят к образованию молекулярного кислорода и озона и регенерации диоксида азота. Эти реакции можно представить в виде:
NO2 +h NO + O, NO2 + O NO + O2, O + O2 O3, NO + O3 NO2 + O2
Регенерированный диоксид азота может вновь вступить в реакцию и, таким образом, этот процесс многократно повторяется до тех пор, пока диоксид азота не превратится в азотную кислоту или в нитросоединение. Даже малые концентрации диоксида азота в атмосфере могут явиться причиной образования значительных количеств атомарного кислорода и озона.
Важной частью атмосферного цикла соединений азота является образование азотной кислоты. Примерно 44% кислоты в тропосфере образуется в результате взаимодействия диоксида азота с гидроксильным радикалом, около 24% кислоты появляется в атмосфере в результате взаимодействия пентаоксида диазота с молекулами воды и до 28% от всей образующейся в атмосфере кислоты образуется при взаимодействии триоксида азота с органическими кислородсодержащими радикалами. Часть азотной кислоты разлагается с образованием диоксида и триоксида азота, которые вновь включаются в атмосферный цикл ( см.рис.1. 6).
Основное количество азотной кислоты выводится из атмосферы с осадками в виде растворов и солей. Из нитратов, присутствующих в атмосфере, основное количество составляет азотнокислый аммоний, который образуется при взаимодействии паров кислоты с аммиаком.
Ежегодно из природных источников в атмосферу поступает около 70 млн т аммиака в пересчете на азот; антропогенный вклад составляет около 4 млн т.
1.5.4. Химические превращения органических соединений
Алканы составляют большую часть углеводородов (УВ), присутствующих в атмосфере. Основным из них является метан, фоновая концентрация которого в среднем составляет 1.4 млн -1 В обычных атмосферных условиях единственной реакцией, врезультате которой происходит расходование алканов, является взаимодействие с радикалами ОН:
ОН + RCH2R1 H2O + RCHR1
 ОН,
О3
OH
ОН,
О3
OH





NH3 ОН NO NO2 HNO3








 h
h
h
h
природные антропогенные
соединения выбросы



NH4NO3
вывод из
атмосферы
Рис. 1.6. Атмосферный цикл соединений азота
Константы скоростей реакций (мл/мольс) взаимодействия алканов с радикалами ОН приведены ниже: метан -8.110-15, этан -3.010-12, пропан -1.910-12, бутан -2.410-12, пентан -5.010-12.
В случае простых алканов (С3) далее протекают реакции:
RCHR1 + O2 RR1CHOO, RR1CHOO + NO RR1CHO + NO2, RR1CHOO+NO2RR1CHO2NO2,
RR1CHO + O2 RCOR1 + HO2
 RCHO
+ R1
RCHO
+ R1
R R1CHO
разложение
R1CHO
разложение
R1CHO + R
и регенерация радикала ОН, ведущего цепь:
HO2 + NO OH + NO2
Приведенная выше схема справедлива для низших алканов. В других случаях возможно протекание реакций с участием радикалов RO2 и RO.
Из схемы следует возможность образования алкил-нитратов. С повышением числа углеродных атомов алкоксидные радикалы имеют тенденцию не столько к взаимодействию с кислородом или мономолекулярному распаду, сколько к изомеризации. В случае н -бутана доля изомеризации составляет 15%, н -пентана -7% от общего числа алкоксидных радикалов. Изомерия носит последовательный характер: после протекания первичной изомеризации может быть вторая, третья и в присутствии кислорода и диоксида азота заканчивается образованием спиртов, кетонов с достаточно высокой молекулярной массой и, в итоге, может привести к образованию аэрозоля.
Значение реакций образования нитрата и изомеризации для алканов с длинными углеродными цепями еще более возрастает с увеличением парка автомобилей, работающих на дизельном топливе, так как в выхлопных газах содержится больше соединений с длинной углеродной цепью, чем в случае бензиновых двигателей.
Алкены. При обычных атмосферных условиях алкены в основном взаимодействуют с озоном и радикалами ОН. Константы скорости (мл/мольс 1012) реакций с радикалами ОН достаточно точно определены для большинства алкенов, в частности:
этилен -2.2, пропилен -25, бутилен -1 - 7.4, транс бутилен -2 -1.14.
В случае этилена и метилзамещенных этиленов радикал ОН присоединяется к двойной связи. Однако для алкенов, содержащих боковые цепи более, чем с двумя атомами углерода, значительная доля радикалов ОН (20 -25%) расходуется по реакции отрыва атома Н от ослабленных аллильных связей С - Н:
OH + CH2=CHCH2CH3 HOCH2CHCH2CH3 + CH2CHOHCH2CH3 H2O+CH2=CHCHCH3
присоединение радикала ОН отрыв атома Н
Радикал СН2 СНСНСН3 способен присоединять кислород с образованием пероксидного радикала:
 СН2=СН
– СН - ОО
СН2=СН
– СН - ОО
СН3
Этот радикал способен не только взаимодействовать с NO, образуя соответствующий алкоксидный радикал, но и подвергаться циклизации:
 NO
O
NO
O
С

 Н2=
СН
– СН
– СН3
NO2
+ CH2=CHCHCH3
Н2=
СН
– СН
– СН3
NO2
+ CH2=CHCHCH3
ОО


 циклизация
СН2
-СН
циклизация
СН2
-СН

 СН
–СН3
СН
–СН3
О -О
В результате происходит накопление кетонов, акролеина. При взаимодействии алкенов с озоном возможными продуктами являются озониды:



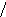

 R1
R3
R1
O O R3
R1COR2
+ [R3R4COO]*
R1
R3
R1
O O R3
R1COR2
+ [R3R4COO]*
O
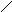

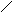
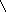


 3
+ C=C C - C
3
+ C=C C - C
 R2
R4
R2
R4
R3COR4
+ [R1R2COO]*
R2
R4
R2
R4
R3COR4
+ [R1R2COO]*
Знак [ ]* обозначает возбужденные частицы с высокой энергией.
Образование вторичных озонидов свидетельствует о том, что значительная часть (20 -40%) бирадикалов с высокой энергией в атмосферных условиях подвергается перегруппировке и (или) разложению с образованием СО, ОН, СО2, альдегидов.
Ароматические углеводороды. Расходование ароматических углеводородов в атмосфере протекает, главным образом, вследствие взаимодействия с радикалами ОН
OH + C6H5CH3 + O2 OH2 + C6H5CH2O2 (бензальдегид)
с образованием бензальдегида (15%) и бициклических радикалов (85%), которые могут присоединять кислород, реагировать с NO по аналогии с алкильными радикалами. Далее происходит самопроизвольное разложение образовавшихся оксидных радикалов с образованием альдегидов, кетонов.
Кислородсодержащие производные углеводородов. Основными производными, представляющими интерес в отношении химии атмосферы являются альдегиды и кетоны. Альдегиды представляют собой один из основных продуктов окисления углеводородов. В результате их превращений может образоваться значительное количество свободных радикалов: HO2, RO2. В атмосфере формальдегид подвергается фотолизу и взаимодействует с радикалами ОН:
НСНО + h H + HCO
HCHO + h H2 + CO
HCHO + h HO2 + CO + H2O
Радикальные продукты первой реакции превращаются далее с образованием радикала НОО:
H + O2 + M HO2 + M
HCO + O2 HO2 + CO
Ацетальдегид также реагирует с радикалами ОН, образуя ацетильный радикал СНННСО, который превращается далее:

 CH3CO
+ O2
+ NO2
CH3
– C – O – O – NO2
CH3CO
+ O2
+ NO2
CH3
– C – O – O – NO2
O
Образующееся соединение - пероксиацетилнитрат вступает в реакцию с NO
CH3CO OO –NO2 + NO 2NO2 + CH3CO2 ,
а затем распадается в конденсированной фазе:

 OH
+ CH3
– CO – OONO2
CH3COOH
+ NO2
+ O2
OH
+ CH3
– CO – OONO2
CH3COOH
+ NO2
+ O2
Кроме альдегидов в городских районах тропосферы возможно присутствие кетонов, спиртов, простых эфиров. Кетоны, также как и альдегиды, подвергаются фотолизу с образованием свободных радикалов, инициирующих окисление монооксида до диокида азота и способствующих образованию фотохимического смога.
Биогенные углеводороды. Углеводороды, образующие из биогенных источников, могут играть существенную роль в сельских районах. Многие биогенные углеводороды быстро реагируют с озоном и радикалами ОН, эффективно способствуют образованию озона при фотоокислении в присутствии оксидов азота (в условиях смога).
К настоящему времени наиболее подробно изучены два углеводорода: изопрен и -пинен. Изопрен выделяется лиственными деревьями - дубом, платаном и эвкалиптом, а -пинен выделяют, в основном, хвойные деревья, такие, как сосна и пихта. Определено, что продуктами фотоокисления изопрена (С5Н7) являются метилвинилкетон и метакролеин. Изопрен эффективно способствует окислению оксидов азота за счет образования органических и неорганических радикалов. Изопрен и два упомянутых продукта его превращения реагируют как с радикалами ОН, так и с озоном.
В целом биогенные углеводороды обладают высокой реакционной способностью и, хотя их концентрации в атмосфере невелики, их необходимо учитывать при проведении региональных исследований и обследований.
