
Работа № 5
Изучение фотолиза триптофана и триптофановых остатков в белках под действием уф-излучением методом флуориметрии
Теоретическое введение
Количественный флуориметрический анализ
Флуориметрический анализ весьма широко используется для количественного определения содержания веществ, способных к флуоресценции. Метод основан на регистрации собственного (первичного) или вторичного излучения света исследуемыми молекулами. Вторичное излучение исследуется в следующих случаях: (1) исследуемая молекула испускает излучение в неудобной спектральной области и (2) исследуемая молекула вообще не способна к флуоресценции. В тех случаях, когда флуоресцирующие молекулы в изучаемом объекте отсутствуют, или их флуоресценция очень слаба или неудобно расположена в спектральном плане, можно специально ввести в объект подобные соединения (флуоресцентные зонды или флуоресцентные метки), связывающиеся нековалентно (зонды) или ковалентно (метки) с исследуемыми молекулами. Другой вариант действий в такой ситуации – химическая модификация исследуемых соединений с целью их трансформации в продукты, способные к интенсивной флуоресценции.
Для того, чтобы можно было определить количество флуорофора (испускающего флуоресценцию вещества) в объекте, необходимо знать, как зависит интенсивность его флуоресценции от концентрации. Мы не будет приводить здесь полный вывод этой зависимости, который доступен в литературе (см., например, Владимиров Ю.А., Потапенко А.Я. Физико-химические основы фотобиологических процессов. М.: «Дрофа», 2006, с. 40). Напомним, что эта зависимость имеет следующий вид:
![]()
где Jф– интенсивность флуоресценции исследуемого вещества;J0– интенсивность падающего на образец возбуждающего света;k – коэффициент, отражающий чувствительность флуориметра,q – квантовый выход флуоресценции (доля поглощенных квантов, которые излучаются в виде квантов флуоресценции);- молярный коэффициент поглощения флуорофора на длине волны возбуждающего света,с– молярная концентрация флуорофора в объекте,l –длина оптического пути. Произведение сl = D, оптической плотности объекта, обусловленной флуорофором.
При малых концентрациях (и, следовательно, оптических плотностях) исследуемого флуорофора эта формула упрощается:
![]()
Обратите внимание на то, что в общем случае зависимость Jфнелинейна (носит экспоненциальный характер), тогда как линейная зависимость между концентрацией флуорофора в объекте и интенсивностью флуоресценции выполняется в очень ограниченных пределах оптической плотности, причем эти пределы для данного конкретного флуорофора, как правило, заранее неизвестны. Поэтому при решении количественной флуориметрической задачи обычно изначально измеряются калибровочные зависимости (Jф=f(c)) с использованием чистых растворов определяемого вещества с известной концентрацией, которые затем и используются для определения количества флуорофора в объекте. При этом, естественно, необходимо, чтобы флуоресценция исследуемого вещества в объекте была такой же, как и при построении калибровочной зависимости. Однако, в биологических объектах очень часто имеют место явления, очень сильно влияющие на измеряемую величинуJф. Этоэкранировка возбуждающего света, реабсорбция флуоресценции, ее тушение, светорассеивание и неоднородное распределение исследуемого соединения по объему объекта.
Поскольку степень воздействия всех этих явлений на величину Jфзависит от применяемой схемы измерения этого показателя, сначала рассмотрим этот вопрос.
Применяется 3 основные схемы регистрации Jф, различающиеся углом между направлениями падения возбуждающего светаJ0на объект, и регистрации квантов флуоресценции. Этот угол может быть (1) тупым; (2) 900; (3) 00(рис. 1). Использование схем (1) и (2) возможно потому, что флуоресценция, как правило, изотропно распределена в пространстве, т.е. кванты флуоресцении могут с одинаковой вероятностью покидать объект в любом направлении. Во всех случаях для отделения квантов флуоресценции от квантов возбуждающего света применяются либо светофильтры, либо монохроматоры (иногда – комбинация этих устройств).
Регистрируемый фотосигнал при измерении флуоресценции будет складываться из собственно Jф, и квантов так называемогопаразитного света.
Паразитный (или «рассеянный») свет складывается из следующих компонентов: (1) части излучения источника возбуждающего света в области флуоресценции исследуемого вещества, проходящей через монохроматор из-за его неидеальности; (2) света, возникающего из-за комбинационного рассеивания возбуждающего излучения (так называемый «красный спутник»; если излучение рассеивается молекулами воды, то это излучение смещено на 20-50 нм в длинноволновую сторону относительно длины волны возбуждающего света); (3) люминесценции кюветы и растворителя. Влияние на результаты флуориметрии компоненты (1) паразитного света будет особенно велико при угле между направлениями возбуждения и регистрации флуоресценции, равном 0о(схема 3 на рис. 1, называется также «регистрацией флуоресценции в проходящем свете»). Поэтому такая схема измеренияJфприменяется очень редко. При применении схем (1) и (2) на рис. 1 влияние паразитного света будет значительно только при сильном светорассеивании в исследуемом объекте.
Эффект экранировки возбуждающего света наблюдается в тех случаях, когда в объекте, помимо исследуемого флуорофора, содержатся и другие вещества, способные поглощать возбуждающий свет. Нужно заметить, что в биологических объектах такая ситуация обычна. Из-за того, что часть квантов возбуждающего излучения поглощается другими молекулами и не вызывает возбуждения молекул изучаемого флуорофора, величинаJф оказывается заниженной. При количественном флуориметрическом анализе неучет эффекта экранировки приводит к занижению результата измерений, т.е. неправильной оценке содержания вещества в объекте. Для того, чтобы избежать этого, определяется поправочный коэффициент на экранировку возбуждающего излучения,э, с помощью которого затем корректируются измеренные величиныJф:


![]()
где Jф– интенсивность флуоресценции с поправкой на экранировку;Jф’ – измеренная интенсивность флуоресценции,D– оптическая плотность исследуемого флуорофора в объекте, аDэ – суммарная оптическая плотность всех содержащихся в нем экранирующих возбуждающее излучение примесей. Вывод приводимых выше формул для расчета поправки на эффект экранировки содержится в первом издании этого практикума. К сожалению, для расчета поправочного коэффициента требуется знаниеD, а это, собственно, и является решением задачи количественной флуориметрии. Но, если общая оптическая плотность объекта (Dоб= D+ Dэ) достаточно мала (Dоб<<1),э будет близок к единице, т.е. экранировкой в сильно разбавленных образцах можно пренебречь. Правда, при разведении падает концентрация определяемого флуорофора, а следовательно - чувствительность флуориметрического количественно анализа.
Эффект реабсорбции квантов флуоресценции состоит в повторном поглощении этих квантов другими молекулами, присутствующими в объекте. При этом в качестве реабсорбирующих молекул могут выступать не только примеси, но и собственно молекулы исследуемого вещества (если спектры его поглощения и флуоресценции перекрываются). В последнем случае принято говорить особственной реабсорбции. Поскольку наличие реабсорбции приводит к снижениюJф с теми длинами волн, которые реабсорбируются, а при собственной реабсорбции поглощаются коротковолновые кванты флуоресценции, наличие этого эффекта приводит к кажущемуся длинноволновому сдвигу максимума в регистрируемом спектре флуоресценции. Если же реабсорбция осуществляется веществами-примесями, регистрируемый спектр флуоресценции может быть искажен различным образом, в зависимости от того, какие кванты флуоресценции реабсорбируются. Искажение спектров флуоресценции вследствие реабсорбции осложняет качественный флуориметрический анализ, основанный на исследовании этих спектров, а снижение величиныJфвследствие этого явления искажает результаты количественного. Как и в случае экранировки, искаженные вследствие реабсорбции результаты флуориметрии можно выправить с помощью поправочного коэффициентар. Для получения истинной величиныJфизмеренные значения интенсивности флуоресценции умножают на соответствующийр. Собственно жеропределяется на каждой из длин волн по формуле:
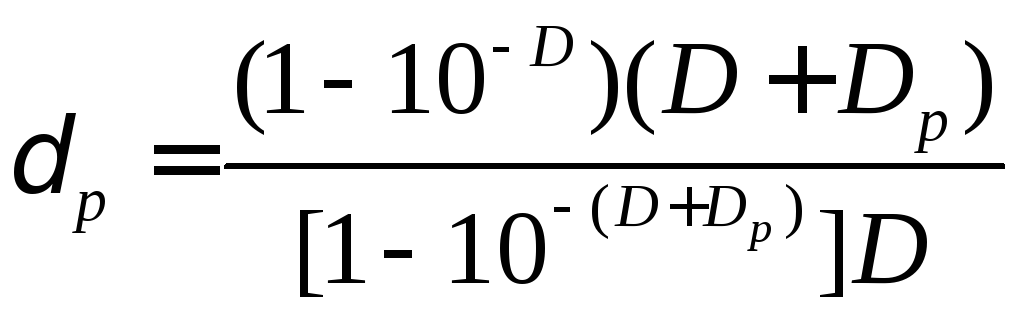
Обозначения в этой формуле те же, что и формуле для расчета э, толькоDэ заменено наDp – суммарную оптическую плотность всех реабсорбирующих флуоресценцию соединений. Как и в случае экранировки возбуждающего света, влияние реабсорбции флуоресценции на результаты флуориметрии падает при снижении оптической плотности объекта (т.е. его разведении). Однако, поскольку этот прием может существенно снизить точность флуориметрического анализа из-за снижения концентрации определяемого флуорофора, чаще прибегают к экспериментальным способам ослабления экранировки и реабсорции. В частности, оба этих явления относительно слабо влияют на регистрируемуюJфпри применении схемы регистрации флуоресценции (1) на рис. 1 (такой способ принято называть «регистрацией флуоресценции с передней стенки кюветы»).
Миграцией энергииназывается безизлучательный перенос энергии электронного возбуждения с одной молекулы (донора) на другую (акцептор) на расстояния, превышающие межатомные, и не связанный с соударением молекул. Реально наличие миграции энергии приводит к снижениюJф молекулы-донора за счет снижения величины квантового выхода ее флуоресценции (q). Для устранения миграции следует тем или иным способом увеличить расстояние между донором и акцептором – вероятность миграции энергии обратно пропорциональна этому расстоянию в 6-й степени. Из-за столь сильной зависимости от расстояния между донором и акцептором в истинных растворах миграция энергии на практике не наблюдается, если только донор и акцептор не входит в состав одного надмолекулярного комплекса и не находятся достаточно близко друг к другу. Более подробно явление миграции энергии будет рассмотрено в теоретическом введении к работе №7.
Тушение флуоресценции– снижение величиныJфза счет паденияq,вызванного воздействием молекул-тушителей. Во время взаимодействия с тушителем энергия возбужденного электрона, как правило, растрачивается на тепловые колебания. К числу сильных тушителей относятся кислород и ионы парамагнитных металлов (включая ионы железа).
Светорассеивание в мутных образцах также влияет на величинуJф. Влияние это разнонаправленное, и зависит от схемы регистрации флуоресценции и типа светорассеивания. Чаще всего, однако, регистрируемая величинаJфв мутных объектах оказывается заниженной.
