
- •Часть 3 . Металлургия цветных металлов
- •3.1. Исторические вехи развития производства цветных металлов на Украине
- •Металлургия титана
- •3.2.1.Физико-химические свойства и области применения
- •Высокая коррозионная стойкость, низкая плотность и теплопроводность, высокая прочность обуславливает его широкое применение в аэрокосмической, химической и судостроительной отраслях промышленности.
- •Сырьевые источники титана
- •Восстановительная плавка ильменитовых концентратов.
- •Магниетермическое получение титана из тетрахлорида титана
- •3.2.5.1. Восстановление четыреххлористого титана магнием
- •3.2.6. Переработка титановой губки в товарную продукцию
- •3.2.7. Плавка титана и его сплавов
- •3.3. Производство меди
- •3.3.1. Свойства меди и области потребления
- •3.3.2 Медные руды и схема их переработки
- •3.3.3. Получение медных штейнов из концентратов
- •3.3.4. Переработка медного штейна
- •3.3.5. Рафинирование меди
- •3.3.5.1. Огневое рафинирование
- •3.3.5.2. Электролитическое рафинирование меди
- •3.3.6. Медные сплавы
- •3.4. Металлургия алюминия
- •3.4.1. Общие сведения об алюминии
- •3.4.2. Сырье для получения алюминия
- •3.4.3. Производство глинозема
- •3.4.3.1. Получение глинозема по способу Байера
- •3.4.3.2. Получение глинозема способом спекания.
- •3.4.3.3. Электролитическое производство алюминия
- •3.5. Металлургия магния
- •3.5.1 Общие сведения о магнии
- •3.5.2. Сырьевые источники магния
- •3.5.3. Общие принципы производства магния
- •3.5.4. Получение безводного хлорида магния
- •3.5.5.Электролитический способ получения магния
- •3.6. Предприятия цветной металлургии Украины
- •3.6.1. Горно- обогатительные предприятия
- •3.6.1.2. Вольногорский горно-металлургический комбинат
- •(Убрать правую часnь)
- •3.6.2. Металлургические предприятия
- •3.6.2.1. Производство алюминия
- •3.6.2.1 Запорожский алюминиевый комбинат (г.Запорожье)
- •3.6.2.3. Вторичный алюминий и сплавы
- •3.6. 2.4. Производство титана и магния
- •3.6.2.4.1.«Запорожский титано - магниевый комбинат» (г. Запорожье).
- •3.6.2. 2. Производство пигментного диоксида титана
- •3. 6.2.3. Производство циркония и гафния
- •3.6.4.4. «Донецкая химико- металлургическая фабрика» (п.Г.Т. Донское, Волновахский район, Донецкая область)
- •2.2.6. Производство меди , никеля, цинка, свинец
- •3. Производство цветных металлов
3.4.3.3. Электролитическое производство алюминия
Получить алюминий из водного раствора, как это, например, делается для меди и некоторых других металлов, методом электролиза невозможно, ввиду того что алюминий имеет более отрицательный потенциал выделения, чем водород.
Алюминий получают путем электролитического разложения глинозема, растворенного в расплавленном электролите (криолите – Na3AlF6 ).
Расплавленный криолит диссоциирует по следующей схеме:
Na3AlF6 ↔ 3 Na+ + AlF3-6
Глинозем, растворенный в расплавленном криолите, диссоциирует на алюминий и кислородсодержащие ионы. Диссоциацию глинозема можно представить в виде следующей схемы:
Al2 O3 ↔ 2 Al 3+ + 3 O2-
Если через расплавленный электролит пропустить постоянный ток, то на различных полюсах электроподводящих электродов будет происходит: выделение алюминия - на отрицательном электроде (катоде), кислорода – на положительном электроде (аноде).
На катоде в первую очередь разряжаются ионы А13 +, так как в электролите нет других более электроположительных ионов (а ионы натрия имеют более отрицательный потенциал).
Процесс электролиза проводят в электролизере, рис. 11.
Электролизер состоит из стального корпуса, футерованного внутри угольными блоками 9 , в подовую часть которого с помощью шин 7 и токоподводящих стержней подведен отрицательный полюс источника тока.
Для того чтобы защитить токоподводящие стержни от разрушения на подину укладывают угольные блоки 9.
Над корпусом подвешены угольные аноды 3, к которым с помощью шин 2 подведен положительный полюс. Если в электролизер залить расплав 10, состоящий из криолита и глинозема, опустить в этот расплав аноды и пропускать через расплав постоянный ток большой силы и необходимого напряжения, то через определенное время на дне электролизера можно обнаружить расплавленный алюминий 8 под слоем расплавленного электролита 10, состоящего из криолита Na 3AIF6, в котором при температуре, близкой к 1000 °С, обычно растворено 1-10 % глинозема.
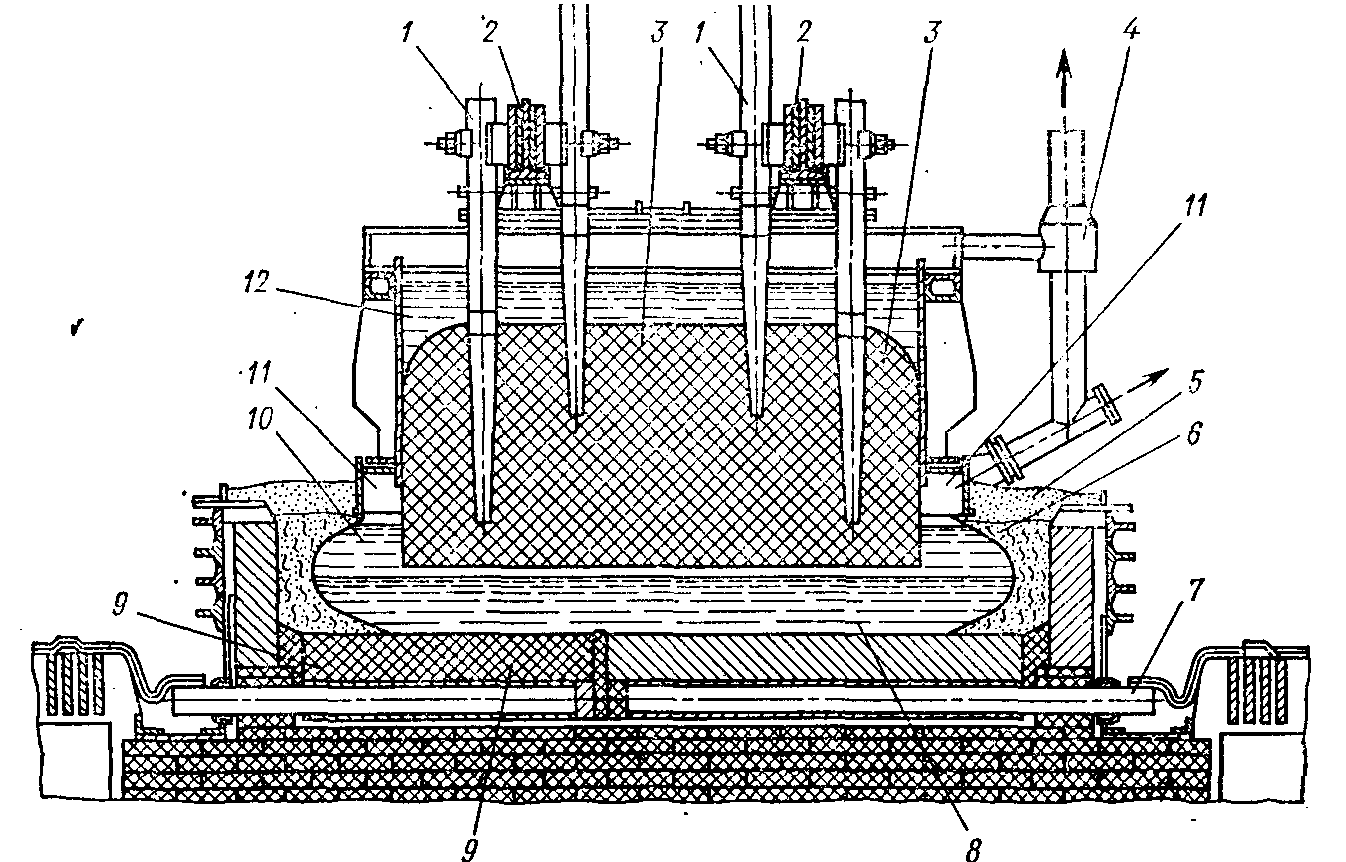
Рис. 11. Схема алюминиевого электролизера с верхним подводом тока к самообжигающемуся аноду:
1 - токоподводящие стержни; 2 - анодные шины; 3 - анодный угольный блок; 4 - газоотсосная система; 5 - слой глинозема;6 - гарнисаж; 7 - катодные шины; 8 - жидкий алюминий у катода; 9 - угольный катод; 10 - жидкий электролит; 11 - чугунный сборник анодных газов; 12 - твердожидкая анодная масса
Процесс электролиза сводится к разряду ионов Al3 + + О2 -, из которых состоит непрерывно расходуемый глинозем. Криолит не подвергается непосредственному электролизу и расходуется мало.
В результате чего на дне ванны образуется слой металлического алюминия 8. На аноде 3 преимущественно разряжаются ионы кислорода, который немедленно окисляет угольный анод, образуя СО и СО2.
Для того чтобы не происходило разрушение боковых графитовых блоков футеровки производят наращивание гарниссажа 6 из застывшего электролита и глинозема.
Электролит поддерживается в расплавленном состоянии только за счет теплоты, выделяющейся при прохождении через него электрического тока, поэтому часть электролита всегда настывает на холодных стенках и образует твердую застывшую корку, на которую сверху насыпают порошкообразную окись алюминия 5.
Алюминий извлекают из электролизера, пробивая корку электролита и опуская на дно футерованную огнеупором стальную трубку, через которую алюминий откачивают в вакуумный ковш.
По мере извлечения алюминия постепенно опускают анод и тщательно регулируют напряжение и межполюсное расстояние электролизера. Поскольку нижняя часть анода сгорает и он постепенно опускается, его необходимо наращивать в верхней части. В кожух анода систематически загружают анодную массу, которая постепенно коксуется на горячем конусе анода за счет теплоты, выделяющейся из ванны. Токоподводящие стальные штыри постепенно опускаются с анодом и во избежание их расплавления и загрязнения алюминия железом в очередной последовательности они выдергиваются из тела анода и поднимаются на более высокий уровень, а в образовавшуюся полость затекает анодная масса и затем коксуется.
