
- •Тестовые задания по курсу коллоидной химии
- •В. Н. Матвеенко
- •Назаров в.В.
- •Оглавление
- •Введение
- •1. Предмет коллоидной химии
- •Основы термодинамики поверхностных явлений
- •Общая характеристика поверхностной энергии
- •Поверхностная энергия и поверхностное натяжение
- •Полная поверхностная энергия
- •Адсорбция и поверхностное натяжение
- •Адсорбция, основные определения
- •Метод избыточных величин и адсорбционное уравнение Гиббса
- •Адгезия, смачивание и растекание жидкостей
- •Работа адгезии и когезии, уравнение Дюпре
- •Краевой угол, уравнения Юнга и Дюпре-Юнга
- •Дисперсность и термодинамические свойства тел
- •Влияние дисперсности на внутреннее давление
- •Капиллярные явления. Уравнение Жюрена
- •Влияние дисперсности на термодинамическую реакционную способность
- •Энергетика диспергирования и конденсации
- •Адсорбция газов и паров на поверхности твёрдых тел
- •Межмолекулярные взаимодействия при адсорбции
- •Адсорбция на однородной поверхности
- •Закон Генри, уравнение Ленгмюра
- •Теория полимолекулярной адсорбции бэт
- •Адсорбция на пористых материалах
- •Теория капиллярной конденсации
- •Теория объёмного заполнения микропор Дубинина
- •4. Адсорбция из растворов
- •Адсорбция поверхностно-активных веществ (пав)
- •Адсорбционные пленки, их характеристики
- •Ионообменная адсорбция
- •Кинетические и оптические свойства дисперсных систем
- •Седиментация и седиментационный анализ
- •Седиментация в гравитационном и центробежном полях
- •Седиментационный анализ
- •Броуновское движение, закон Эйнштейна-Смолуховского
- •Седиментационно-диффузионное равновесие
- •Оптические свойства дисперсных систем
- •6. Электрические явления на поверхностях
- •Образование и строение двойного электрического слоя (дэс)
- •Влияние электролитов на дэс. Перезарядка поверхности
- •Формулы дэс (строение мицелл)
- •Электрокинетические явления
- •Агрегативная устойчивость и коагуляция дисперсных систем
- •Седиментационная и агрегативная устойчивость
- •Лиофильные дисперсные системы
- •Классификация и общая характеристика пав
- •Мицеллообразование в растворах пав. Солюбилизация
- •Критическая концентрация мицеллообразования (ккм)
- •Лиофобные дисперсные системы
- •Факторы устойчивости лиофобных систем
- •Теория устойчивости и коагуляции лиофобных дисперсных си- стем (теория длфо)
- •Быстрая коагуляция. Уравнение Смолуховского
- •Электролитная коагуляция
- •Структурно-механические свойства дисперсных систем
- •Механизм структурообразования в дисперсных системах
- •Моделирование реологических свойств
- •Классификация дисперсных систем по реологическим свойствам
- •Реологические свойства агрегативно-устойчивых и структуриро- ванных систем
- •Предмет коллоидной химии
- •Основы термодинамики поверхностных явлений
- •Общая характеристика поверхностной энергии
- •Поверхностная энергия и поверхностное натяжение
- •Полная поверхностная энергия
- •Адсорбция и поверхностное натяжение
- •Адсорбция, основные определения
- •Метод избыточных величин и адсорбционное уравнение Гиббса
- •Адгезия, смачивание и растекание жидкостей
- •Работа адгезии и когезии, уравнение Дюпре
- •Краевой угол, уравнения Юнга и Дюпре-Юнга
- •Дисперсность и термодинамические свойства тел
- •Влияние дисперсности на внутреннее давление
- •Капиллярные явления. Уравнение Жюрена
- •Влияние дисперсности на термодинамическую реакционную спо- собность
- •Энергетика диспергирования и конденсации
- •Адсорбция газов и паров на поверхности твердых тел
- •Межмолекулярные взаимодействия при адсорбции
- •Адсорбция на однородной поверхности
- •Закон Генри, уравнение Ленгмюра
- •Теория полимолекулярной адсорбции бэт
- •Адсорбция на пористых материалах
- •Теория капиллярной конденсации
- •Теория объёмного заполнения микропор Дубинина
- •Адсорбция из растворов
- •Адсорбция поверхностно-активных веществ (пав)
- •Адсорбционные пленки, их характеристики
- •Ионообменная адсорбция
- •Кинетические и оптические свойства дисперсных систем
- •Седиментация и седиментационный анализ
- •Седиментация в гравитационном и центробежном полях
- •Седиментационный анализ
- •Броуновское движение, закон Эйнштейна-Смолуховского
- •Седиментационно-диффузионное равновесие
- •Оптические свойства дисперсных систем
- •Электрические явления на поверхностях
- •Образование и строение двойного электрического слоя (дэс)
- •Влияние электролитов на дэс. Перезарядка поверхности
- •Формулы дэс (строение мицелл)
- •Электрокинетические явления
- •Агрегативная устойчивость и коагуляция дисперсных систем
- •Седиментационная и агрегативная устойчивость
- •Лиофильные дисперсные системы
- •Классификация и общая характеристика пав
- •Мицеллообразование в растворах пав. Солюбилизация
- •Критическая концентрация мицеллообразования (ккм)
- •Лиофобные дисперсные системы
- •Факторы устойчивости лиофобных систем
- •Теория устойчивости и коагуляции лиофобных дисперсных си- стем (теория длфо)
- •Быстрая коагуляция. Уравнение Смолуховского
- •Электролитная коагуляция
- •Структурно-механические свойства дисперсных систем
- •Механизм структурообразования в дисперсных системах
- •Моделирование реологических свойств
- •Классификация дисперсных систем по реологическим свойствам
- •Реологические свойства агрегативно-устойчивых и структуриро- ванных систем
- •Учебное издание
- •Назаров Виктор Васильевич Жилина Ольга Викторовна Гродский Александр Сергеевич
- •Тестовые задания
- •По курсу коллоидной химии
- •125047 Москва, Миусская пл., 9
Критическая концентрация мицеллообразования (ккм)
На величину ККМ не влияет: А) температура;
Б) давление;
В) длина углеводородного радикала молекулы ПАВ; Г) тип полярной группы молекулы ПАВ;
Д) концентрация электролита в растворе.
Значение ККМ ионных ПАВ в водных растворах повышается при: А) повышении температуры;
Б) увеличении длины углеводородного радикала молекулы ПАВ; В) уменьшении длины углеводородного радикала молекулы ПАВ; Г) увеличении концентрации электролита в растворе;
Д) уменьшении концентрации электролита в растворе.
Значение ККМ в неполярных растворителях повышается при:
А) увеличении длины углеводородного радикала в молекуле ПАВ; Б) уменьшении длины углеводородного радикала в молекуле ПАВ; В) увеличении давления;
Г) уменьшении давления.
Значение ККМ ионных ПАВ в водных растворах уменьшается при: А) повышении температуры;
Б) понижении температуры;
В) увеличении длины углеводородного радикала в молекуле ПАВ; Г) уменьшении длины углеводородного радикала в молекуле ПАВ; Д) увеличении концентрации электролита в растворе;
Е) уменьшении концентрации электролита в растворе.
Значение ККМ коллоидных ПАВ в неполярных растворителях уменьша- ется при:
А) уменьшении длины углеводородного радикала в молекуле
ПАВ;
Б) увеличении длины углеводородного радикала в молекуле ПАВ; В) понижении давления;
Г) повышении давления.
При увеличении длины углеводородного радикала молекулы ПАВ зна- чение ККМ в водной среде:
А) возрастает; Б) снижается; В) не меняется;
При уменьшении длины углеводородного радикала молекулы ПАВ зна- чение ККМ в неполярных растворителях:
А) возрастает; Б) снижается; В) не меняется.
При увеличении концентрации электролита значение ККМ ионных ПАВ в водных растворах:
А) возрастает; Б) снижается; В) не меняется.
При уменьшении концентрации электролита значение ККМ неионных ПАВ в водных растворах:
А) возрастает; Б) снижается; В) меняется незначительно.
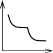
Установите соответствие между рисунком и зависимостью различных физико-химических параметров раствора от концентрации ПАВ:
А) x
Б) x
В) x


 cПАВ
cПАВ
сПАВ
сПАВ
зависимость поверхностного натяжения раствора коллоидного ПАВ от концентрации; Б
зависимость удельной электропроводности раствора коллоидного ПАВ от концентрации; А
зависимость эквивалентной электропроводности раствора колло- идного ПАВ от концентрации. В
Установите соответствие между формулой для расчёта стандартной
свободной энергии мицеллообразования
G0
и случаем её применимости:
М
А) G0 1 m RT ln ККМ ; Б) G0

2RT ln ККМ ;
М n М
М
В) G0 RT ln ККМ ,где m – число ионных пар в составе мицеллы, n – число агрегации.
для раствора неионного ПАВ. В
для раствора ионного ПАВ при неполной диссоциации. А
для раствора ионного ПАВ при полной ассоциации ионов в ми- целле. Б
Установите соответствие между формулой для расчёта стандартной
М
свободной энтальпии мицеллообразования сти:H 0
и случаем её применимо-
d ln ККМ ЛH 0
 А)
– M
; Б)
А)
– M
; Б)
d ln ККМ ЛH 0
– M ;
dT RT 2
d ln ККМ ЛH 0
В) – M ,
dT 2RT 2
dT 1+ m RT 2
n
где m – число ионных пар в составе мицеллы, n – число агрегации.
для раствора ионного ПАВ при неполной диссоциации. В
для раствора неионного ПАВ. А
для раствора ионного ПАВ при полной ассоциации ионов в ми-
целле. Б
