
- •Тестовые задания по курсу коллоидной химии
- •В. Н. Матвеенко
- •Назаров в.В.
- •Оглавление
- •Введение
- •1. Предмет коллоидной химии
- •Основы термодинамики поверхностных явлений
- •Общая характеристика поверхностной энергии
- •Поверхностная энергия и поверхностное натяжение
- •Полная поверхностная энергия
- •Адсорбция и поверхностное натяжение
- •Адсорбция, основные определения
- •Метод избыточных величин и адсорбционное уравнение Гиббса
- •Адгезия, смачивание и растекание жидкостей
- •Работа адгезии и когезии, уравнение Дюпре
- •Краевой угол, уравнения Юнга и Дюпре-Юнга
- •Дисперсность и термодинамические свойства тел
- •Влияние дисперсности на внутреннее давление
- •Капиллярные явления. Уравнение Жюрена
- •Влияние дисперсности на термодинамическую реакционную способность
- •Энергетика диспергирования и конденсации
- •Адсорбция газов и паров на поверхности твёрдых тел
- •Межмолекулярные взаимодействия при адсорбции
- •Адсорбция на однородной поверхности
- •Закон Генри, уравнение Ленгмюра
- •Теория полимолекулярной адсорбции бэт
- •Адсорбция на пористых материалах
- •Теория капиллярной конденсации
- •Теория объёмного заполнения микропор Дубинина
- •4. Адсорбция из растворов
- •Адсорбция поверхностно-активных веществ (пав)
- •Адсорбционные пленки, их характеристики
- •Ионообменная адсорбция
- •Кинетические и оптические свойства дисперсных систем
- •Седиментация и седиментационный анализ
- •Седиментация в гравитационном и центробежном полях
- •Седиментационный анализ
- •Броуновское движение, закон Эйнштейна-Смолуховского
- •Седиментационно-диффузионное равновесие
- •Оптические свойства дисперсных систем
- •6. Электрические явления на поверхностях
- •Образование и строение двойного электрического слоя (дэс)
- •Влияние электролитов на дэс. Перезарядка поверхности
- •Формулы дэс (строение мицелл)
- •Электрокинетические явления
- •Агрегативная устойчивость и коагуляция дисперсных систем
- •Седиментационная и агрегативная устойчивость
- •Лиофильные дисперсные системы
- •Классификация и общая характеристика пав
- •Мицеллообразование в растворах пав. Солюбилизация
- •Критическая концентрация мицеллообразования (ккм)
- •Лиофобные дисперсные системы
- •Факторы устойчивости лиофобных систем
- •Теория устойчивости и коагуляции лиофобных дисперсных си- стем (теория длфо)
- •Быстрая коагуляция. Уравнение Смолуховского
- •Электролитная коагуляция
- •Структурно-механические свойства дисперсных систем
- •Механизм структурообразования в дисперсных системах
- •Моделирование реологических свойств
- •Классификация дисперсных систем по реологическим свойствам
- •Реологические свойства агрегативно-устойчивых и структуриро- ванных систем
- •Предмет коллоидной химии
- •Основы термодинамики поверхностных явлений
- •Общая характеристика поверхностной энергии
- •Поверхностная энергия и поверхностное натяжение
- •Полная поверхностная энергия
- •Адсорбция и поверхностное натяжение
- •Адсорбция, основные определения
- •Метод избыточных величин и адсорбционное уравнение Гиббса
- •Адгезия, смачивание и растекание жидкостей
- •Работа адгезии и когезии, уравнение Дюпре
- •Краевой угол, уравнения Юнга и Дюпре-Юнга
- •Дисперсность и термодинамические свойства тел
- •Влияние дисперсности на внутреннее давление
- •Капиллярные явления. Уравнение Жюрена
- •Влияние дисперсности на термодинамическую реакционную спо- собность
- •Энергетика диспергирования и конденсации
- •Адсорбция газов и паров на поверхности твердых тел
- •Межмолекулярные взаимодействия при адсорбции
- •Адсорбция на однородной поверхности
- •Закон Генри, уравнение Ленгмюра
- •Теория полимолекулярной адсорбции бэт
- •Адсорбция на пористых материалах
- •Теория капиллярной конденсации
- •Теория объёмного заполнения микропор Дубинина
- •Адсорбция из растворов
- •Адсорбция поверхностно-активных веществ (пав)
- •Адсорбционные пленки, их характеристики
- •Ионообменная адсорбция
- •Кинетические и оптические свойства дисперсных систем
- •Седиментация и седиментационный анализ
- •Седиментация в гравитационном и центробежном полях
- •Седиментационный анализ
- •Броуновское движение, закон Эйнштейна-Смолуховского
- •Седиментационно-диффузионное равновесие
- •Оптические свойства дисперсных систем
- •Электрические явления на поверхностях
- •Образование и строение двойного электрического слоя (дэс)
- •Влияние электролитов на дэс. Перезарядка поверхности
- •Формулы дэс (строение мицелл)
- •Электрокинетические явления
- •Агрегативная устойчивость и коагуляция дисперсных систем
- •Седиментационная и агрегативная устойчивость
- •Лиофильные дисперсные системы
- •Классификация и общая характеристика пав
- •Мицеллообразование в растворах пав. Солюбилизация
- •Критическая концентрация мицеллообразования (ккм)
- •Лиофобные дисперсные системы
- •Факторы устойчивости лиофобных систем
- •Теория устойчивости и коагуляции лиофобных дисперсных си- стем (теория длфо)
- •Быстрая коагуляция. Уравнение Смолуховского
- •Электролитная коагуляция
- •Структурно-механические свойства дисперсных систем
- •Механизм структурообразования в дисперсных системах
- •Моделирование реологических свойств
- •Классификация дисперсных систем по реологическим свойствам
- •Реологические свойства агрегативно-устойчивых и структуриро- ванных систем
- •Учебное издание
- •Назаров Виктор Васильевич Жилина Ольга Викторовна Гродский Александр Сергеевич
- •Тестовые задания
- •По курсу коллоидной химии
- •125047 Москва, Миусская пл., 9
Адсорбция на однородной поверхности
Закон Генри, уравнение Ленгмюра
В соответствии с законом Генри начальный участок изотермы адсорб- ции (при малых концентрациях или давлениях) должен быть:
А) выпуклым по отношению к оси абсцисс; Б) вогнутым по отношению к оси абсцисс; В) линейным.
Закон Генри соблюдается:
А) при высокой концентрации (давлении паров) адсорбата; Б) при низкой концентрации (давлении паров) адсорбата; В) в средней части изотермы адсорбции.
Уравнение Ленгмюра используется в случае:
А) нелокализованной адсорбции на энергетически однородной по- верхности;
Б) локализованной адсорбции на энергетически неоднородной по- верхности;
В) локализованной адсорбции на энергетически однородной по- верхности;
Г) капиллярной конденсации.
Уравнение Ленгмюра может быть использовано при адсорбции на: А) микропористых адсорбентах;
Б) адсорбентах с переходными порами в области высоких давле- ний паров;
В) макропористых адсорбентах.
Константа К, входящая в уравнение Ленгмюра
ляет собой константу:
А) скорости адсорбции;
Б) адсорбционного равновесия; В) конденсации.
А А Kp , представ-
1 KpВыберите правильное соотношение между константами уравнений Ленгмюра (А, К) и Генри (KГ):
А) АК = KГ; Б) А = KГ; В) К
К KГ
= А; Г) KГ
К
= А
Уравнение Ленгмюра в области низких концентраций принимает вид:
А) А = Кс; Б) А = Ас; В) = АКс; Г) = Кс; Д) 0 Kc ,
1 Kc
где А – адсорбция; А – максимальная адсорбция; – степень заполнения поверхности адсорбента; K – константа адсорбционного равновесия; с – равновесная концентрация адсорбата.
Выберите рисунок, на котором правильно показан общий вид изотермы адсорбции Ленгмюра:
А) А
1
 Б) A
Б) A
В) А

 р 1 р
р 1 р
p
Г) p A
Д) А
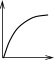
 р p
р p
ps
(А – адсорбция; р – равновесное давление пара; ps – давление насыщенного пара адсорбата).
Выберите рисунок, на котором правильно показана изотерма адсорбции
в координатах линейной формы уравнения Ленгмюра:
А) А
1

 Б) A
Б) A
В) c A
с 1

 c
c
Г) A
c
с с
(А – адсорбция; А – максимальная адсорбция; K – константа адсорбцион- ного равновесия; – угол наклона прямой; с – равновесная концентрация адсорбата).
На приведённой изотерме адсорбции уравнением Генри описывается участок
 А
А
p ps
А) 1; Б) 2; В) 3.
На приведённой изотерме адсорбции уравнением Ленгмюра описыва- ются участки:
 А
А
p ps
А) 1; Б) 1 и 2; В) 3; Г) 1, 2 и 3.
Теория полимолекулярной адсорбции бэт
В теории БЭТ, в отличие от теории Ленгмюра, предполагается, что: А) адсорбционные центры энергетически неоднородны;
Б) на каждом адсорбционном центре адсорбируется только одна молекула;
В) каждая адсорбированная молекула является новым центром ад- сорбции;
Г) адсорбированные молекулы, находящиеся в соседних слоях ад- сорбата, не взаимодействуют друг с другом.
Параметр с, входящий в уравнение БЭТ
А
AC p
ps
p
,
p
1 p 1 (C 1) p
представляет собой:
s
s
А) ёмкость двойного электрического слоя адсорбента;
Б) равновесную концентрацию адсорбата в объёме фазы, из кото- рой произошла адсорбция;
В) теплоёмкость адсорбента; Г) константу равновесия.
При выводе уравнения БЭТ принимается, что: А) все слои адсорбата равноценны;
Б) все слои адсорбата равноценны, за исключением первого слоя; В) число слоёв адсорбата не является бесконечным;
Г) отсутствует взаимодействие между разными слоями адсорбата.
При определении удельной поверхности адсорбентов с использованием уравнения БЭТ в качестве адсорбатов используются азот и инертные газы, потому что:
А) эти адсорбаты обладают повышенной адсорбционной способ-
ностью;
Б) у этих адсорбатов слабые межмолекулярные взаимодействия; В) эти адсорбаты обладают высокой теплотой адсорбции.
Как правило, уравнение БЭТ не соблюдается в области низких давлений
паров адсорбата (при p
ps
� 0,05), потому что в этих условиях:
сти;
А) полимолекулярная адсорбция не происходит;
Б) степень заполнения поверхности является недостаточной;
В) сильно проявляется энергетическая неоднородность поверхно-
Г) велика ошибка в определении величины адсорбции.
Как правило, уравнение БЭТ плохо соблюдается в области относитель-
ных давлений паров p
ps
0,3, потому что в этих условиях:
А) начинают проявляться межмолекулярные взаимодействия меж- ду соседними адсорбированными молекулами одного и того же слоя ад-
сорбата;
Б) образуется слишком много слоёв адсорбата; В) адсорбция становится нелокализованной;
Г) велика ошибка в определении величины адсорбции.
Выберите рисунок, на котором правильно показан общий вид изотермы полимолекулярной адсорбции (БЭТ):
А) А
Б) lnА
В) А


 p ln
p p
p ln
p p
ps ps ps

 Д) А
Д) А
Г)
p
ps ps
(А – адсорбция; р – равновесное давление пара адсорбата; ps – давление насыщенного пара адсорбата).
Выберите рисунок, на котором правильно показана изотерма адсорбции, представленная в координатах линейной формы уравнения БЭТ:
А) А
Б) p A
 tg=
1
tg=
1
Ас
p p
В) s
с

 tg=
tg=
с 1 Ас
Г) p A
p ps
 tg=
tg=
с 1
p
A1
Ас
p
s
p p
ps ps
(А – адсорбция; с – равновесная концентрация адсорбата; р – равновесное давление пара; ps – давление насыщенного пара; А и с – константы урав- нения БЭТ)
Взаимосвязь между константой К уравнения Ленгмюра и константой с
уравнения БЭТ выражается соотношением:
А) Кс = рs; Б) Крs = с; В) с
К
= рs; Г) К = срs,
где рs – давление насыщенного пара над жидким адсорбатом.
