
Структура и свойства аминокислот, пептидов, белков
Нейтральной аминокислотой является:
1) аргинин 2) лизин 3) валин 4) гистидин
Положительно заряженной аминокислотой является:
1) аргинин 2) глутаминовая кислота 3) валин 4) аспарагин
Отрицательно заряженной аминокислотой является:
1) лизин 2) аспарагиновая кислота 3) аланин 4) гистидин
Нейтральной аминокислотой является:
1) аспартат 2) глутамин 3) аргинин 4) гистидин
Положительно заряженной аминокислотой является:
1) глутамат 2) аспарагинова кислота 3) валин 4) аргинин
Отрицательно заряженной аминокислотой является:
1) лизин 2) глутамин 3) аланин 4) аспартат
На рисунке представлен радикал аминокислоты. Определите, к какой группе аминокислот она относится:

1) гидрофобные 2) полярные незаряженные 3) заряженные положительно 4) заряженные отрицательно
На рисунке представлен радикал аминокислоты. Определите, к какой группе аминокислот она относится:
![]()
1) гидрофобные 2) полярные незаряженные 3) заряженные положительно 4) заряженные отрицательно
На рисунке представлен радикал аминокислоты. Определите, к какой группе аминокислот она относится:

1) гидрофобные 2) полярные незаряженные 3) заряженные положительно 4) заряженные отрицательно
На рисунке представлен радикал аминокислоты. Определите, к какой группе аминокислот она относится:
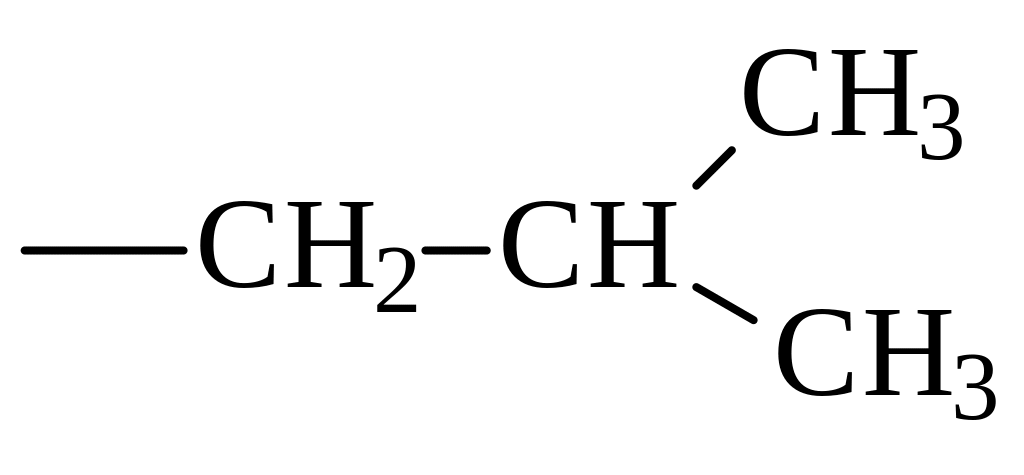
1) гидрофобные 2) полярные незаряженные 3) заряженные положительно 4) заряженные отрицательно
Н
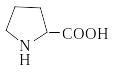 а
рисунке представлена аминокислота.
Определите, к какой группе аминокислот
она относится:
а
рисунке представлена аминокислота.
Определите, к какой группе аминокислот
она относится:
1) гидрофобные 2) полярные незаряженные 3) заряженные положительно 4) заряженные отрицательно
Аминокислоты, входящие в состав белков, являются:
1) жирными кислотами 2) a-аминокислотами 3) g-аминокислотами
4) ненасыщенными карбоновыми кислотами
Оптической активностью не обладает аминокислота:
1) лейцин 2) цистеин 3) глицин 4) триптофан
Биполярный ион моноаминомонокарбоновой кислоты заряжен:
отрицательно 2)положительно 3)электронейтрален
Изоэлектрическую точку при рН 9,74 имеет:
1) аспарагиновая кислота 2) аланин 3) лизин 4) глицин
Каков суммарный заряд лизина при рН 11?
Каков суммарный заряд глутаминовой кислоты при рН 10?
Каков суммарный заряд глутаминовой кислоты при рН 2?
Выберите аминокислоту, R-группа которой при физиологических условиях рН несет положительный заряд:
а) Валин б) Аспарагиновая кислота в)Глутамин г)Цистеин д)Аргинин
Какая аминокислота имеет серусодержащую группу нейтральную при всех значениях рН?
а) цистеин б) метионин в) глутамин г) фенилаланин д) серин
Какая аминокислота образует дисульфидные поперечные связи между участками полипептидной цепи?
а) цистеин б) метионин в) глутамин г) фенилаланин д) серин
Единственная аминокислота, содержащая замещенную a-аминогруппу. Эта аминокислота влияет на процесс свертывания белков, так как служит местом вынужденного изгиба полипептидной цепи.
а) Гистидин б) Лизин в) Пролин г) Глутамин д) Валин
Выберите аминокислоту с полярной небольшой R-группой, содержащей гидроксильную группу. Эта аминокислота играет важную роль в функционировании некоторых ферментов:
а) Гистидин б) Лизин в) Серин г) Глутамин д) Валин
Укажите аминокислоту с боковой R-группой, которая создает наименьшие стерические ограничения.
а) Валин б) Глицин в)Глутамин г)Цистеин д)Аргинин
Выберите ту аминокислоту, которая имеет полярную, но незаряженную R-группу. Если эту группу подвергнуть гидролизу, то аминокислота превращается в другую аминокислоту с отрицательно заряженной R-группой при рН 7:
а) Лизин б)Аспарагин в) Цистеин г)Фенилаланин д)Серин
Рассчитайте возможное число изомеров треонина:
а) 4 б) 2 в) 6 г) 8
Рассчитайте возможное число изомеров изолейцина:
а) 4 б) 2 в) 6 г) 8
Выберите структуру пептидной связи:
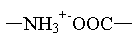
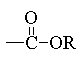 1.
1.2.
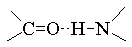
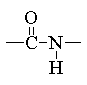 3.
3.4.
Пептидную связь содержит:
1.
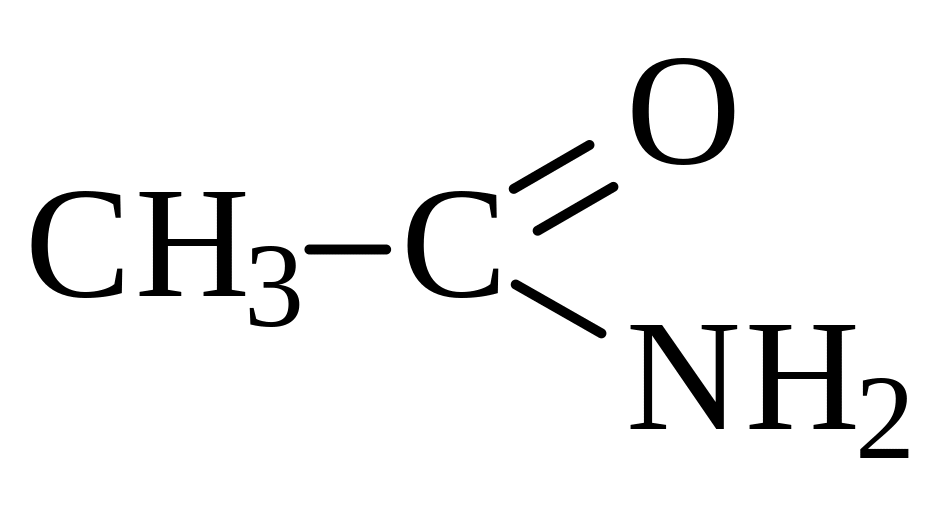
2.

3.

4.

Из приведенных ниже аминокислот выберите ту, радикалы которой могут участвовать в образовании водородных связей в качестве донора водорода при рН 7.
а) Глутаминовая кислота б) Аспарагин в) Глицин г) Валин д) Метионин
Из приведенных ниже аминокислот выберите ту, радикалы которой могут участвовать в образовании водородных связей в качестве донора водорода при рН 7.
а) Серин б) Лейцин в) Аспарагиновая кислота г) Фенилаланин
Выберите те типы связей, которые стабилизируют третичную структуру полипептидной цепи:
Водородная связь между пептидными группами
Связь между a-амино- и a-карбоксильными группами аминокислот
Водородные связи между радикалами аминокислот
Гидрофобные взаимодействия радикалов аминокислот
Ковалентные связи между радикалами цистеина
Электростатическое притяжение между противоположено заряженными боковыми группами аминокислот
Выберите тип связей, стабилизирующий вторичную структуру полипептидной цепи:
Водородная связь между пептидными группами
Связь между a-амино- и a-карбоксильными группами аминокислот
Водородные связи между радикалами аминокислот
Гидрофобные взаимодействия радикалов аминокислот
Ковалентные связи между радикалами цистеина
Электростатическое притяжение между противоположено заряженными боковыми группами аминокислот
Выберите тип связей, стабилизирующий первичную структуру полипептидной цепи:
Водородная связь между пептидными группами
Связь между a-амино- и a-карбоксильными группами аминокислот
Водородные связи между радикалами аминокислот
Гидрофобные взаимодействия радикалов аминокислот
Ковалентные связи между радикалами цистеина
Электростатическое притяжение между противоположено заряженными боковыми группами аминокислот
Укажите аминокислоты, которые вероятнее всего расположена на поверхности молекулы белка
а) Аспарагиновая кислота б) Фенилаланин в) Лизин г) Аланин
Укажите аминокислоты, которые вероятнее всего расположена внутри глобулы белка
а) Глутаминовая кислота б) Изолейцин в) Аргинин г) Валин
Что понимают под изменением конформации белков?
Изменение аминокислотной последовательности полипептидной цепи
Изменение вторичной и третичной структур
Замену одной простетической группы в белке на другую
Разрыв пептидных связей в белке
Первичная структура белка –
пространственная структура, образованная связями, возникающими между атомами боковых заместителей аминокислотных остатков;
порядок чередования аминокислот, соединенных пептидными связями;
пространственная структура, образованная слабыми взаимодействиями между контактными поверхностями протомеров;
пространственная структура, образованная водородными связями, возникающими между атомами пептидного остова.
Вторичная структура белка –
пространственная структура, образованная связями, возникающими между атомами боковых заместителей аминокислотных остатков;
порядок чередования аминокислот, соединенных пептидными связями;
пространственная структура, образованная слабыми взаимодействиями между контактными поверхностями протомеров;
пространственная структура, образованная водородными связями, возникающими между атомами пептидного остова.
Третичная структура белка –
пространственная структура, образованная связями, возникающими между атомами боковых заместителей аминокислотных остатков;
порядок чередования аминокислот, соединенных пептидными связями;
пространственная структура, образованная слабыми взаимодействиями между контактными поверхностями протомеров;
пространственная структура, образованная водородными связями, возникающими между атомами пептидного остова.
Четвертичная структура белка –
пространственная структура, образованная связями, возникающими между атомами боковых заместителей аминокислотных остатков;
порядок чередования аминокислот, соединенных пептидными связями;
пространственная структура, образованная слабыми взаимодействиями между контактными поверхностями протомеров;
пространственная структура, образованная водородными связями, возникающими между атомами пептидного остова.
Н
 а
рисунках представлены схемы активного
центра белка и возможных лигандов.
а
рисунках представлены схемы активного
центра белка и возможных лигандов.
Определите, какой лиганд комплементарен активному центру данного белка:
-
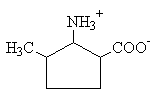
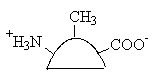 1.
1.2.
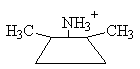
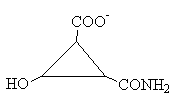 3.
3.4.
Выберите правильные ответы. Комплементарностью молекул обусловлены взаимодействия:
белка с лигандом;
протомеров в олигомерном белке;
белка с диполями воды в растворе;
радикалов аминокислот при формировании третичной структуры белка.
Выберите правильные ответы. Лигандом для белка может быть:
ион металла;
простетическая группа;
другой белок;
молекула воды;
целая клетка.
Выберите один неправильный ответ. Активный центр белка:
расположен в углублении белковой молекулы;
сформирован радикалами аминокислот, удаленных в первичной структуре белка;
занимает большую часть молекулы белка;
способен комплементарно взаимодействовать со специфическими лигандами.
Выберите один неправильный ответ. В результате денатурации белков:
уменьшается их растворимость;
разрушается нативная конформация;
увеличивается доступность белка для действия протеолитических ферментов;
происходит гидролиз пептидных связей.
Какие из перечисленных факторов могут вызывать денатурацию белка.
Увеличение температуры
Взаимодействие белков с субстратами
Взаимодействие белков с кофакторами
Изменение рН
Действие солей тяжелых металлов
Н
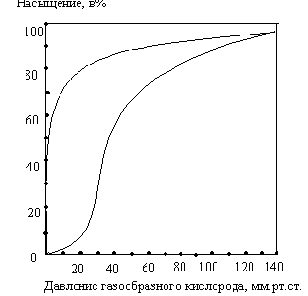 а
рисунке представлены кривые насыщения
кислородом гемоглобина и миоглобина.
Выберите причину такой разной зависимости
насыщения этих белков.
а
рисунке представлены кривые насыщения
кислородом гемоглобина и миоглобина.
Выберите причину такой разной зависимости
насыщения этих белков.
Разные простетические группы в составе белков
Разные уровни пространственной организации белков
Различный аминокислотный состав гемоглобина и миоглобина
Какова функция миоглобина в организме?
Транспорт кислорода от легких к тканям
Компонент буферной системы крови
Резервный источник кислорода в мышцах
Компонент соединительной ткани
В состав белков пищи, которую скармливали животным, входили аминокислоты, перечисленные ниже. Выберите среди них незаменимые:
а ) Треонин б) Серин в) Глицин г) Аланин д) Фенилаланин
В состав белков пищи, которую скармливали животным, входили аминокислоты, перечисленные ниже. Выберите среди них незаменимые:
а ) Лизин б) Глутамин в) Лейцин г) Цистеин д) Пролин
В состав белков пищи, которую скармливали животным, входили аминокислоты, перечисленные ниже. Выберите среди них частично заменимую:
а) Серин б) Глицин в) Гистидин г) Валин д) Лейцин
В состав белков пищи, которую скармливали животным, входили аминокислоты, перечисленные ниже. Выберите среди них частично заменимую:
а) Аргинин б) Глутамат в) Аспарагин г) Изолейцин д) Лизин
В состав белков пищи, которую скармливали животным, входили аминокислоты, перечисленные ниже. Выберите среди них заменимые:
а) Серин б) Аспартат в) Триптофан г) Гистидин д) Валин
В состав белков пищи, которую скармливали животным, входили аминокислоты, перечисленные ниже. Выберите среди них условно заменимую:
а) Глицин б) Серин в) Тирозин г) Фенилаланин д) Лизин
Наиболее специфичным методом выделения белков является:
гель-фильтрация;
высаливание;
ультрацентрифугирование;
ионная хроматоргафия;
аффинная хроматография.
Подобрать к каждому пронумерованному методу разделения и очистки белков соответствующие различия в свойствах белков, обозначенные буквой:
1. Ультрацентрифугирование А. Различия по растворимости
2. Электрофорез В. Различия по величине заряда
суммарного заряда
3. Гель-фильтрация
4. Ионообменная хроматография С.Различия по молекулярной массе
5. Солевое фракционирование
. Подобрать каждому пронумерованному названию уровня структурной организации белка соответствующее понятие, обозначенное буквой:
1. Первичная структура 2. Вторичная структура 3. Третичная структура 4. Четвертичная структура |
А. Пространственное взаиморасположение -спиралей, -структур, обусловленное образование связей между радикалами аминокислот. |
В. Порядок чередования аминоксилот в полипептидной цели. |
|
С. Объединение в определенном порядке двух или большего количества протомеров в молекулу олигомерного белка. |
|
Д. Способ укладки пептидной цепи в виде -спиралей, -структур. |
|
Е. Конформация полипептидной цепи, в образовании которой участвуют эфирные связи. |
Какому уровню структурной организации белка соответствует каждый пронумерованный тип связи? Подобрать пары.
1. Связь между карбоксильными и аминогруппами радикалов аминокислот. |
А. Первичная структура |
2. Связь между -амино и -карбоксильными группами аминокислот. |
В. Вторичная группа |
3. Связь между радикалами цистеина. |
С. Третичная группа |
4. Водородные связи между атомами пептидного остова |
|
5. Водородные связи между радикалами аминокислот. |
|
6. Межрадикальные гидрофобные взаимодействия. |
|
Подобрать к каждому белку соответствующую функцию, основываясь на классификации белков по функциям.
1. Коллаген А. Структурная
2. Иммуноглобулим В. Сократительная
3. Инсулин С. Транспортная
4. Гемоглобин Д. Каталитическая
5. Актин Е.Защитная
6. Кератин F. Рецепторная
7. Трансферрин G. Регуляторная
8. Мозин
9. Церулоплазмин
10. Каталаза
11. Альбумин
