
Методы воздействия на скорость распространения фронта реагирования в самораспространяющемся высокотемпературном синтезе – новом направлении химико-технологических процессов (90
..pdfконверсии исходных реагентов в конечные продукты меньше
единицы.
Скорость распространения волны горения первого рода для классического газового пламени приближенно можно охарактеризовать масштабной величиной, характеризующей скорость тепловыделения в волне горения и скорость передачи тепла:
U2 @ |
2 × λ × R ×T 2 |
× r × exp (- |
E |
) |
(3) |
|
ρ × Q × E |
0 |
R0 ×Tад |
|
|
|
|
|
|||
В таких волнах горения ширина зоны реакции много меньше ширины зоны прогрева и по протяженности и по интервалу температуры. Скорость горения связана с максимальной термодинамически равновесной адиабатической температурой горения. Такая теория горения называется равновесной.
Для процессов, которые характеризуются широкими зонами реакции, а скорость горения определяется не максимальной температурой, а некоторой промежуточной Тг , которая меньше
Тад . Для таких процессов характерно немонотонное изменение
температуры прогретого слоя (изломы, плато). Структура волны горения сложная, многозонная.
Скорость горения систем рассматривается в рамках неравновесной теории распространения пламени.
Реализация экзотермического взаимодействия в конденсированной системе с конденсированными конечными и промежуточными продуктами часто называют безгазовым горением. Наряду с горением газовых систем горение конденсированных систем с конденсированными продуктами относится к предельным разновидностям горения.
Если рассматривать скорость горения как интегральную макроскопическую характеристику, то для зоны тепловыделения толщиной δ и тепловым эффектом Q при теплоемкости материальной среды С простейшее выражение закона сохранения
энергии имеет вид: |
|
Q = C ( Тад - Т0 ) |
(4) |
11

Тепловыделение в единицу времени в единице объема зоны горения при средней скорости химической реакции φ будет равно С·( Тад - Т0 )·φ·δ. Выделившееся тепло расходуется на прогрев
исходной смеси от Ò 0 до |
Ò |
|
àä посредством теплопроводности с |
|||||||
соответствующим коэффициентом λ, то есть: |
|
|
||||||||
λ |
dT |
= |
|
λ(Тад - Т |
0 ) |
(5) |
||||
dx |
|
δ |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||
следовательно: |
|
|
|
|
|
|
|
|
|
|
С(Тад - Т |
0 )× ϕ × δ @ |
λ(Тад - Т |
0 ) |
|||||||
|
|
|
|
(6) |
||||||
|
|
δ |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
Если все выделившееся в зоне реакции тепло расходуется на прогрев исходной смеси, то толщина прогретого слоя будет:
δ = |
λ |
(7) |
|
ñ× ϕ |
|||
|
|
Для конденсированных систем с конденсированными продуктами реакции расход исходной смеси равен (U × ρ ), который
в зоне реакции перерабатывается в продукты со скоростью δ ×ϕ . Следовательно, U × ρ = δ ×ϕ . Значение макроскопической скорости горения будет:
U = |
1 |
ϕδ = |
1 |
ϕλ |
|
|
ρ |
ρ |
c |
(8) |
|||
|
|
Скорость горения для выбранной простой модели пропорциональна корню квадратному из произведения скорости реакции на отношение коэффициента теплопроводности к теплоемкости и обратно пропорциональна плотности исходной
12
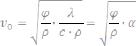
смеси. Если плотность ввести под знак корня, то можно получить другую зависимость:
(9)
где α – коэффициент температуропроводности.
При известных скорости горения и теплофизических характеристиках смеси можно оценить толщину прогретого слоя.
Для смеси |
титана |
с |
сажей скорость горения U=10мм/с, |
теплоемкость |
смеси |
с=1 |
кДж/(кг·С), плотность ρ 0 = 2 ×103 кг/м3 , |
λ=3Вт/(м·К). Толщина прогретого слоя будет примерно равна 0,15 мм.
δ |
а |
(10) |
|
U |
|||
|
|
1.4 Влияние управляющих факторов на скорость горения в СВС
В литературе подробно описано влияние различных параметров системы на скорость горения U. Обобщены данные по изменению U от соотношения компонентов в исходной смеси (α), концентрации инертной добавки в шихте (ơ), размеров частиц реагентов (r), относительной плотности ( ) и начальной температуры (То) гетерогенной среды, давления газа окружающей среды (Р), диаметра образца (d) [4]. На рисунках 2 – 9 приведены некоторые конкретные примеры.
1.4.1 Влияние качества перемешивания
Учитывая гетерогенность реакционных систем СВС, понятно и действие условий их приготовления. Степень гомогенизации и качество контакта реагирующих частиц обуславливают скорость массообмена, уровень тепловыделения, скорость химической реакции в волне горения.
13
В аппаратах одного типа качество смешения зависит от многих факторов, и в том числе от времени перемешивания. Кроме того, на качество перемешивания по уровню гомогенности получаемой смеси влияют условия смешения. Например, в вакууме (остаточное давление 1 – 10 мм рт ст) состав смесей Ti+C и Ti+B достигает одинаковой степени распределения углерода и бора в сравнении с перемешиванием в нормальных условиях (воздух и атмосферное давление) в 6 – 8 раз быстрее.
Длительное перемешивание в энергонапряженных аппаратах приводит к образованию на поверхности частиц продукта. Это при инициировании экзотермической реакции приводит к снижению скорости и температуры реагирования. Скорость реагирования снижается также за счет изменения поверхности и морфологии частиц титана. Поверхность частиц уменьшается, частицы становятся более компактными.
1.4.2 Зависимость скорости горения от давления
Скорость горения U практически не изменяется с ростом давления инертного газа (см. рис. 2). На первых этапах исследований в области СВС, когда проводились сравнения с горением взрывчатых ве- ществ и твердых ракетных топлив, этому обстоятельству придавалось большое значение как характерному признаку СВС. Позже детальные исследования показали, что постоянство скорости горения в безгазовых СВС-системах при варьировании давления инертного газа в окружающей среде строго выполняется для образцов с большой относительной плотностью ( > 0,7). Для высокопористых гетерогенных сред вклад механизма переноса тепла через газовую фазу может быть значительным, и при этом скорость горения зависит от природы и плотности газа.
В ряде металлотермических процессов горение при атмосферном давлении сопровождается сильным разбросом реагирующего расплава, а иногда протекает в виде взрыва. Сопутствующие газы образуют пузырьки или газовые прослойки. Они и выбрасывают реакционную смесь.
14
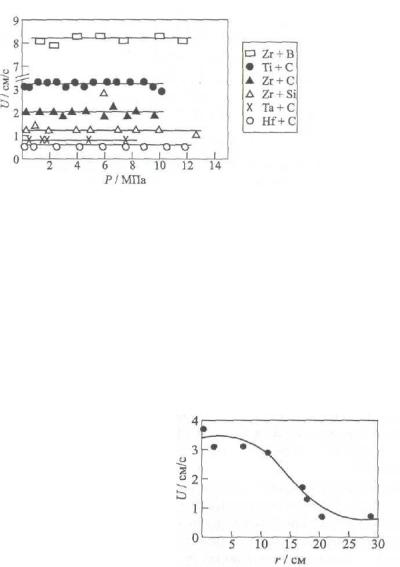
Рис. 2 . Зависимость скорости горения (U) от давления инертного газа (аргона) окружающей среды (Р) для разных систем
1.4.3 Зависимость скорости горения от дисперсности реагентов
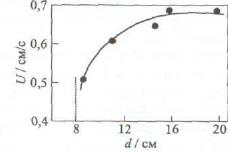
Зависимость скорости горения U от дисперсности реагентов (см. рис.3) является типичной для гетерогенных систем — крупные частицы требуют большего времени для реагирования, поэтому функция U(r) является убывающей, хотя ее вид может быть различным. В средней части кривой обычно U ~ r для малых и крупных частиц имеют место отклонения от этого закона.
Рис. 3. Зависимость скороcти горения (U) от размера частиц Ti (г)
в системе Ti + С
15
1.4.4 Зависимость скорости горения от диаметра образца
Характерна зависимость скорости горения U от диаметра образца d. Традиционно считается, что при d ниже некоторого критического значения образцы не горят. При дальнейшем увеличении диаметра скорость горения возрастает с тенденцией к насыщению. Действительно, увеличение d ведет к увеличению отношения объемного количества выделившегося тепла (~ d3) к теплопотерям через поверхность (~ d2). Можно представить, что существуют два критических диаметра: минимальный — при d < dmin реакция в самораспространяющемся режиме невозможна — и максимальный — при d > > dmax достигнуты адиабатические условия и параметры горения слабо зависят от теплопотерь. Следовательно, вид зависимости U(d), показанный на рис. 4, отражает тепловую природу горения и роль теплопотерь.
Рис. 4. Зависимость скорости горения (U) от диаметра образ-ца (d) в
системе Hf + С Эксперименты с
закалкой фронта горения в
клину показывают, что значение dmin для некоторых систем может быть очень малым (300-500 мкм), иногда сравнимым с размером нескольких частиц исходных реагентов.
1.4.5 Зависимость скорости горения от плотности |
|
сформованного элемента |
|
Часто зависимость U от плотности образца |
имеет |
максимум (см. рис.5). В литературе нет однозначной трактовки этого эффекта. Максимум объясняется действием двух конкурирующих процессов. С одной стороны, увеличение плотности среды способствует улучшению межчастичных контактов, что ведет к ускорению химической реакции и увеличению скорости распространения волны горения. С дру- гой стороны, соответствующее возрастание теплопроводности среды с ростом плотности увеличивает отвод тепла из зоны горения в холодную часть образца, тем самым замедляя процесс
16
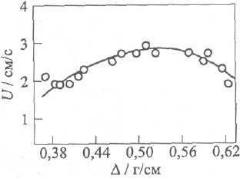
горения. Теоретическая модель, в которой использовались экспериментальные зависимости изменения теплопроводности от плотности среды, дает монотонное увеличение скорости горения во всем диапазоне изменения плотности .
Рис. 5. Зависимость скорости горения от плотности образца в системе Hf + С
Предложена другая гипотеза для систем с одним плавящимся компонентом (например, Ti+С, Ti+В), в которых предполагается, что капиллярное растекание расплава по пористой твердой среде лимитирует процесс горения. В этом случае существует критическое значение пористости среды (объем пор равен объему растекающейся жидкости), ниже которого (большие плотности) скорость процесса горения замедляется.
Наконец, еще одно объяснение наличия максимума на зави- симости U( ) связано с наличием газифицирующихся примесей в порошках с достаточно большой удельной поверхностью. На рис.6 представлены экспериментальные данные по изменению скорости горения в системе Ni-Al в зависимости от плотности исходной среды для различных смесей порошков реагентов.
17
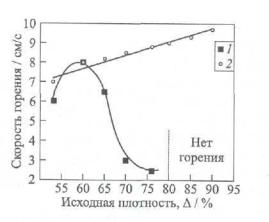
Рис. 6. Зависимость скорости горения в системе Ni-Al от исходной плотности реакционной среды:
1-без предварительной обработки; 2-с дегазированием, Т=570К, Р=13Па
Видно, что для предварительно не обработанных образцов (кривая 1) зависимость имеет характерный максимум. В то же время для дегазированных порошков (кривая 2) скорость горе- ния в среднем выше и меняется монотонно с увеличением плотности. Аналогичные данные были получены и для других систем. На основе этих результатов можно заключить, что при относительно малых плотностях реакционной среды ( < 0,6) газ, десорбирующийся в волне горения, беспрепятственно (не нарушая ее целостности) покидает реакционную среду, имеющую высокую фильтрационную проницаемость. Поэтому в этом диапазоне плотностей скорость горения возрастает с ростом плотности как результат увеличения эффективной теплопроводности среды. В малопористых образцах ( > 0,6) с малой проницаемостью десорбция газа ведет к локальному увеличению газового давления во фронте волны, что в свою очередь приводит к разрушению микроструктуры среды — образованию микротрещин. Микротрещины понижают эффективную теплопроводность, и, как результат, средняя скорость горения падает.
18
Высокоскоростная микровидеосъемка распространения процесса в образцах с высокой исходной плотностью показала, что причиной наблюдаемых макроосцилляций является пери- одическое образование микротрещин перед фронтом волны горения.
1.4.6 Зависимость скорости горения от соотношения компонентов
При стехиометрическом соотношении реагентов, соответствующем адиабатической температуре горения в системе, наблюдается максимум на зависимости U от α (рис. 7), то есть величина скорости горения однозначно определяется тепловыделением в зоне реакции.
Увеличение начальное температуры То приводит к общему росту температуры горения и увеличению скорости химической реакции. Типичная зависимость скорости горения от То (рис. 8) возрастающая функция. В отличие от изменения То введение в систему СВС инертного разбавителя снижает тепловыделение в зоне реакции. Скорость химического взаимодействия снижается вслед за температурой горения. Скорость горения убывает (рис.9).
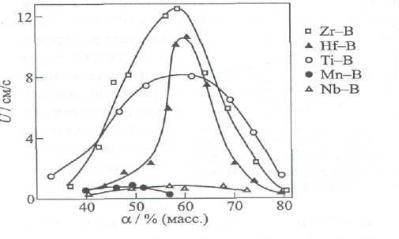
Рис. 7. Зависимости скорости горения U
от соотношения компонентов α в системе Me + αB
19
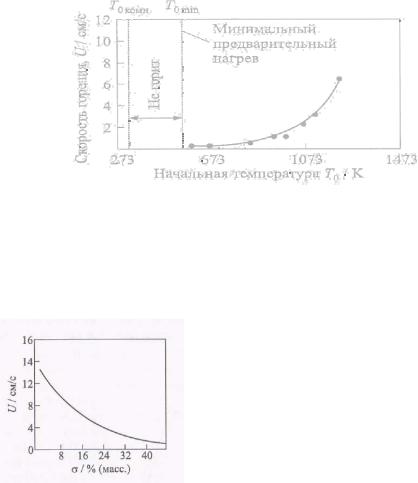
Рис. 8. Зависимость скорости горения U от начальной температуры То в системе Ti + Ni
Рис. 9. Зависимость скорости горения U от разбавления конечным продуктом а в системе Ni+Al
(Т=300К)
1.4.7 Влияние массовых сил на горение гетерогенных систем с конденсированными продуктами
Эффект влияния массовых сил на горение конденсированных систем основан на действии перегрузок на процессы, протекающие
20
