
Методические указания к решению задач по курсу общей физики. Раздел «Термодинамика» (96
.pdf
|
|
|
R(T1 −T2 )ln |
pmax |
|
|
(T1 −T2 )ln |
Vmax |
|
|
||||||
η= |
A |
= |
p |
= |
V |
|||||||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
min |
|
|
|
|
min |
|||||||
|
|
|
|
|
|
|
|
|
|
. |
||||||
Q |
RT1 ln |
pmax |
+Cp |
(T1 −T2 ) |
|
V |
γ(T −T ) |
|||||||||
|
нагр |
|
|
T ln |
max |
+ |
1 2 |
|
||||||||
|
pmin |
|||||||||||||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
1 |
V |
|
γ −1 |
||||||
|
|
|
|
|
|
|
|
|
|
min |
|
|
|
|
||
Подставляя числовые значения, находим
η= 16 .
3.2. Воду массой m = 20 г нагревают с t1 = 20 DC до t2 =100 DC , а затем выпаривают при t2 =100 DC . Определите изменение энтропии воды S в этом процессе, если ее плотность ρ=103 кг/м3,
удельная теплоемкость c = 4,2 кгкДжK , удельная теплота парообра-
зования r = 2,3 МДжкг . Процесс считайте равновесным и проте-
кающим при нормальном атмосферном давлении. Парообразованием при t <t2 =100 DC пренебречь.
Решение. Описанный в условии задачи процесс может быть разделен на два этапа – нагревание без парообразования от
t = 20 DC до t |
2 |
=100 DC , |
в ходе которого изменение энтропии со- |
|||||
1 |
|
|
|
|
|
|
|
|
ставляет |
|
|
|
|
|
|
|
|
|
|
T2 |
δQ |
T2 |
cmdT |
|
T |
|
|
|
S ' = ∫ |
T |
= ∫ |
|
= cmln |
2 |
, |
|
|
T |
T |
|||||
|
|
T |
|
T |
|
|
1 |
|
|
|
1 |
|
1 |
|
|
|
|
и изотермическое испарение воды, в ходе которого изменение энтропии системы составляет
m rdm |
|
rm |
|
|
|
|
|
|
|||
S '' = ∫ |
|
= |
|
|
. |
|
|
|
|
|
|
T |
T |
|
|
|
|
|
|
||||
0 |
2 |
|
2 |
|
|
|
|
|
|
|
|
Полное изменение энтропии воды |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
T |
|
r |
|
|
|||
S = S '+ S '' = m cln |
2 |
+ |
|
|
. |
||||||
T1 |
|
|
|||||||||
|
|
|
|
|
T2 |
||||||
Подставляя числовые значения, получим |
|
S =1, 28 103 |
Дж |
. |
|||||||
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
K |
|
31

3.3. Идеальный газ с показателем адиабаты γ совершает по-
литропный процесс. При каком значении показателя политропы энтропия системы уменьшается при равновесном увеличении ее температуры?
Решение. Элементарное изменение энтропии в равновесном процессе
dS = δTQ = CνTdT ,
откуда
dTdS = CTν .
Энтропия газа оказывается убывающей функцией температуры, если
dS |
= |
Cν |
< 0 . |
(3.21) |
|
dT |
T |
||||
|
|
|
Теплоемкость C системы в политропном процессе определена выражением (2.15)
n = C −Cp , C −CV
откуда с учетом формулы Майера (2.13) получим
C = |
n −γ |
C = |
(n −γ) R |
|
. |
(3.22) |
|
(n −1)(γ − |
1) |
||||
|
n −1 V |
|
|
|||
Подставляя (3.22) в (3.21), получим, что dTdS < 0 при условии nn−−1γ < 0. Таким образом, энтропия в политропном процессе явля-
ется убывающей функцией температуры, если n (1; γ) .
3.4. Изобразите обратимый цикл Карно для произвольной термодинамической системы на диаграмме T–S. Пользуясь этой диаграммой (рис. 3), определите КПД цикла, зная, что максимальная температура рабочего тела Tmax =T1 , минимальная температура
Tmin =T2 .
32
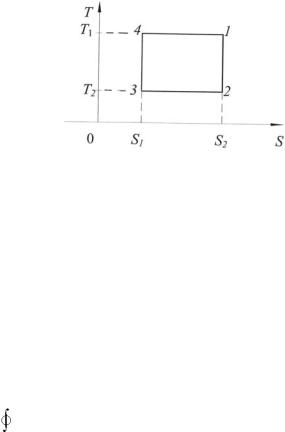
Рис. 3
Решение. В обратимом адиабатном процессе энтропия рабочего тела остается постоянной: S = const, поэтому цикл Карно на диаграмме T–S имеет вид, не зависящий от природы рабочего тела и устройства тепловой машины.
Имея в виду, что в равновесном процессе δQ =TdS, для теплоты, полученной рабочим телом от нагревателя, имеем
S2
Qнагр = ∫ δQ = ∫ T1dS =T1 (S2 − S1 ).
4→1 S1
Работа, совершенная рабочим телом за цикл, в соответствии с первым началом термодинамики (2.3)
|
|
S |
S |
A = δQ =Q12 +Q23 +Q34 +Q41 = ∫ δQ + ∫ δQ = ∫2 |
T1dS + ∫1 T2 dS. |
||
4→1 |
2→3 |
S1 |
S2 |
Окончательно получим
A =(T1 −T2 )(S2 − S1 ) .
Термический КПД цикла
η= |
A |
= |
T1 −T2 |
. |
Q |
|
|||
|
|
T |
||
|
нагр |
1 |
|
|
3.5. Покажите, что КПД любого обратимого цикла, совершаемого в интервале температур от Tmax =T1 до Tmin =T2 меньше КПД
обратимого цикла Карно, осуществляемого в том же интервале температур.
33
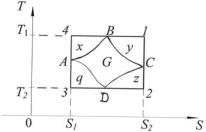
Решение. Рассмотрим графическое представление произвольного циклического процесса ABCD на диаграмме T–S (рис. 4). Теплота
Q = ∫TdS ,
сообщенная рабочему телу в любом процессе, может быть определена графически как некоторая площадь на диаграмме T–S. Теплота, полученная рабочим телом от нагревателя в циклическом процессе ABCD, может быть таким образом определена как площадь под кривой ABC:
Qнагр = T1 (S2 − S1 ) − x − y ,
где x и y – площади криволинейных треугольников A4B и B1C соответственно. Теплота, отданная рабочим телом холодильнику, может быть определена как площадь под кривой CDA.
Рис. 4
Таким образом, суммарное количество теплоты, полученное системой в круговом процессе, может быть определено как площадь G фигуры ABCD на диаграмме T–S. В соответствии с первым началом термодинамики для кругового процесса
A =  δQ =(T1 −T2 )(S2 − S1 ) − x − y − z −q ,
δQ =(T1 −T2 )(S2 − S1 ) − x − y − z −q ,
где z и q – площади криволинейных треугольников C2D и D3A. Термический КПД цикла ABCD
η= |
A |
= |
|
|
|
|
Q |
|
|
|
|||
|
|
|
|
|
|
|
|
|
нагр |
|
|
|
(3.23) |
= |
(T1 −T2 )(S2 − S1 ) − x − y − z −q |
< |
(T1 −T2 )(S2 − S1 ) − x − y |
|||
|
|
T1 (S2 − S1 ) − x − y |
T1 (S2 − S1 ) − x − y |
. |
||
34

Заметим, что для любых положительных a, b и c |
|
|
|
|||||||||
|
|
|
|
a |
< |
a +c |
. |
(3.24) |
||||
|
|
|
|
|
|
|||||||
|
|
|
|
b |
b +c |
|
|
|
|
|||
Тогда из (3.23) и (3.24) следует |
|
|
|
|
|
|
||||||
|
A |
(T1 −T2 )(S2 − S1 ) − x − y |
|
|
(T1 −T2 )(S2 − S1 ) |
|
T2 |
|
||||
η= |
|
< |
T1 (S2 − S1 ) − x − y |
|
< |
T1 (S2 − S1 ) |
<1− |
|
, |
|||
Qнагр |
|
T1 |
||||||||||
что и требовалось доказать.
Задачи для самостоятельного решения
3.6. Идеальная тепловая машина, работающая по циклу Карно, получает за каждый цикл от нагревателя 1,2 кДж. Температура нагревателя 400 K, температура холодильника 300 K. Определите работу, совершаемую тепловой машиной за один цикл, и количество теплоты, отдаваемое холодильнику за один цикл.
Ответ: A =300 Дж, Qхол =900 Дж.
3.7. Найдите КПД тепловой машины, работающей с ν моль идеального газа по циклу, состоящему из адиабатного расширения 1–2, изотермического сжатия 2–3 и изохорического процесса 3–1. Работа, совершенная над газом в изотермическом процессе, равна А. Разность максимальной и минимальной температур газа в цикле равна T. Показатель адиабаты газа равен γ .
Ответ: η=1 − (γ −1) A .
νR T
3.8. При изотермическом расширении идеальный газ совершил работу, равную A =1, 4 кДж. Определите изменение энтропии газа, если процесс протекал при температуре T = 350 K .
Ответ: S = 7 ДжK .
3.9. Определите изменение энтропии, происходящее при превращении m = 2 кг воды, находившейся при температуре
t1 = 20 DC , в лед с температурой t2 = −20 DC . Теплоемкость воды
считать равной c = 4, 2 |
кДж |
, теплоемкость льда |
c |
|
= 2,1 |
кДж |
. |
кг K |
2 |
|
|||||
1 |
|
|
|
кг K |
|||
|
|
|
|
|
|||
35
Температуру плавления льда принять равной t0 = 0 DC . Удельная
теплота плавления льда λ = 0,33 |
|
МДж |
. |
|
|
|
|
|||||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
кг |
|
|
|
|
|
|
|
|
T |
|
|
T |
λ |
|
кДж |
|
||||
Ответ: |
S = −m c1 ln |
1 |
+c2 ln |
|
0 |
+ |
|
|
|
= −3,33 |
|
. |
T0 |
|
|
|
K |
||||||||
|
|
|
|
T2 |
T0 |
|
|
|||||
3.10.Углекислый газ массой m = 220 г переводят из состояния
сдавлением p1 = 0, 2 МПа и температурой t1 = 27 DC в состояние с
давлением p2 =1,6 МПа при температуре t2 =327 DC . Определи-
те приращение его энтропии, считая газ идеальным, а его молекулы – жесткими.
Ответ: |
S = |
mR i + 2 |
ln |
T |
−ln |
p |
2 |
|
= 28,8 |
Дж |
. |
|||
|
|
|
2 |
|
|
|
||||||||
μ |
2 |
T1 |
p1 |
K |
||||||||||
|
|
|
|
|
|
|
|
|||||||
36
СПИСОК ЛИТЕРАТУРЫ
1.Глаголев К.В., Морозов А.Н. Физическая термодинамика: Учеб. пособие. М.: Изд-во МГТУ им. Н.Э. Баумана, 2004. 272 с.
2.Иродов И.Е. Задачи по общей физике: Учеб. пособие. М.:
БИНОМ, 1998. 448 с.
3.Иродов И.Е. Задачи по общей физике: Учеб. пособие. М.:
Высш. шк., 1991. 175 с.
4.Базаров И.П. Термодинамика: Учеб. для вузов. 4-е изд., перераб. и доп. М.: Высш. шк., 1991. 376 с.
37
ОГЛАВЛЕНИЕ |
|
I. Основные положения термодинамики. Уравнения |
|
состояния............................................................................................. |
3 |
II. Первое начало термодинамики. Теплота и работа................ |
15 |
III. Круговые процессы. Второе начало термодинамики.......... |
24 |
Список литературы ........................................................................... |
37 |
38
