
2 курс / Биохимия / Книжки и сборники / Словарь БХ_2018 (шифр)
.pdf11
изменения, которые будут наиболее оптимальными для образования фермент-
субстратного комплекса.
ЛИАЗЫ (синтазы) – это класс ферментов, которые катализируют два типа биохимических реакций: 1) реакции разрыва связей С – С (углерод – углерод), С – О (углерод – кислород), С – N (углерод – азот), С – S (углерод – сера) без участия воды; 2) реакции присоединения определенных групп по месту двойных связей.
Примеры ферментов: декарбоксилазы, лиазы кетокислот, альдолазы, или альдегид-лиазы, гидратазы.
ЛИГАЗЫ (синтетазы) – это класс ферментов, которые катализируют синтез новых молекул из двух других с использованием энергии макроэргических соединений, чаще всего АТФ. Примеры ферментов: аминоацил-тРНК-синтетазы,
карбоксилазы.
МЕЖДУНАРОДНЫЕ ЕДИНИЦЫ АКТИВНОСТИ ФЕРМЕНТОВ
(сокращенно МЕ, размерность – мкмоль/мин) - это единицы активности ферментов, которые означают количество фермента, необходимое для превращения одного микромоля субстрата в продукт в течение минуты.
МУЛЬТИФЕРМЕНТНЫЕ КОМПЛЕКСЫ – это системы ферментов,
катализирующие в интактной клетке последовательные реакции, в которых продукт, полученный в первой реакции при участии первого фермента,
становится субстратом для последующего фермента и так далее. Например,
пируватдегидрогеназный мультиферментный комплекс, комплекс синтаза высших жирных кислот.
НОМЕНКЛАТУРА ФЕРМЕНТОВ – это классификация ферментов, в
основу которой положены типы биохимических реакций, катализируемых ферментами. Согласно номенклатуре все ферменты разделены на классы, классы
12
– на подклассы, подклассы – на подподклассы. Различают шесть классов ферментов: оксидоредуктазы, трансферазы, гидролазы, лиазы (синтазы),
изомеразы и синтетазы (лигазы).
ОКСИДОРЕДУКТАЗЫ – это класс ферментов, которые катализируют окислительно-восстановительные реакции. Примеры ферментов:
лактатдегидрогеназа, сукцинатдегидрогеназа, ксантиноксидаза, пероксидазы.
ПРОДУКТ (Р) – это вещество, получаемое в результате химической
реакции.
ПРОСТЕТИЧЕСКАЯ ГРУППА – это название кофактора в том случае,
когда кофактор прочно связан с белковой частью фермента, или апоферментом.
РЕТРОИНГИБИРОВАНИЕ – смотрите «Ингибирование по принципу
обратной связи».
СИНТАЗЫ – смотрите «Лиазы».
СИНТЕТАЗЫ – смотрите «Синтетазы».
СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ – это высокая избирательность действия ферментов как в отношении субстрата реакции, так и в отношении типа катализируемой реакции. Последняя лежит в основе номенклатуры, или
классификации, ферментов.
СПЕЦИФИЧНОСТЬ АБСОЛЮТНАЯ – это разновидность специфичности фермента по отношению к субстрату реакции, при которой один фермент действует только на один субстрат и катализирует только одну реакцию.
Например, аргиназа, уреаза.
13
СПЕЦИФИЧНОСТЬ ОТНОСИТЕЛЬНАЯ (специфичность групповая)
- это разновидность специфичности фермента по отношению к субстрату реакции,
при которой один фермент действует на ряд близкородственных субстратов и катализирует реакцию одного и того же типа. Например, пепсин, трипсин.
СТЕРЕОСПЕЦИФИЧНОСТЬ - это разновидность специфичности ферментов по отношению к субстрату реакции, при которой фермент действует только на один из оптических изомеров субстрата реакции. Если субстраты реакций относятся к D- или L-ряду оптических изомеров, то фермент действует только на один тип изомеров.
СУБСТРАТ (S) - вещество, с которым связывается фермент, или энзим (Е).
Субстрат связывается с активным центром фермента, что приводит к образованию фермент-субстратного комплекса (ES), в составе которого субстрат постепенно преобразуется в продукт реакции (Р).
ТЕОРИЯ ИНДУЦИРОВАННОЙ АДАПТАЦИИ (теория индуцированного соответствия) – смотрите «Кошланда теория».
ТЕРМОЛАБИЛЬНОСТЬ – это зависимость активности фермента или скорости ферментативной реакции от температуры. При высоких температурах падение активности фермента происходит вследствие денатурации ферментов,
которые по своей химической природе являются белками. При низких температурах снижается скорость броуновского движения молекул, что приводит к уменьшению вероятности столкновения частиц, необходимого для образования фермент-субстратного комплекса.
ТРАНСФЕРАЗЫ – это класс ферментов, которые катализируют перенос групп атомов от одного соединения (донора группы) к другому (акцептор
14
группы). Примеры ферментов: аминотрансферазы, метилтрансферазы,
гликозилтрансферазы.
УРАВНЕНИЕ МИХАЭЛИСА - МЕНТЕН (уравнение скорости
ферментативной реакции (v)) – это уравнение, которое показывает, что скорость ферментативной реакции численно равна отношению произведения максимальной скорости реакции и концентрации субстрата (vmax [S]) к сумме концентрации субстрата и константы Михаэлиса ([S] + KM):
v = (vmax [S])/([S] + KM)
ФЕРМЕНТЫ (энзимы, Е) - это биологические катализаторы белковой
природы.
ФИШЕРА ГИПОТЕЗА – это гипотеза, согласно которой для образования фермент-субстратного комплекса как начального этапа ферментативного катализа между ферментом и субстратом должно быть идеальное пространственное соответствие, подобное тому, которое имеется между ключом и замком.
ХОЛОФЕРМЕНТЫ – это ферменты, которые по своей химической природе являются сложными белками. Белковая часть холофермента называется апоферментом, небелковая – кофактором. В качестве кофакторов могут выступать ионы металлов либо органические низкомолекулярные соединения, которые чаще всего являются производными водорастворимых витаминов.
ЭНЕРГИЯ АКТИВАЦИИ – это энергия, которую надо сообщить молекулам, чтобы они стали реакционноспособными. Чем больше энергия активации, тем медленнее скорость реакции. Ферменты снижают энергию активации.
15
ЭНЗИМЫ – смотрите «Ферменты».
ЭФФЕКТОРЫ – это низкомолекулярные вещества, которые влияют на активность ферментов и скорость ферментативной реакции. Изостерические эффекторы действуют на активные центры, аллостерические – на аллостерические центры ферментов, активируя или угнетая их действие путем изменения конформации.
16
ГЛАВА 2. ВИТАМИНЫ
АВИТАМИНОЗ – это крайне выраженный дефицит витаминов, вызванный либо полным отсутствием витаминов в продуктах питания, либо нарушением их утилизации в организме при нормальном поступлении с пищей.
АНТИВИТАМИНЫ – это природные и синтетические соединения,
которые препятствуют биологическому эффекту витаминов. Существует две группы антивитаминов: 1) структурные аналоги естественных витаминов и 2)
вещества, не являющиеся структурными аналогами естественных витаминов.
Антивитамины первой группы конкурируют с витаминами за связывание с апоферментами - белковыми компонентами соответствующих ферментов. В
результате образуется неактивный фермент, и нарушается обмен веществ.
Например, изониазид – препарат, который используется для лечения туберкулеза,
является антивитамином витаминов РР и В6. Примерами антивитаминов второй группы являются ферменты тиаминаза и аскорбатоксидаза, инактивирующие тиамин и аскорбиновую кислоту, соответственно, а также сырой белок куриного яйца авидин – антивитамин витамина Н (биотина). Авидин образует комплексное соединение с витамином Н и тем самым препятствует его всасыванию.
АНТИМЕТАБОЛИТЫ – это вещества, которые по химической структуре близки к природным соединениям, участвующим в обмене веществ, или метаболизме (метаболитам). Поэтому антиметаболиты могут замещать естественные метаболиты в биохимических реакциях. Однако антиметаболиты не могут обеспечить нормальное протекание реакций, что обусловливает изменение обмена веществ.
17
АНТИОКСИДАНТЫ – это группа веществ, защищающих клеточные
мембраны от разрушения свободными радикалами и активными формами
кислорода.
АСКОРБИНОВАЯ КИСЛОТА (витамин С, антискорбутный витамин)
– это витамин, не имеющий коферментой формы. По химическому строению витамин С относится к производным углеводов. В организме человека аскорбиновая кислота не синтезируется. Она принимает участие в окислительно-
восстановительных реакциях в качестве донора атомов водорода, в том числе в реакциях гидроксилирования остатков пролина и лизина в коллагене
(посттрансляционная модификация). Кроме того, с участием аскорбиновой кислоты проходят реакции гидроксилирования, необходимые для образования тирозина из фенилаланина, гомогентизиновой кислоты из пара-
оксифенилпирувата, 5-окситриптофана из триптофана, а также для образования гормонов коры надпочечников и гидроксильных производных различных стероидов. Аскорбиновая кислота предохраняет адреналин от окисления. Данный витамин участвует в обмене железа: он способствует восстановлению трехвалентного железа в двухвалентное, которое легко усваивается в кишечнике и используется для синтеза гема. Аскорбиновая кислота является витамином-
антиоксидантом. Авитаминоз аскорбиновой кислоты – это заболевание скорбут,
или цинга. Патологические изменения при цинге связаны с дезорганизацией соединительной ткани. Заболевание характеризуется слабостью, апатией,
повышенной утомляемостью, повышенной восприимчивостью к инфекциям,
железодефицитной анемией, кровоточивостью и воспалением десен,
расшатыванием и выпадением зубов, точечными кровоизлияниями на коже
(петехиями), кровоизлияниями в мышцы и внутренние органы, а в тяжелых случаях – в кости.

18
БИОТИН (витамин Н, антисеборейный витамин) - это витамин, который может синтезироваться в организме человека кишечной микрофлорой. Биотин принимает участие в реакциях карбоксилирования и транскарбоксилирования.
Реакции карбоксилирования, или фиксации диоксида углерода, сопряжены с расходованием АТФ, ферменты – карбоксилазы. Реакции транскарбоксилирования, протекающие без использования АТФ, характеризуются тем, что карбоксилирование одного субстрата сопровождается одновременным декарбоксилированием другого вещества, ферменты – транскарбоксилазы. Биотин необходим для таких жизненно необходимых биохимических процессов как глюконеогенез, синтез высших жирных кислот, обмен лейцина. Проявления дефицита биотина характеризуются депрессией, галлюцинациями, мышечные болями, алопецией, себореей, дерматитом.
ВИТАМИН А – смотрите «Ретинол».
ВИТАМИН В1 – смотрите «Тиамин».
ВИТАМИН В2 – смотрите «Рибофлавин».
ВИТАМИН В3 – смотрите «Пантотеновая кислота».
ВИТАМИН В5 – смотрите «Ниацин».
19
ВИТАМИН В6 – смотрите «Пиридоксин».
ВИТАМИН В9 – смотрите «Фолиевая кислота».
ВИТАМИН В12 – смотрите «Кобаламин».
ВИТАМИН С – смотрите «Аскорбиновая кислота».
ВИТАМИН D – смотрите «Кальциферол».
ВИТАМИН Е – смотрите «Токоферол».
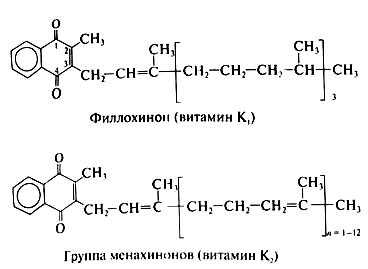
ВИТАМИН К (нафтохиноны, антигеморрагический витамин, витамин гемокоагуляции) – это витамин, который представляет собой две группы хинонов с боковыми изопреноидными цепями: витамин К1 (филлохинон) и
витамин К2 (менахинон), которые различаюся по количеству изопреновых групп в боковой цепи и происхождению. Витамин К1 впервые был выделен из люцерны, а
витамин К2 может синтезироваться бактериями. Буква «К» в названии витамина связана с тем, что он участвует в коагуляции, или свертывании, крови. Витамин К является коферментом γ-глутаматкарбоксилазы, которая катализирует гамма-
карбоксилирование глутамата II, VII, IX и X факторов свертывания крови в процессе посттрансляционной модификации. Благодаря данной реакции происходит связывание белков с катионами кальция и мембранами клеток.
При гиповитаминозе витамина К возникают самопроизвольные паренхиматозные и капиллярные кровотечения (носовые кровотечения,

20
внутренние кровоизлияния). Кроме того, любые поражения сосудов, в том числе и при хирургических операциях, могут привести к обильным кровотечениям. У
человека гиповитаминоз К встречается реже, чем другие авитаминозы, так как
смешанная пища содержит |
данный витамин в большом количестве. Кроме того, |
|
витамин К синтезируется |
кишечной микрофлорой. Недостаточность витамина К |
|
обычно развивается при |
нарушениях |
выведения желчи, что затрудняет |
всасывание витамина в кишечнике. У детей грудного возраста часто возникают обильные подкожные кровотечения и кровоизлияния. Они наблюдаются при геморрагической болезни новорожденных, которая может быть вызвана как низким содержанием витамина К в материнском молоке, так и недостаточно сформированной микрофлорой кишечника. Синтезирован водорастворимый аналог витамина К – викасол.
ВИТАМИН F - это линолевая, линоленовая и арахидоновая полиненасыщенные жирные кислоты:
Ненасыщенные жирные кислоты входят в состав сложных липидов,
поэтому они являются компонентами для синтеза клеточных мембран. Линолевая кислота является предшественником арахидоновой кислоты, которая используется для синтеза эйкозаноидов – гормонов локального типа действия.
Витамин F необходим для регенерации эпителиальных клеток кожи, он играет регуляторную роль в жизнедеятельности клеток. Недостаточность витамина
