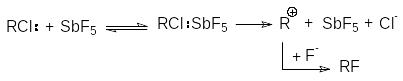Конкуренция реакций нуклеофильного замещения
П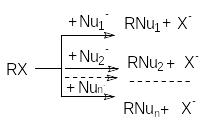 ри
проведении реакций нуклеофильного
замещения в реакционных смесях могут
присутствовать несколько нуклеофилов.
В этих случаях имеет место конкуренция
нескольких нуклеофильных реакций:
ри
проведении реакций нуклеофильного
замещения в реакционных смесях могут
присутствовать несколько нуклеофилов.
В этих случаях имеет место конкуренция
нескольких нуклеофильных реакций:
Из схемы конкуренции видно, что увеличение выхода любого из продуктов достигается увеличением избытка нуклеофила, ответственного за его образование. Так, при реализации щелочного гидролиза хлоралканов протекают следующие реакции
RCl + OH– ROH + Cl– (3)
ROH + OH– K;(( RO– + H2O (4)
RCl + RO– ROR + Cl– (5)
Можно видеть, что соотношение скоростей основной реакции (3) и побочной реакции образования простого эфира (5) определяется конкурентным взаимодействием
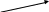 +OH-
ROH
+OH-
ROH
 RCl
RCl
+RO- ROR
и увеличение выхода
основного продукта, спирта, может быть
обеспечено увеличением избытка
гидроксил-аниона. Поскольку соотношение
![]() определяется в соответствие с равновесием
(4) равенством
определяется в соответствие с равновесием
(4) равенством
![]()
факторами увеличения выхода спирта являются увеличение избытка воды и снижение конверсии хлоралкана (что равносильно понижению концентрации спирта).
Некоторые нуклеофилы обладают двумя реакционными центрами и поэтому дают разные продукты замещения. При этом преимущественное образование продукта замещения по тому или иному реакционному центру определяется правилом Корнблюма: Если реакция протекает по SN2-механизму, то нуклеофил реагирует с субстратом своим более нуклеофильным (поляризуемым) центром. Если реакция протекает по SN1-механизму, то нуклеофил реагирует с субстратом своим более электроотрицательным основным центром. Примером ионов с двойственной реакционной способностью (амбидентных ионов) являются цианид-анион СN и нитрит-анион
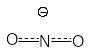
Эти анионы в зависимости от механизма реакции, определяемого условиями их проведения и структурой субстрата, могут давать следующие продукты
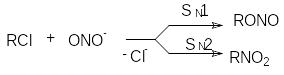
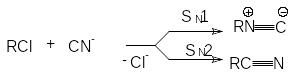
Подобная ситуация имеет место при обмене галогенов. Реакция SN2 всегда протекает в сторону замещения более электроотрицательного атома на более нуклеофильный (поляризуемый) (F и Cl на Br и J). Однако при SN1-замещении образуется продукт с более электроотрицательным заместителем (например, RF из RСl). Для изменения механизма используют соли или катализаторы с сильно электрофильным катионом (AgF, HgF2, SbF3, SbF5):