
Влияние строения реагентов на реакции нуклеофильного замещения Влияние структуры радикала r субстрата
У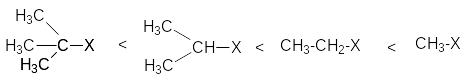 спех
реакции SN2
определяется эффективностью атаки
нуклеофила на положительно заряженный
реакционный центр субстрата. При этом,
чем выше этот положительный заряд, тем
эффективнее взаимодействие. Поэтому
электронодонорные заместители в радикале
R, понижая положительный заряд на
реакционном центре, замедляет нуклеофильную
атаку. В то же время увеличению объема
R затрудняет подход нуклеофила к
реакционному центру. Совместное действие
индуктивного и объемного эффектов
определяет ряд реакционных способностей
субстратов в реакциях нуклеофильного
замещения:
спех
реакции SN2
определяется эффективностью атаки
нуклеофила на положительно заряженный
реакционный центр субстрата. При этом,
чем выше этот положительный заряд, тем
эффективнее взаимодействие. Поэтому
электронодонорные заместители в радикале
R, понижая положительный заряд на
реакционном центре, замедляет нуклеофильную
атаку. В то же время увеличению объема
R затрудняет подход нуклеофила к
реакционному центру. Совместное действие
индуктивного и объемного эффектов
определяет ряд реакционных способностей
субстратов в реакциях нуклеофильного
замещения:
Введение электроакцепторных заместителей в радикал R приводит к увеличению положительного заряда на реакционном центре субстрата, что делает нуклеофильную атаку более эффективной. Так, аллилхлорид гидролизуется более эффективно, чем хлорпропан из-за активирующего действия отрицательного индуктивного эффекта винильной группы:
CH2 = CH CH2Cl CH3CH2 CH2Cl
В реакциях SN1 скорость-определяющей стадией является образованием карбкатиона. В соответствии с постулатом Хэммонда высокая эндотермичность этой стадии обусловливает высокую степень разрыва связей в ее переходном состоянии
[ R+ ............ X–]
Поэтому структура фрагмента R в переходном состоянии приближается к структуре свободного карбкатиона и все факторы, стабилизирующие карбкатионы, будут стабилизировать переходное состояние а, следовательно, приводить к ускорению реакции.
Факторами стабилизации карбкатиона и, соответственно, переходного состояния гетеролиза связи С-Х являются увеличение объема заместителей при реакционном центре и их электронодонорные свойства. Так, ряд реакционной способности соединений R-X в SN1-реакциях
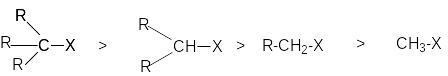
определяются совместным вкладом в стабилизацию соответствующих этому ряду карбкатионов
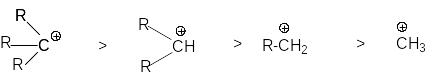
положительного индуктивного эффекта алкильных групп и увеличением объема алкильной группы за счет ее удлинения и разветвления.
Активирующее действие +М-эффекта на скорость SN1-реакций можно проиллюстрировать на примере гидролиза этоксиметилбромида и 2-бромпропана. Первое соединение обладает намного большей реакционной способностью из-за существенной стабилизации карбкатиона
![]()
CH3CH2OCH2 CH3CH2O=CH2
Противоположное влияние индуктивного и объемного эффектов на реакции SN1 и SN2 может быть проиллюстрировано типичной зависимостью скорости реакций нуклеофильного замещения от числа алкильных заместителей при реакционном центре
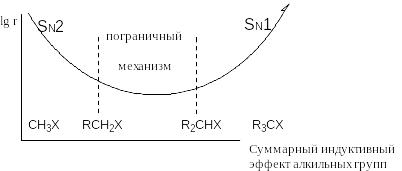
Можно видеть, что в области SN2-механизма электронодонорный и объемный эффект алкильных групп замедляет реакции, в области SN1 – ускоряет. Между этими предельными случаями находится область пограничных механизмов, когда факторы SN1 и SN2 реакций конкурируют между собой.
Влияние уходящей группы
При прочих одинаковых условиях нуклеофильное замещение как по SN1- так и по SN2-механизму должно протекать тем быстрее, чем ниже энергия гетеролитического разрыва связи С-Х. Понижение этой энергии во многом связано со стабилизацией образующегося аниона за счет его лучшей поляризуемости (в случае галогенид-анионов) или эффектов сопряжения (для эфиров сульфокислот и диалкилсульфенов)
В то же время у спиртов и эфиров в уходящих группах –ОН и –OR отсутствуют структурные возможности для стабилизации, поэтому их отщепление эффективно при действии кислотного катализа (см. выше).
Стабилизация уходящей группы гораздо рельефнее влияет на ускорение SN1-реакций по сравнению с реакциями SN2. Это связано с большей степенью разрыва связей в скорость-определяющей стадии SN1-реакции. Поэтому чем больше способность к стабилизации у уходящей группы, тем больше вероятность SN1-механизма.
