
- •Лекции №51-52 гетероциклические соединения
- •Классификация
- •П ятичленные ароматические гетероциклы с одним гетероатомом
- •Пятичленные ароматические гетероциклы с одним гетероатомом Пиррол, фуран, тиофен
- •Методы получения
- •Физические свойства и строение
- •Химические свойства
- •Основные свойства
- •Кислотные свойства пиррола
- •Р еакции электрофильного замещения
- •Реакции присоединения
- •Методы получения
- •Физические свойства и строение
- •Химические свойства
- •Основные свойства
- •Реакции электрофильного замещения
Реакции присоединения
Гидрирование
П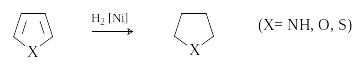 иррол,
фуран и тиофен присоединяют водород в
условиях каталитического гидрирования
с образованием тетрагидропроизводных.
иррол,
фуран и тиофен присоединяют водород в
условиях каталитического гидрирования
с образованием тетрагидропроизводных.
Т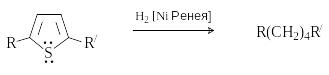 руднее
других гидрируется тиофен, который
отравляет катализатор. Особенностью
химии тиофена является восстановительная
десульфуризация, которая используется
в синтетических целях для получения
соединений, трудно доступных другими
методами.
руднее
других гидрируется тиофен, который
отравляет катализатор. Особенностью
химии тиофена является восстановительная
десульфуризация, которая используется
в синтетических целях для получения
соединений, трудно доступных другими
методами.
Реакция Дильса-Альдера
Р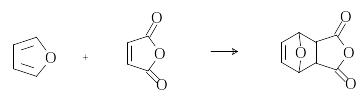 еакции
циклоприсоединения характерны для
фурана, который в большей степени, чем
пиррол и тиофен, проявляет свойства
сопряженного диена. Например, он вступает
при комнатной температуре в реакцию
диенового синтеза с таким активным
диенофилом, как малеиновый ангидрид.
еакции
циклоприсоединения характерны для
фурана, который в большей степени, чем
пиррол и тиофен, проявляет свойства
сопряженного диена. Например, он вступает
при комнатной температуре в реакцию
диенового синтеза с таким активным
диенофилом, как малеиновый ангидрид.
Индол
И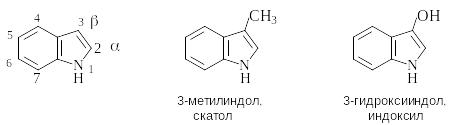 ндол
содержит конденсированные бензольный
и пиррольный циклы (является бензологом
пиррола). Ниже приведены нумерация
циклов и примеры систематической и
тривиальной номенклатуры производных
индола.
ндол
содержит конденсированные бензольный
и пиррольный циклы (является бензологом
пиррола). Ниже приведены нумерация
циклов и примеры систематической и
тривиальной номенклатуры производных
индола.
Методы получения
Синтез индолов по Фишеру
М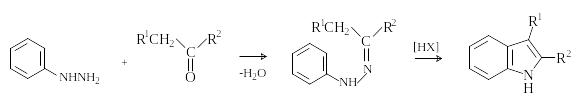 етод
состоит в циклизации фенилгидразонов
в присутствии кислотного катализатора
(H2SO4,
ZnCl2).
етод
состоит в циклизации фенилгидразонов
в присутствии кислотного катализатора
(H2SO4,
ZnCl2).
Механизм реакции:
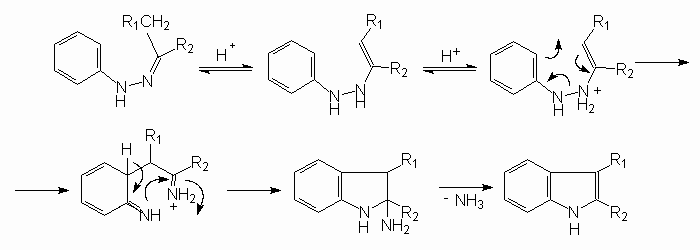
В присутствии кислот происходит изомеризация гидразонов в гидразины с последующей сигматропной перегруппировкой и замыканием пиррольного цикла. Ключевой стадией процесса является разрыв слабой связи N-N и образование прочной связи С-С. Это согласованный процесс, аналогичный перегруппировке Кляйзена аллилфениловых эфиров (см. лек. №30).
Физические свойства и строение
Индол и его гомологи – бесцветные кристаллические вещества с неприятным запахом.
Индол содержит плоскую циклическую сопряженную систему, включающую 10 -электронов, в том числе неподеленную пару электронов атома азота. Таким образом, индол может быть отнесен к ароматическим -избыточным гетероциклическим соединениям. Атом азота выступает как электронодонор, повышая электронную плотность на атомах углерода.
И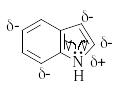 ндол
является электронодонорным соединением
(ЭИ 7,8 эВ).
ндол
является электронодонорным соединением
(ЭИ 7,8 эВ).
Химические свойства
Основные свойства
И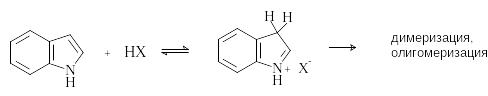 ндол
является очень слабым основанием.
Протонирование происходит по положению
3, далее протекает олигомеризация.
ндол
является очень слабым основанием.
Протонирование происходит по положению
3, далее протекает олигомеризация.
Таким образом, индол, как и пиррол, является ацидофобным соединением.
Реакции электрофильного замещения
Все реакции электрофильного замещения в индоле идут по пиррольному кольцу. Существенным отличием от пиррола является ориентация электрофильного замещения в положение 3, что обусловлено более эффективной стабилизацией промежуточно образующегося катиона.

(I)
(II)
Катион (I), образующийся при атаке электрофилом по положению 3, эффективно стабилизирован с участием атома азота, тогда как для изомерного катиона (II) невозможна стабилизация без нарушения ароматичности бензольного кольца.
И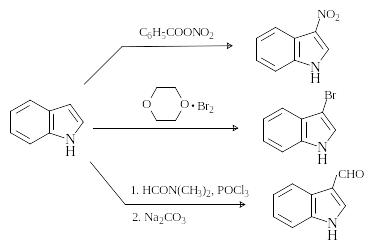 з-за
ацидофобности индола выбор условий
электрофильного замещения требует тех
же самых предосторожностей, что и в
случае пиррола.
з-за
ацидофобности индола выбор условий
электрофильного замещения требует тех
же самых предосторожностей, что и в
случае пиррола.
