
- •Лекции №51-52 гетероциклические соединения
- •Классификация
- •П ятичленные ароматические гетероциклы с одним гетероатомом
- •Пятичленные ароматические гетероциклы с одним гетероатомом Пиррол, фуран, тиофен
- •Методы получения
- •Физические свойства и строение
- •Химические свойства
- •Основные свойства
- •Кислотные свойства пиррола
- •Р еакции электрофильного замещения
- •Реакции присоединения
- •Методы получения
- •Физические свойства и строение
- •Химические свойства
- •Основные свойства
- •Реакции электрофильного замещения
Химические свойства
Основные свойства
П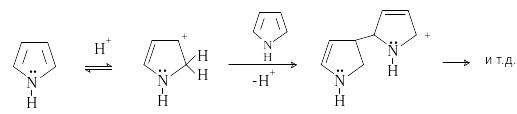 иррол
является чрезвычайно слабым основанием.
Протонирование по атому азота означает
нарушение стабильной -системы
и потерю ароматичности. В действительности
присоединение протона происходит по
атомам углерода пиррольного кольца,
преимущественно по -положению.
Образующаяся таким образом сопряженная
кислота атакует молекулу пиррола, в
результате чего происходит полимеризация.
иррол
является чрезвычайно слабым основанием.
Протонирование по атому азота означает
нарушение стабильной -системы
и потерю ароматичности. В действительности
присоединение протона происходит по
атомам углерода пиррольного кольца,
преимущественно по -положению.
Образующаяся таким образом сопряженная
кислота атакует молекулу пиррола, в
результате чего происходит полимеризация.
Фуран также полимеризуется под действием кислот. Поэтому пиррол и фуран называют ацидофобными соединениями. Введение электроноакцепторных групп снижает ацидофобность. Например, фурфурол и пирослизевая кислота устойчивы к действию кислот.
Тиофен, в отличие от пиррола и фурана, неацидофобен.
Кислотные свойства пиррола
Пиррол является слабой NH-кислотой (рКа=17,5). По кислотности он превосходит амины и близок к спиртам. Соли пиррола получают взаимодействием пиррола с металлами, амидами металлов, металлоорганическим соединениями.
Р еакции электрофильного замещения
Пиррол, фуран и тиофен являются электронодонорными соединениями и проявляют высокую реакционную способность по отношению к электрофилам. Реакционная способность в реакциях электрофильного замещения возрастает в ряду бензол<тиофен<фуран<пиррол.
Электрофильное замещение идет преимущественно в положение 2, что вытекает из сравнения стабильности -коплексов, ведущих к продуктам 2- и 3-замещения.

(I)
(II)
Как видно из приведенной выше для пиррола схемы, в -коплексе (I) достигается более эффективная делокализации положительного заряда (три резонансные структуры), чем в -коплексе (II) (две резонансные структуры).
Взаимодействие гетероциклов с электрофилами может привести и к образованию продуктов присоединения (см. кислотные свойства). Склонность к такого рода превращениям убывает в ряду фуран>пиррол>тиофен, что соответствует степени стабилизации их ароматических систем.
Пиррол по реакционной способности по отношению к электрофилам напоминает активированные ароматические субстраты (фенол или ароматические амины). Из-за ацидифобности пиррола при проведении реакций электрофильного замещения необходимо избегать сильно кислых сред. Основные SE-реакции пиррола суммированы на схеме.
Нитрование и сульфирование пиррола возможны только в том случае, если исключена сильнокислая среда. Нитрование проводят действием ацетилнитрата при низких температурах. Для сульфирование используют связанный в комплекс SO3, например, пиридинсульфотриоксид. Галогенирование протекает без катализатора и дает тетрагалогенпирролы.
П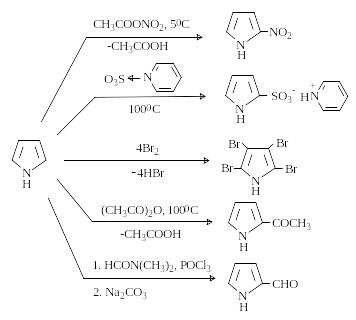 иррол
ацилируется ангидридами кислот в
отсутствие катализатора. Как активированный
субстрат пиррол вступает в реакции
формилирования. Наиболее общим методом
формилирования пирролов является
реакция Вильсмейера-Хаака.
иррол
ацилируется ангидридами кислот в
отсутствие катализатора. Как активированный
субстрат пиррол вступает в реакции
формилирования. Наиболее общим методом
формилирования пирролов является
реакция Вильсмейера-Хаака.
Ф уран,
как и пиррол, ацидофобен, поэтому реакции
с электрофилами проводят в отсутствие
сильных кислот. Фуран ацилируется
ангидридами кислот в присутствии мягких
кислот Льюиса, сульфируется
пиридинсульфотриоксидом, формилируется
по реакции Вильсмейера-Хаака. Фуран
реагирует более селективно, чем пиррол.
Во всех случаях образуются исключительно
продукты замещения по положению 2.
уран,
как и пиррол, ацидофобен, поэтому реакции
с электрофилами проводят в отсутствие
сильных кислот. Фуран ацилируется
ангидридами кислот в присутствии мягких
кислот Льюиса, сульфируется
пиридинсульфотриоксидом, формилируется
по реакции Вильсмейера-Хаака. Фуран
реагирует более селективно, чем пиррол.
Во всех случаях образуются исключительно
продукты замещения по положению 2.
Ф уран
в большей степени, чем пиррол, склонен
к образованию с электрофилами продуктов
не замещения, а присоединения. Даже
реакции, результатом которых является
замещение, могут происходить через
промежуточное образование продуктов
присоединения (по механизму
присоединения-отщепления). При нитровании
фурана ацетилнитратом можно выделить
продукт 2,5-присоединения, который под
действием пиридина (Py),
подвергается элиминированию с образованием
в конечном итоге продукта замещения.
уран
в большей степени, чем пиррол, склонен
к образованию с электрофилами продуктов
не замещения, а присоединения. Даже
реакции, результатом которых является
замещение, могут происходить через
промежуточное образование продуктов
присоединения (по механизму
присоединения-отщепления). При нитровании
фурана ацетилнитратом можно выделить
продукт 2,5-присоединения, который под
действием пиридина (Py),
подвергается элиминированию с образованием
в конечном итоге продукта замещения.
Т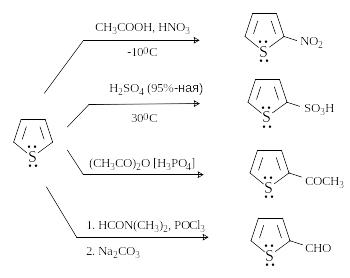 иофен,
в отличие от пиррола и фурана,
неацидофобен, поэтому реакции
электрофильного замещения можно
проводить с обычными электрофильными
агентами, в том числе с использованием
водных растворов минеральных кислот
или в присутствии кислот Льюиса. Реакции
электрофильного замещения превалируют
над процессами присоединения.
иофен,
в отличие от пиррола и фурана,
неацидофобен, поэтому реакции
электрофильного замещения можно
проводить с обычными электрофильными
агентами, в том числе с использованием
водных растворов минеральных кислот
или в присутствии кислот Льюиса. Реакции
электрофильного замещения превалируют
над процессами присоединения.
