
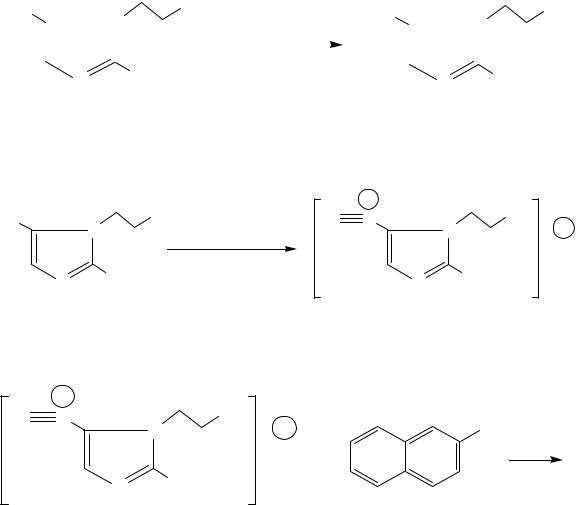
Подлинность
1.ИК-спектр препарата должен полностью совпадать со спектром стандарта.
2.Температура плавления.
3.УФ-спектр препарата в 0,1 M HCl в интервале длин волн 230–350 нм имеет максимум поглощения при 277 нм и минимум при 240 нм. Удельный показатель поглощения в максимуме 277 нм от 365–396.
Химические реакции
1. Реакция восстановления ароматической нитрогруппы до первичной ароматической аминогруппы цинковой пылью в присутствии HCl (водородом в момент выделения).
Zn + HCl = ZnCl2 + 2[H]
O2N |
|
|
N |
OH |
Zn + HCl |
H2N |
|
|
|
OH |
|
|
|
|
CH3 |
|
|
|
N |
||||
|
|
|
|
|
|
|
|
|
CH3 |
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
|
|
N |
|
|
|
N |
|
||||
Продукт дает реакцию на первичные ароматические амины – диазотирования с последующим азосочетанием.
|
|
OH |
+ |
|
OH |
|
H2N |
|
N N |
|
- |
||
N |
NaNO2 + HCl |
N |
|
|||
|
|
|
Cl |
|||
|
|
|
|
|
|
|
|
N |
CH3 |
N |
|
CH3 |
|
Появляется интенсивное оранжевое или красное окрашивание или осадок.
+ |
|
OH |
|
|
N N |
N |
- |
OH |
|
|
|
|||
|
|
|
Cl |
+ |
|
N |
CH3 |
|
|
59
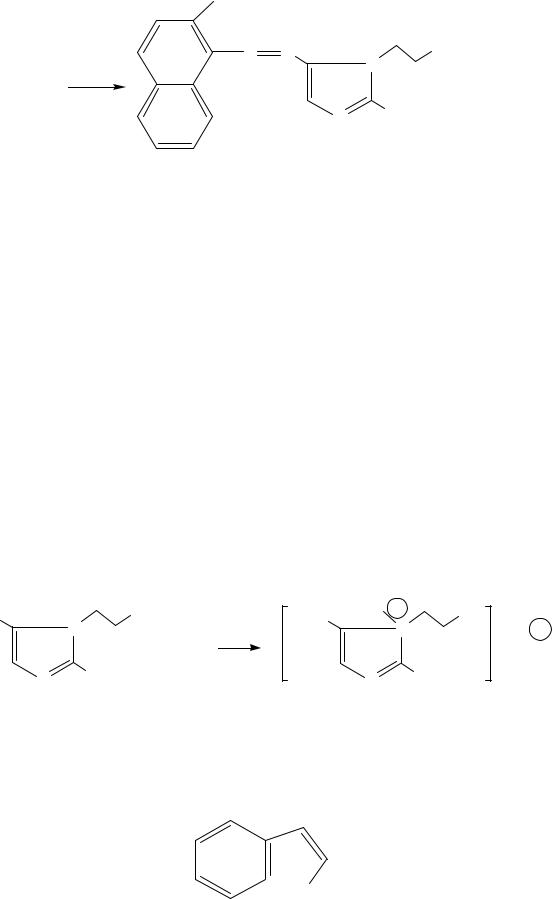
OH |
|
N N |
OH |
|
N |
N |
CH3 |
Чистота
Прозрачность и цветность раствора.
Родственные примеси определяются методом ВЭЖХ, в ФС указаны условия хроматографии (колонка, подвижная фаза, время, детектирование). Метронидазол – фотолабилен (разлагается под действием света), растворы необходимо готовить в защищенном от света месте.
Тяжелые металлы, потеря в весе при высушивании, сульфатная зола.
Количественное определение
Ацидиметрический метод неводного титрования в среде без-
водной уксусной кислоты. Метод основан на слабых основных свойствах основания метронидазола, которые усиливаются в среде про-
тогенного растворителя.
Титрант – 0,1 М хлорная кислота, конечную точку титрования устанавливают потенциометрически.
fэкв = 1.
O2N |
N |
OH |
O2N |
H |
+ |
OH |
|
N |
|||||
|
+ HClO4 |
|
|
- |
||
|
|
|
|
|
ClO4 |
|
N |
|
CH3 |
|
N |
|
CH3 |
Производные бензимидазола
Бензимидазол конденсированная система, содержащая ароматические системы бензола и имидазола. Дибазол – производное бензимидазола.
N
 N
N
H
60
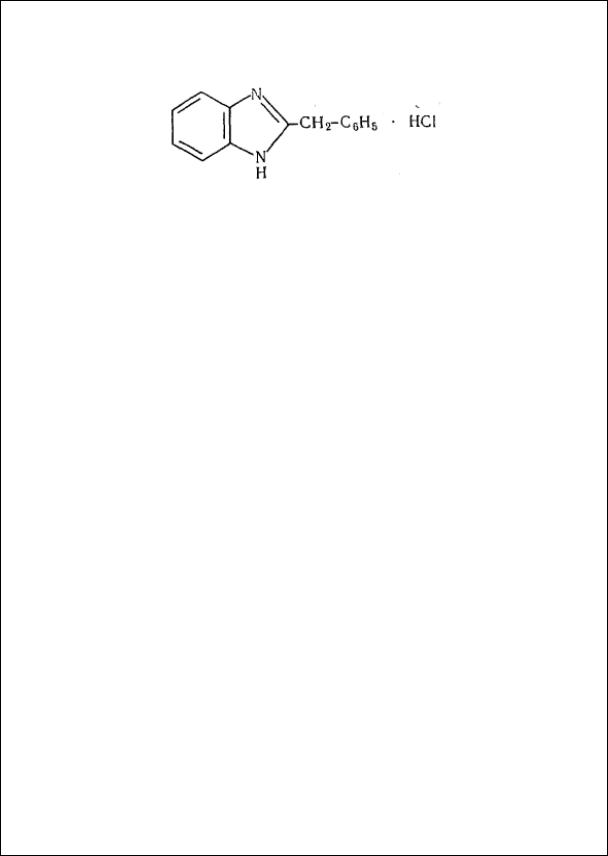
Анализ качества дибазола (бендазола гидрохлорида)
Dibazolum – Дибазол (ГФ Х, с. 243)
Bendazoli Hydrochloridum* 2-Бензилбензимидазола гидрохлорид
C14H12N2 · HC1, М.в.244,73
Описание. Белый или белый со слегка сероватым или желтоватым оттенком кристаллический порошок, горько-соленого вкуса. Гигроскопичен.
Растворимость. Трудно растворим в воде и хлороформе, легко растворим в спирте, мало растворим в ацетоне, практически нерастворим в эфире.
Подлинность. 0,02 г препарата растворяют в 5 мл воды, прибавляют 3 капли разведенной соляной кислоты, 2–3 капли 0,1 н. раствора йода и взбалтывают; образуется красновато-серебри- стый осадок.
0,02 г препарата растворяют в 3 мл воды, прибавляют 1 мл раствора аммиака и образующийся осадок отфильтровывают. Фильтрат, подкисленный 2,5 мл разведенной азотной кислоты, дает характерную реакцию на хлориды (с. 747).
Температура плавления 182–186° (в пределах 3°).
Фенилендиамин. 0,5 г препарата растворяют в 10 мл воды при нагревании до 90°, подкисляют 0,5 мл 1 н. раствора соляной кислоты, прибавляют 1 каплю 1 % раствора хлорида окисного железа; не должно появляться розовое окрашивание.
Потеря в весе при высушивании. Около 0,5 г препарата
(точная навеска) сушат при 70–80° до постоянного веса. Потеря в весе не должна превышать 1,5 %.
Органические примеси. 0,3 г препарата растворяют в 5 мл концентрированной серной кислоты. Окраска полученного раствора не должна быть интенсивнее эталонов № 5а или № 4в.
Сульфатная зола и тяжелые металлы. Сульфатная зола из 0,5 г препарата не должна превышать 0,1 % и должна выдерживать испытание на тяжелые металлы (не более 0,001 % в препарате).
61
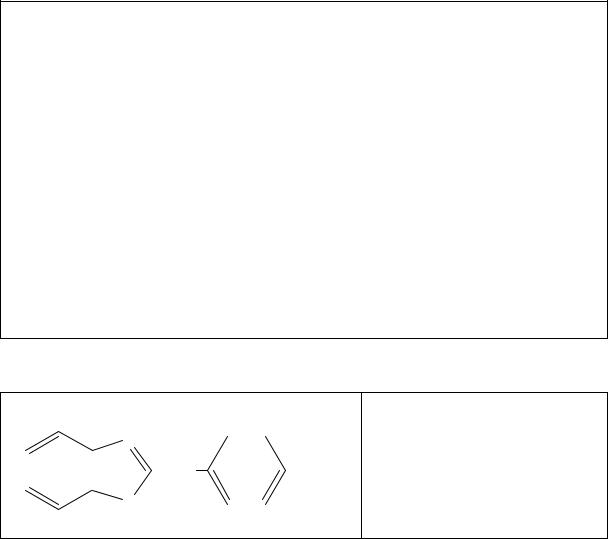
Количественное определение. Около 0,15 г препарата (точ-
ная навеска), предварительно высушенного при 70–80° до постоянного веса, растворяют в 10 мл безводной уксусной кислоты, прибавляют 5 мл раствора ацетата окисной ртути и титруют 0,1 н. раствором хлорной кислоты до голубовато-зеленого окрашивания (индикатор – кристаллический фиолетовый).
Параллельно проводят контрольный опыт.
1 мл 0,1 н. раствора хлорной кислоты соответствует 0,02447 г C14H12N2 · HCl, которого в высушенном препарате должно быть не менее 99,0 %.
Хранение. Список Б. В хорошо укупоренной таре.
Высшая разовая доза внутрь 0,05 г. Высшая суточная доза внутрь 0,15 г.
Спазмолитическое, гипотензивное средство.
Фармакопейный анализ бендазола гидрохлорида
Химическая структура |
Функциональные группы |
|
|
|
N |
1) |
Вторичная аминогруппа |
||||||
|
|
|
|
|
|
|
|
||||
2) |
Третичный атом азота |
||||||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
CH2 |
|
|
|
* HCl 3) |
Соль гидрохлорид |
|
|
|
|
|
|
|||||||
|
|
|
N |
|
|
|
|
|
|||
|
|
|
|
|
|||||||
|
|
|
H |
|
|
|
|
|
|||
Подлинность
1.ИК-спектр препарата должен полностью совпадать со спектром стандарта или с рисунком, прилагаемым к фармакопейной статье.
2.УФ-спектр спиртового раствора препарата имеет характерные максимумы и минимумы поглощения.
3.Температура плавления.
Химические реакции
1. Реакция комплексообразования с раствором йода протекает за счет наличия в молекуле бендазола гидрохлорида третичного атома азота. Реакция проводится в кислой среде, способствующей ионизации ЛВ.
Образуется красно-серебристый с перламутровым блеском осадок полийодида бендазола:
62
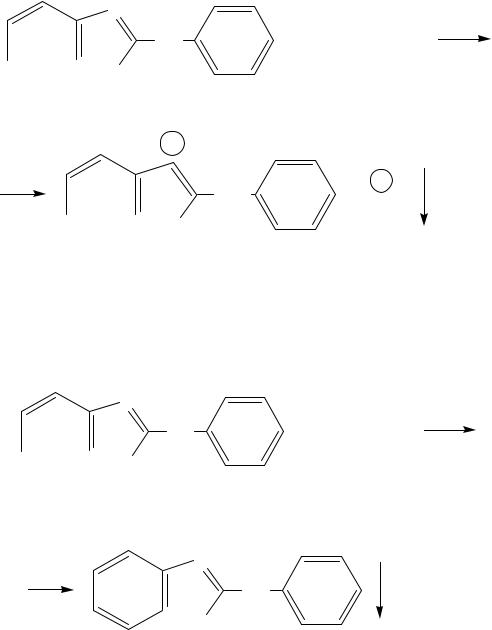
N
CH2 |
* |
HCl + |
I |
+ KI |
|
|
2 |
|
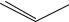
 N
N
H
+ |
|
NH |
* I - * I2 + KCl |
CH2 |
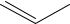
 N
N
H
2. Реакция на хлорид-ион.
Предварительно осаждают раствором аммиака основание дибазола, чтобы исключить реакцию образования серебряной соли по вторичной аминогруппе.
N
CH2 |
* |
HCl + NH |
|
3 |
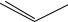
 N
N
H
N |
|
CH2 |
+ NH4Cl |
 N
N
H
Основание отфильтровывают, в фильтрате после подкисления HNO3 доказывают хлорид-ионы по реакции с AgNO3.
NH4Cl + AgNO3 = AgCl↓ + NH4NO3
Нефармакопейные реакции
3. Реакция образования серебряной соли бендазола. При действии AgNO3 в спиртовой среде, в присутствии NH3 конц. выпадает белый осадок серебряной соли дибазола. Образующийся AgCl в условиях реакции растворяется в аммиаке.
63
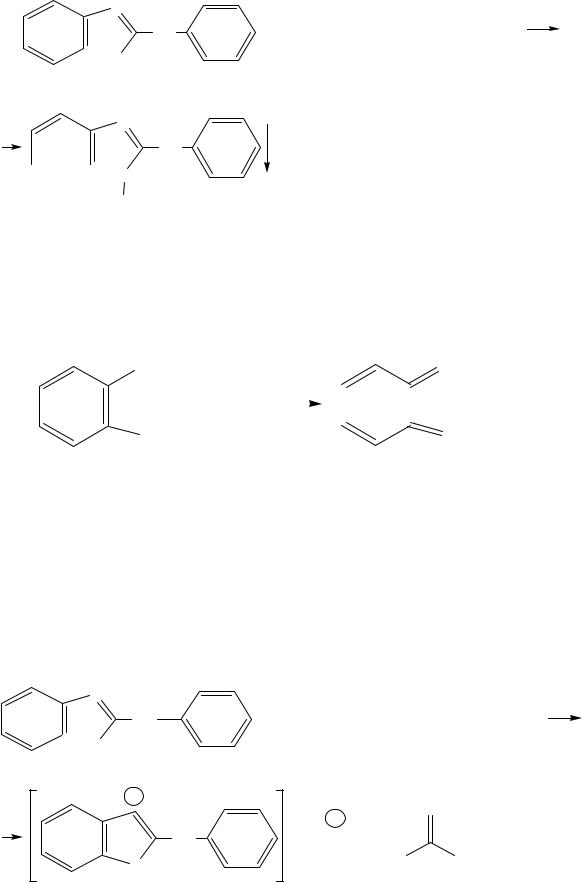
N |
|
CH2 |
* HCl + 2 AgNO3 + 4 NH4OH |
 N
N
H
N |
|
CH2 |
+ Ag(NH3)2Cl + 2 NH4NO3+ 4 H2O |
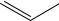
 N
N
Ag
Чистота
Специфическая примесь – 1,2-фенилендиамин определяют по реакции окисления хлоридом железа (III) в присутствии HCl. Не должно быть желтого окрашивания. При наличии примеси образуется окрашенный хинондиимин.
NH2 NH
+ FeCl3 |
|
|
|
+ FeCl2 |
|
|
|||
NH2 |
|
NH |
||
Количественное определение
1. Ацидиметрический метод неводного титрования в среде муравьиной кислоты и уксусного ангидрида (для подавления диссо-
циации хлорид-ионов). Метод основан на слабых основных свойствах оснований бендазола, которые усиливаются в среде протогенного растворителя.
Титрант – 0,1 М хлорная кислота, индикатор – кристаллический фиолетовый.
N |
|
CH2 |
* HCl + HClO4 + (CH3COO)2O |
 N
N
H
+ |
|
|
NH |
- |
O |
CH2 |
ClO4 + |
+ CH3COOH |
N |
H3C |
Cl |
H |
|
|
fэкв = 1.
64
Нефармакопейные методы количественного определения
2. Алкалиметрический метод (вариант вытеснения). Метод основан на реакции вытеснения органического основания сильным основанием NaOH. Индикатор – фенолфталеин. Титруют в водноспиртовой среде для извлечения основания, f = 1.
N |
|
CH2 |
* HCl + NaOH |
 N
N
H
N |
|
CH2 |
+ NaCl + H2O |
 N
N
H
Производные имидазолина
Имидазолин – частично гидрированный имидазол.
43 N
51 2
N
H
К производным имидазолина относятся клонидина гидрохлорид
(Клофелин), нафазолина нитрат (Нафтизин), ксилометазолин (Галазолин).
Гистамин – биологический амин, производное имидазола. Производные гистамина и близкие по структуре соединения:
дифенгидрамина гидрохлорид (димедрол), хлоропирамин (супрастин), ранитидин, фамотидин.
65
Определение качества лекарственных средств из группы производных пиридина
Лекарственные препараты, производные пиридина
Производные пиридинметанола: пиридоксина гидрохлорид,
пиридоксальфосфат, пирикарбат (пармидин), эмоксипин.
Производные дигидропиридина: нифедипин, амлодипин,
никардипин.
Производные пиридин-3-карбоновой кислоты: кислота никотиновая, никотинамид, никетамид (диэтиламид кислоты никотиновой), пикамилон.
Производные пиридин-4-карбоновой кислоты: изониазид,
фтивазид, протионамид, этионамид.
Производные пиперидина: тригексифенидила гидрохлорид (циклодол), кетотифен (задитен), лоратидин (кларитин).
Производные пиперазина: циннаризин.
Пиридин – шестичленный ароматический гетероцикл с одним атомом азота.
N
Анализ качества пиридоксина гидрохлорида
Pyridoxini hydrochloridum Пиридоксина гидрохлорид
(ГФ Х, с. 572)
Pyridoxinum hydrochloricum Vitaminum В6
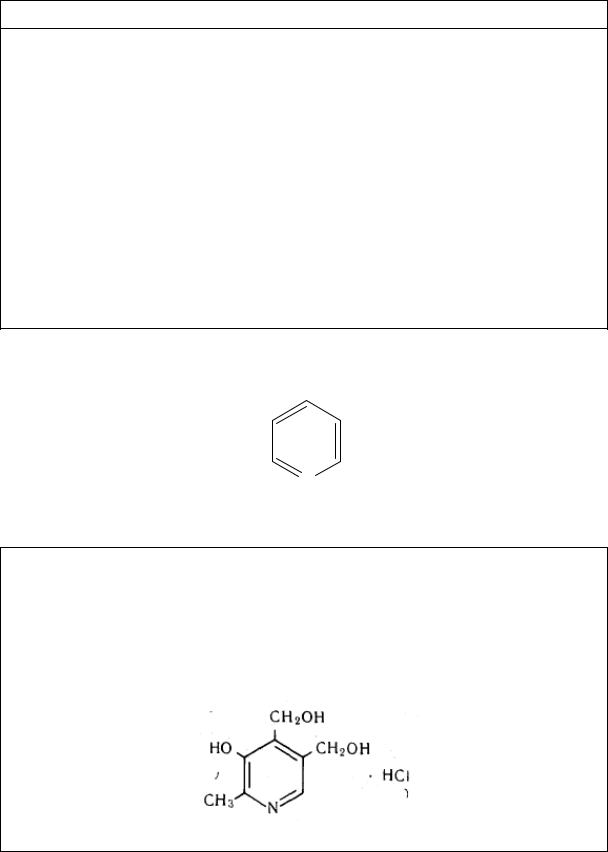
Витамин В6 2-Метил-3-окси-4,5-ди-(оксиметил)-пиридина гидрохлорид
C8H11NО3 HCl, М. в. 205,64
66

Описание. Белый мелкокристаллический порошок без запаха, горьковато-кислого вкуса.
Растворимость. Легко растворим в воде, трудно растворим в 95 % спирте, практически нерастворим в эфире.
Подлинность. 0,01 г препарата растворяют в 10 мл воды. К 0,1 мл полученного раствора прибавляют 1 мл воды, 2 мл аммиачного буферного раствора, 1 мл раствора 2,6-дихлорхинонхлори- мида, 2 мл бутилового спирта и встряхивают в течение 1 минуты.
Вслое бутилового спирта появляется голубое окрашивание.
К1 мл того же раствора прибавляют две капли раствора хлорида окисного железа; появляется красное окрашивание, исчезающее при добавлении разведенной серной кислоты.
Температура плавления 203–206° (с разложением). Скорость подъема температуры 5° в минуту.
Прозрачность и цветность раствора. Раствор 0,5 г препара-
та в 5 мл воды должен быть прозрачным и бесцветным. Кислотность. рН 2,5–3,2 (1 % водный раствор).
Метиловый эфир пиридоксина. 0,01 г препарата растворяют в 10 мл воды. К 0,1 мл полученного раствора прибавляют 1 мл раствора борной кислоты, 2 мл аммиачного буферного раствора, 1 мл раствора 2,6-дихлорхинонхлоримида, 2 мл бутилового спирта и встряхивают в течение 1 минуты. В слое бутилового спирта не должно появляться голубое окрашивание.
Потеря в весе при высушивании. Около 0,5 г препарата
(точная навеска) сушат при 100–105° до постоянного веса. Потеря в весе не должна превышать 0,5 %.
Сульфатная зола и тяжелые металлы. Сульфатная зола из
0,5 г препарата не должна превышать 0,1 % и должна выдерживать испытание на тяжелые металлы (не более 0,001 % в препарате).
Количественное определение. 1. Около 0,15 г препарата (точ-
ная навеска) растворяют в 20 мл безводной уксусной кислоты при слабом нагревании. Раствор охлаждают, прибавляют 5 мл раствора ацетата окисной ртути и титруют 0,1 н. раствором хлорной кислоты до появления изумрудно-зеленого окрашивания (индикатор – кристаллический фиолетовый).
Параллельно проводят контрольный опыт.
1 мл 0,1 н. раствора хлорной кислоты соответствует 0,02056 г C8H11NО3 HCl, которого в пересчете на сухое вещество должно быть не менее 99,0 %.
2.Около 0,1 г препарата (точная навеска) растворяют в воде
вмерной колбе емкостью 50 мл и доводят объем раствора водой
67

до метки. К 20 мл полученного раствора прибавляют 2–3 капли раствора бромтимолового синего и титруют из микробюретки 0,1 н. раствором едкого натра до первого появления голубой окраски.
1 мл 0,1 н. раствора едкого натра соответствует 0,003545 г Cl, которого в пересчете на сухое вещество должно быть не менее
17,1 % и не более 17,35 %.
Хранение. В хорошо укупоренных банках оранжевого стекла, в прохладном месте.
Применение. Витамин В6.
Фармакопейный анализ пиридоксина гидрохлорида
Химическая структура |
|
Функциональные группы |
||||
|
|
|
|
|||
|
CH2OH |
1) |
Фенольный ОН |
|||
HO |
|
|
|
CH2OH |
2) |
Два спиртовых ОН |
|
|
|
||||
|
|
|
3) |
Третичная аминогруппа |
||
|
|
|
||||
H3C |
|
|
|
* HCl |
4) |
Соль гидрохлорид |
N |
|
|
||||
|
|
|
|
|
|
|
Подлинность
1.Температура плавления 203−206 C (с разложением).
2.ИК-спектр препарата должен полностью совпадать со спектром стандарта.
3.УФ-спектр в фосфатном буферном растворе (рН 7), в диапазоне 280 450 нм у препарата имеются два максимума при 254
и324 нм.
Химические реакции
1. Реакция конденсации образование индофенолового красителя. Препарат растворяют в воде, прибавляют аммиачный буферный раствор, раствор 2,6-дихлорхинонхлоримид и бутиловый спирт, встряхивают реакционную смесь 1 мин.
Продукт конденсации извлекается в бутанол, слой бутанола окрашивается в голубой цвет.
68
