

Посторонние алкалоиды. 1 г препарата помещают в делительную воронку и растворяют в 15 мл раствора едкого натра. Полученный раствор взбалтывают с хлороформом (3 раза по 15 мл). Хлороформные извлечения собирают в колбу и отгоняют хлороформ на водяной бане до объема 1–2 мл. Остаток растворяют в 15–20 мл эфира. Эфирный раствор помещают в делительную воронку, ополаскивают колбу эфиром (3 раза по 5 мл) и сливают его в ту же делительную воронку, затем прибавляют 5 мл раствора едкого натра и взбалтывают в течение 2 минут. Отстоявшийся водно-щелочной слой отделяют возможно полнее, эфирный раствор промывают водой (3 раза по 10 мл) и после отделения от водного слоя сливают в сухую колбу, содержащую 3 г безводного сульфата натрия. Делительную воронку промывают эфиром (2 раза по 5 мл), присоединяя его к основному раствору. Содержимое колбы хорошо встряхивают и оставляют на 10 минут. Обезвоженный эфирный раствор фильтруют в сухую взвешенную колбу, фильтр и сульфат натрия промывают эфиром (2 раза по 5 мл), собирая последний в ту же колбу, затем отгоняют эфир и остаток в колбе сушат при 100–105° до постоянного веса. Остаток не должен превы-
шать 0,6 %.
Потеря в весе при высушивании. Около 0,5 г препарата
(точная навеска) сушат при 100–105° до постоянного веса. Потеря в весе не должна превышать 14,5 %.
Сульфатная зола из 0,5 г препарата не должна превышать
0,1 %.
Количественное определение. Около 0,15 г препарата (точ-
ная навеска) растворяют в 5 мл раствора ацетата окисной ртути, предварительно нейтрализованного 0,1 н. раствором хлорной кислоты по кристаллическому фиолетовому, прибавляют 10 мл безводной уксусной кислоты и титруют с тем же индикатором 0,1 н. раствором хлорной кислоты до перехода фиолетовой окраски
взеленую.
1мл 0,1 н. раствора хлорной кислоты соответствует 0,03218 г
C17Hl9NО3 HCl, которого в пересчете на сухое вещество должно быть не менее 98,5 %.
Хранение. Список А. В хорошо закрытых банках оранжевого стекла, в защищенном от света месте.
Высшая разовая доза внутрь и под кожу 0,02 г. Высшая суточная доза внутрь и под кожу 0,05 г.
Анальгезирующее (наркотическое) средство.
109
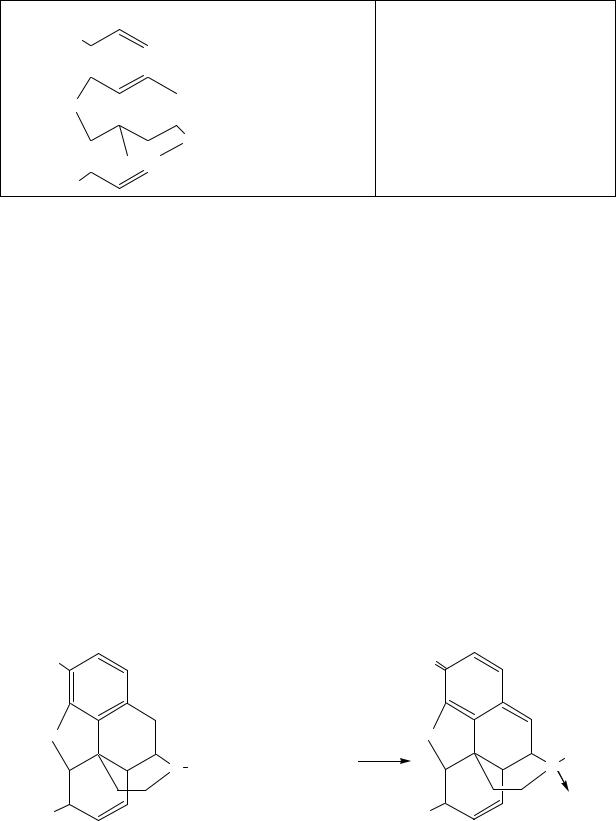
Фармакопейный анализ морфина гидрохлорида
Химическая структура |
Функциональные группы |
HO |
A |
|
|
1) |
Фенольный гидроксил |
||||||||
|
|
|
|
|
2) |
Спиртовой гидроксил |
|||||||
|
|
|
|
|
|
|
|
|
3) |
Третичная аминогруппа |
|||
O E |
|
|
|
|
|
|
|||||||
|
|
B |
|
4) |
Соль гидрохлорид |
||||||||
|
|
|
C |
|
|
|
|
D |
N |
|
CH3 * HCl * 3H2O |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||
HO |
|
|
|
|
|
|
|
|
|
|
|
||
Морфин – производное алкалоида морфинана. Морфинан – частично гидрированный октагидрофенантренизохинолин. Циклы А, B, C образуют частично гидрированный фенантрен, C, D – гидрированный изохинолин (цикл D – пиперидин). Цикл Е – фурановый.
Подлинность
1.ИК-спектр препарата должен полностью совпадать со спектром стандарта.
2.УФ-спектр поглощения. Положение максимумов и минимумов должно соответствовать значениям, приведенным в ФС.
3.Удельное вращение 2 %-го водного раствора морфина гидрохлорида. Препарат имеет пять асимметрических атомов углерода, применяется в виде левовращающего изомера.
Химические реакции
1. Реакция окисления с реактивом Фреде (раствором молибдата аммония в концентрированной серной кислоте – (NH4)2MoO4 в H2SO4). Реакция основана на восстановительных свойствах морфина гидрохлорида (окисляется фенольный фрагмент и аминогруппа).
HO |
O |
O |
* HCl |
H2SO4 |
O |
CH3 |
|
N CH3 + (NH4)2MoO4 |
|
N |
|
|
|
|
||
HO |
|
HO |
O |
|
|
|
|||
Mo(VI) 1e = Mo(V)
Появляется фиолетовая окраска, переходящая в синюю, при стоянии окраска переходит в зеленую.
110
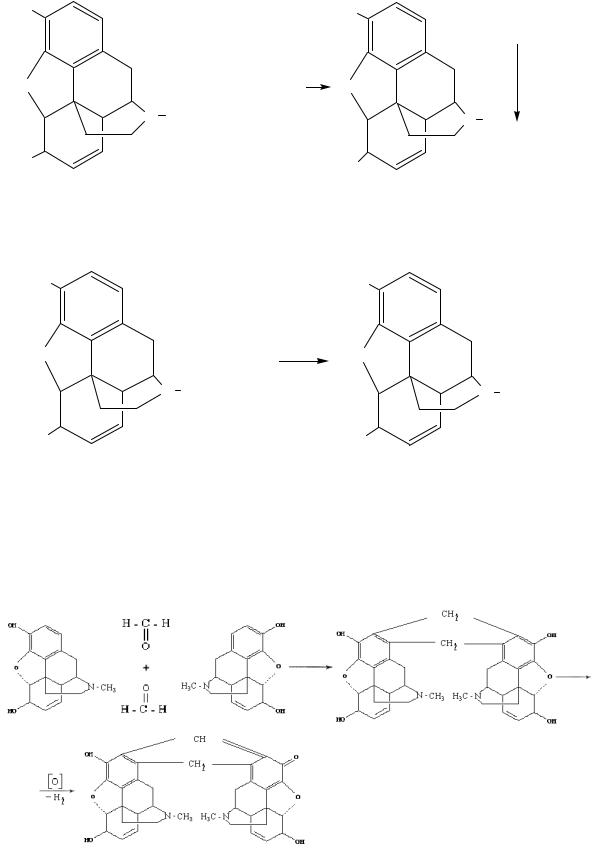
2. Реакция осаждения основания морфина гидрохлорида из растворов при добавлении аммиака. Образуется белый кристаллический осадок.
HO |
HO |
O |
* HCl * H2O + NH3 |
O |
+NH4Cl |
|
N CH3 |
|
N CH |
|
|
|
3 |
HO |
|
HO |
|
Далее осадок основания морфина растворяется в щелочи. При добавлении избытка раствора едкого натра за счет фенольного гидроксила образуются растворимые морфинаты.
HO |
NaO |
O
+ NaOH
O |
+ H2O |
|
N CH3 |
N CH3 |
HO |
HO |
3. Реакция окислительной конденсации с реактивом Марки. Реакция конденсации протекает как электрофильное замещение в ортоположении к фенольному гидроксилу. Далее в присутствии конц. H2SO4 образуется окрашенное соединение хиноидной структуры. Возникает пурпурное окрашивание, быстро переходящее в синефиолетовое (отличие от кодеина).
111
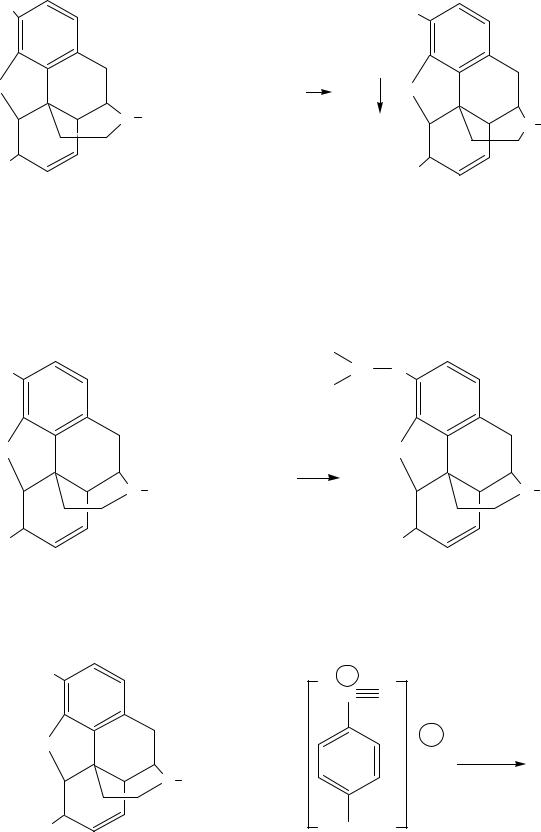
4. Раствор препарата дает характерную реакцию на хлориды.
HO |
HO |
|
O |
* HCl * H2O + AgNO3 |
AgCl + O |
|
||
|
N CH3 |
N CH3 |
HO |
|
HO |
|
|
Нефармакопейные реакции
4. Реакция комплексообразования на фенольный гидроксил c FeCl3. Образуется комплексное соединение синего цвета.
|
|
|
Cl |
HO |
|
|
Fe O |
|
|
|
Cl |
O |
* HCl |
|
O |
|
+ FeCl3 |
|
|
|
N CH3 |
N CH3 |
|
HO |
|
|
HO |
5. Морфин, как производное фенола, вступает в реакцию азосочетания с солями диазония. Образуется азокраситель красного цвета.
HO |
|
|
+ |
|
|
|
|
N N |
|
O |
* HCl |
|
- |
|
+ |
Cl |
|||
|
||||
|
N CH3 |
|
||
|
|
|
||
HO |
|
|
SO3H |
112
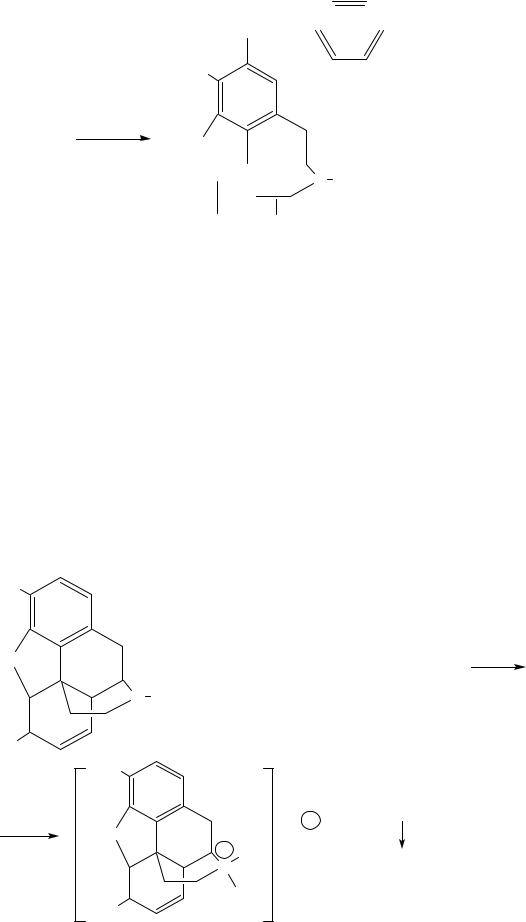
N N
N
 SO3H
SO3H
HO
O


 N CH3
N CH3
HO
7. Реакция нитрозирования с натрия нитритом – электрофильное замещение в орто-положении к фенольному гидроксилу. Образуется 2-нитрозоморфин, который при подщелачивании аммиаком дает желтое окрашивание.
Чистота
Специфические примеси – посторонние алкалоиды.
Количественное определение
Ацидиметрия (кислотно-основное титрование) в неводной среде. Метод основан на слабых основных свойствах третичного атома азота морфина, которые усиливаются при растворении в протогенном растворителе. Титрант – HClO4, индикатор – кристал-
лический фиолетовый, растворитель – безводная уксусная кислота. Титруют в присутствии ацетата окисной ртути для связывания хло- рид-ионов, fэкв = 1.
HO
O |
* HCl |
+ HClO4 + Hg(CH3COO)2 |
||
|
||||
|
N CH3 |
|
|
|
HO |
|
|
|
|
|
HO |
|
|
|
|
O |
+ |
ClO4- |
+ HgCl2 + 2CH3COOH |
|
|
CH3 |
|
|
|
|
N |
|
|
|
HO |
|
H |
|
|
|
|
|
|
113
Библиографический список
Основной
1.Арзамасцев, А. П. Фармацевтическая химия / А. П. Арзамас-
цев. – М. : ГЭОТАР-МЕД, 2004. 640 с.
2.Беликов, В. Г. Фармацевтическая химия / В. Г. Беликов. М. : Медпресс-информ, 2007. – 624 с.
3. Машковский, М. Д. Лекарственные средства : в 2 т. / М. Д. Машковский. М. : Новая волна, 2001.
4.Руководство к лабораторным занятиям по фармацевтической химии / А. П. Арзамасцев, Э. Н. Аксенова, О. П. Андрианова [и др.].
М. : Медицина, 2001. 384 с.
5.Анализ лекарственных смесей / А. П. Арзамасцев, В. М. Печенников, Г. М. Родионова [и др.]. М. : Компания Спутник+, 2000. 275 с.
6.Государственная фармакопея СССР. 10 изд. М. : Медици-
на, 1968. – 1079 с.
7.Государственная фармакопея СССР / МЗ СССР. – 11-е изд., доп. М. : Медицина, 1987–1989. Вып. 1, 2. Общие методы анализа.
8.Государственная Фармакопея Российской Федерации. 12-е изд. М. : Научный центр экспертизы средств медицинской промышленности, 2008. 704 с.
9.Фармакопея Великобритании. British Pharmacopoeia 2007. London : System Simulation Ltd., 2007.
10.Фармакопея США: USP 29. Национальный формуляр. NF24 : в 2 т. М. : ГЭОТАР-Медиа, 2009. – 1720 с.
Дополнительный
1.Приказ МЗ РФ № 214 от 16.07.97 г. «О контроле качества лекарственных средств, изготовляемых в аптеках».
2.Приказ МЗ РФ № 305 от 16.10.97 г. «О нормах отклонений, допустимых при изготовлении лекарственных средств и фасовке промышленной продукции в аптеках».
3.Бертрам, Г. Катцунг. Базисная и клиническая фармакология /
Г. Катцунг Бертрам. СПб. : Невский диалект ; М. : Бином, 2000.
Т. I.
114
4.Кулешова, М. И. Анализ лекарственных форм, изготовляемых в аптеках / М. И. Кулешова, Л. Н. Гусева, О. К. Сивицкая. М. : Медицина, 1989.
5.Сливкин, А. А. Функциональный анализ органических лекарственных веществ : учеб. пособие / А. А. Сливкин, Н. П. Садчико-
ва. Воронеж, 2007. 426 с.
6.Регистр лекарственных средств России : энциклопедия лекарств. – 7-е изд., перераб. и доп. – М., 2000. – 1520 с.
7.Кузнецова, А. В. Фармацевтическая химия : учеб.-метод. пособие для студентов III курса специальности «Фармация» (5 семестр) / А. В. Кузнецова. – Пенза : Изд-во ПГУ, 2010.
8.Кузнецова, А. В. Фармацевтическая химия : учеб.-метод. пособие для студентов III курса специальности «Фармация» (6 семестр) / А. В. Кузнецова. – Пенза : Изд-во ПГУ, 2010.
115
Учебное издание
Кузнецова Анна Викторовна
Фармакопейный анализ производных фурана, пиррола, пиразола, имидазола, пиридина, хинолина
Редактор Ж. А. Лубенцова
Компьютерная верстка Н. В. Ивановой
Подписано в печать 15.05.2013.
Формат 60x841/16. Усл. печ. л. 6,74.
Тираж 100. Заказ № 463.
_______________________________________________________
Издательство ПГУ
440026, Пенза, Красная, 40. Тел./факс: (8412) 56-47-33; e-mail: iic@pnzgu.ru
116
117

118
