
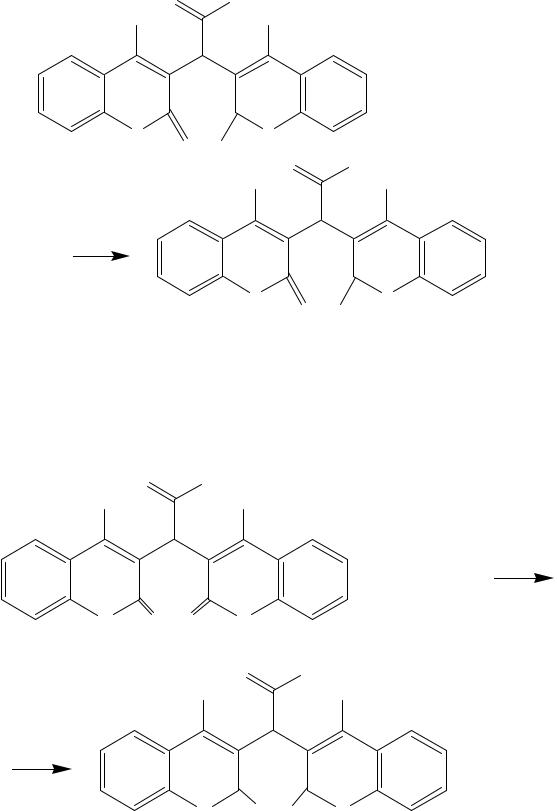
К другой части прибавляют 5 мл раствора аммиака; получается бесцветный раствор.
O OH
OH |
OH |
+ NH3 
O  O
O
O O
O ONH4
OH |
OH |
O 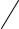 O
O
O O
Нефармакопейные реакции
3. Йодоформенная проба. При щелочном гидролизе сложноэфирной группы этилбискумацетата выделяется этанол, который доказывают реакцией образования йодоформа (CHI3, характерный
запах).
O OH
OH OH
+ 3 NaOH
O O O |
O |
|
|
O |
ONa |
|
ONa |
ONa |
+ C2H5OH
O  O O
O O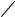 O
O
C2H5OH + 4I2 + 6NaOH = CHI3 + 5NaI + 5H2O + HCOONa
19
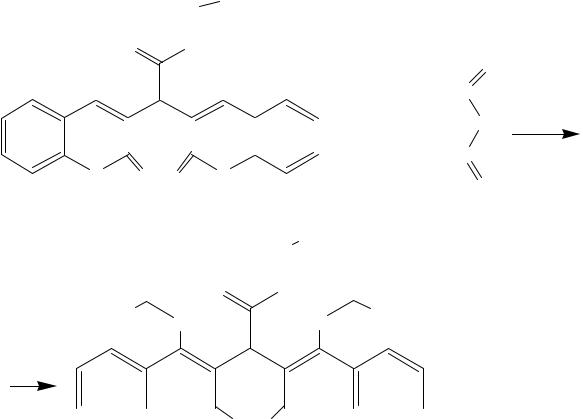
4. Реакция ацетилирования. Енольные гидроксилы с уксусным ангидридом образуют сложные эфиры.
|
|
|
|
|
H2C |
CH3 |
|
|
|
|
|
|
|
|
|
|
||
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
OH |
|
|
|
|
|
|
|
|
|
|
||||
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
2 |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
C |
O |
O O O |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C |
CH3 |
|
|
|
|||||
|
|
|
O |
|
|
|
O |
|
|
|
||||||||
|
|
|
O |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
H3C |
|
|
|
|
|
O |
|
|
|
|
CH3 |
|
|
||||
|
|
|
O |
|
|
|
|
|
O |
|
|
|||||||
+ 2 CH3COOH
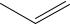
 O
O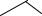 O O
O O O
O

Образуется осадок диацетата этилбискумацетата, его высушивают и определяют температуру плавления.
Чистота
Специфическая примесь ди-(4-оксикумаринил-3)-уксусная кислота определяется методом тонкослойной хроматографии со свидетелем.
Количественное определение
1. Алкалиметрический метод основан на использовании кислотных свойств енольнОГО гидроксила. Препарат не растворим в воде, титрование проводят в среде ацетона. Титрант – раствор – NaOH, индикатор смешанный – метиловый красный и метиленовый синий.
f = 1.
Параллельно проводят контрольный опыт:
20

H2C  CH3
CH3
O O
OH |
OH |
+ NaOH 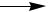
O O
O O
H2C  CH3
CH3
O O
OH |
ONa |
+ H2O
O O
OO
2.Алкалиметрический метод неводного титрования в среде протофильного растворителя (ДМФА), титрант NaOH. В реакции участвуют оба енольных гидроксила.
f(этилбискумацетата) = 1/2.
3. Ацетилирование по реакции образования сложных эфиров с уксусным ангидридом по енольным гидроксилам. Выделившуюся уксусную кислоту титруют натрия гидроксидом.
f(этилбискумацетата) = 1/2.
Анализ качества рутина
Rutinum – Рутин – Rutin (ГФ Х, с. 599)
3-рутинозид кверцетина; 3-рамногликозил-3,5,7, 3’,4’-пентаоксифлавон
C27H30O16 3H2O, М. в. 664,6
21

Описание. Зеленовато-желтый мелкокристаллический порошок без запаха и вкуса.
Растворимость. Практически нерастворим в воде, мало растворим в 95 % спирте, трудно растворим в кипящем спирте, практически нерастворим в растворах кислот, в эфире, хлороформе, ацетоне и бензоле, растворим в разбавленных растворах едких щелочей.
Подлинность. 1 г препарата кипятят со 100 мл 0,5 % раствора соляной кислоты и фильтруют. К 5 мл фильтрата прибавляют 0,3 мл раствора едкого натра и 3 мл реактива Фелинга; при кипячении смеси образуется красный осадок.
5 мг препарата растворяют в 5 мл 1 н. раствора едкого натра; появляется желто-оранжевое окрашивание.
0,02 г препарата растворяют в 5 мл горячего 95 % спирта, добавляют несколько капель концентрированной соляной кислоты и 0,05 г порошка магния или магниевой стружки; постепенно раствор окрашивается в красный цвет.
0,002 % раствор препарата в абсолютном спирте при измерении на спектрофотометре в кювете с толщиной слоя 1 см имеет максимумы поглощения при длинах волн 259 ± 1 нм и 362,5 ± 1 нм.
Примеси, нерастворимые в спирте. 0,1 г препарата кипятят с 6 мл 95 % спирта в колбе с обратным холодильником в течение 5–6 минут. Раствор должен быть прозрачным.
Хлорофилл и пигменты, растворимые в эфире. 0,1 г пре-
парата взбалтывают с 5 мл эфира; эфир должен быть бесцветным.
Алкалоиды. К 2–3 мл насыщенного спиртового раствора препарата приливают 2–3 мл насыщенного раствора пикриновой кислоты. Не должен выделяться осадок.
Кверцетин. Определяют оптическую плотность раствора препарата, приготовленного для количественного определения спектрофотометрическим методом при длинах волн 375 нм (D1) и 362,5 нм (D2). Если отношение D1/D2 не превышает 0,879, то препарат не содержит кверцетина, если оно превышает 0,879, то содержание кверцетина в процентах (X) рассчитывают по формуле
X = 5,943D1 5,200D2 a
где D1 – оптическая плотность испытуемого раствора при длине волны 375 нм; D2 – оптическая плотность испытуемого раствора при длине волны 362,5 нм; а – навеска в граммах.
22

Содержание кверцетина в пересчете на сухое вещество должно быть не более 5,0 %.
Потеря в весе при высушивании. Около 0,5 г препарата
(точная навеска) сушат при 135° до постоянного веса. Потеря в весе должна быть не менее 6 % и не более 9 %.
Сульфатная зола из 0,5 г препарата не должна превышать
0,1 %.
Количественное определение. Около 0,025 г препарата (точ-
ная навеска) растворяют в 10 мл горячего абсолютного спирта и фильтруют через стеклянный фильтр № 4 при слабом разрежении. Фильтр промывают горячим абсолютным спиртом (2 раза по 10 мл). Объединенные фильтраты переносят в мерную колбу емкостью 100 мл, охлаждают и доводят объем раствора тем же спиртом до метки. 5 мл спиртового раствора помещают в мерную колбу емкостью 50 мл и доводят объем раствора абсолютным спиртом до метки. Определяют оптическую плотность полученного раствора на спектрофотометре при длинах волн 375 нм (D1) и 362,5 нм (D2)
вкювете с толщиной слоя 1 см. Если отношение D1/D2 находится
впределах 0,875 ± 0,004, то содержание рутина в процентах (X) вычисляют по формуле
X = D325,5a2 1000 ,
где 325,5 – удельный показатель поглощения E11%см чистого рутина
(безводного) в абсолютном спирте при длине волны 362,5 нм; а – навеска в граммах.
Если отношение D1/D2 превышает 0,879, то содержание рутина в процентах (X) вычисляют по формуле
X = 14,60D2 13,18D1 a
Содержание C27H30O16 в пересчете на сухое вещество должно быть не менее 95,0 %.
Хранение. В хорошо укупоренной таре, предохраняющей от действия света.
Фармакопейный анализ рутина
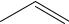
Рутин – производное флавана, в его структуре присутствует флаван или 2-фенилхроман. Производные флавана проявляют Р-витаминную активность – капиллярукрепляющее действие.
23
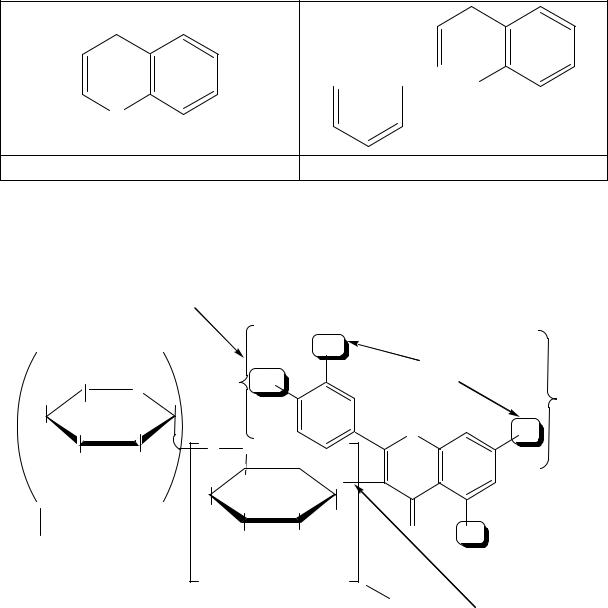
 O
O
O
Хроман |
Флаван |
Рутин по химическому строению гликозид. Сахарная часть включает D-глюкозу и L-рамнозу, агликон – кверцетин, относится к флавоноидам.
агликон кверцетин
|
|
|
|
|
|
OH |
фенольные |
|
H |
|
|
|
|
|
|
OH |
O |
|
HO |
|
|
гидроксилы |
|
|
|
|
|
|
|
||
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H H |
H |
|
|
|
O |
OH |
|
|
|
|
O |
CH2 |
|
||
|
OH |
OH |
|
|
|
||
|
|
|
|
|
x 3H2O |
||
|
|
|
H |
H |
|
O |
|
|
|
|
|
|
|||
|
|
|
OH |
OH |
H |
H |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
L-рамноза |
|
|
H |
OH |
O |
OH |
|
|
|
|
|
||||
|
|
|
|
|
|
||
D-глюкоза гликозидная связь
Подлинность
1.ИК-спектр препарата в области 4000 400 см 1 должен полностью совпадать со спектром стандарта.
2.ГФ Х. УФ-спектр раствора препарата в абсолютном спирте
вобласти 240 400 нм имеет максимум поглощения при 259 нм и
362,5 нм.
3.ВЭЖХ. Время удерживания препарата должно совпадать с временем удерживания стандартного образца рутина.
Химические реакции
1. ГФ Х. Реакция гидролиза гликозидных связей в кислой среде. При кипячении препарата с раствором HCl образуется глюкоза, ко-
24
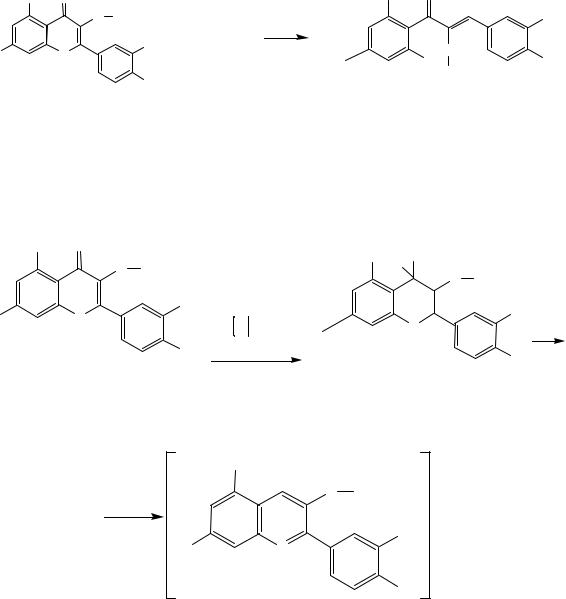
торую доказывают по реакции с реактивом Фелинга. Образуется красный осадок оксида меди (I).
2. ГФ Х. Реакция с гидроксидом натрия. Под действием NaOH происходит гидролиз пиранового кольца агликона кверцетина, образование халкона. Появляется желто-оранжевое окрашивание.
OH |
O |
|
|
ОН O |
|
|
|
О R |
|
|
ONa |
HO |
O |
ОН |
+ NaOH |
|
О |
|
НО |
ОН |
ONa |
||
|
|
|
|||
|
|
ОН |
|
|
R |
|
|
|
халкон (желто-оранжевое окрашивание) |
||
рутозид |
|
|
|
||
|
|
|
|
|
|
3. ГФ Х. Цианиновая реакция. Действуют на рутозид порошком магния и конц. HCl в спиртовой среде. Реакция основана на образовании окрашенных в красный цвет пирилиевых солей при восстановлении флавона водородом и дальнейшей дегидратации.
ОН |
O |
|
ОН |
Н |
ОН |
|
|
О R |
|||
|
|
|
|
О R |
|
|
|
|
|
|
|
НО |
О |
ОН |
|
|
ОН |
Н |
|
|
|||
|
|
О |
|||
|
|
НО |
|
||
|
|
ОН (Mg + HCl) |
|
|
|
|
|
|
|
ОН |
|
рутозид |
|
|
|
|
|
|
|
хроменол |
|
||
|
ОН |
|
HCl |
О |
R |
|
|
|
-H2O |
+ |
ОН Cl- |
НО |
О |
|
|
|
ОН |
цианин хлорид (пирилиевая соль) красное окрашивание
Нефармакопейные реакции
4. Реакция комплексообразования с хлоридом железа (III), на фенольные гидроксилы. Наблюдается темно-зеленое окрашивание, с солями свинца образуется оранжевый осадок.
25
5.Как фенол, рутозид вступает в реакцию азосочетания с диазотированной сульфаниловой кислотой. Соль диазония прибавляют
кщелочному раствору рутина. Образуется азокраситель темно-крас- ного цвета.
6.Реакция окислительной конденсации с формальдегидом в
конц. H2SO4. Образуется красно-оранжевое окрашивание. Реакция основана на наличии фенольных гидроксилов.
7.При кислотном гидролизе рутина кроме глюкозы образуется кверцетин (агликон). Его отделяют, сушат и определяют температу-
ру плавления +308 С. Метод можно использовать для гравиметрического определения рутозида.
Чистота
1.Примеси, нерастворимые в спирте.
2.Хлорофилл, пигменты, растворимые в эфире. Препарат взбалтывают с эфиром – эфир должен быть бесцветным.
3. Алкалоиды. Примеси алкалоидов определяют по реакции
спикриновой кислотой. Не должен выделяться осадок.
4.Кверцетин (не более 5 %). УФ-спектроскопия (измеряют поглощение раствора препарата при 375 и 362,5 нм и по формуле определяют содержание кверцетина). При хроматографии на бумаге допускается наличие одного пятна кверцетина, кроме пятна рутозида. Не должно быть пятен, обусловленных примесями алкалоидов, хлорофилла и т.д.
5.Потеря в весе при высушивании.
6.Сульфатная зола.
Количественное определение
ГФ X. Спектрофотометрия в УФ-области в абсолютном этаноле. Метод основан на определении поглощения препарата при 375 (D1) и 362,5 (D2) нм в кювете толщиной 1 см.
По закону Бугера Ламберта Бера оптическая плотность раствора препарата зависит от концентрации раствора.
А = E11см% l C(%),
где E11см% удельный показатель поглощения препарата, т.е. погло-
щение 1 %-го раствора в кювете толщиной 1 см; l – толщина кюветы; С(%) концентрация препарата в процентах (%).
26
Содержание рутина в % (Х) вычисляют по формуле
X D2 1000 , 325,5 a
где 325,5 – удельный показатель поглощения E11см% чистого рутина
(безводного) в абсолютном спирте при длине волны 362,5 нм; а – навеска, г.
Если отношение D1/D2 превышает 0,879, то содержание рутина вычисляют по формуле
X 14,60D2 13,18D1 . a
Содержание должно быть не менее 95,0 %.
Хранение
В хорошо укупоренной таре, в сухом месте, предохраняя от действия света.
Применение
Капилляроукрепляющее средство. Внутрь для профилактики и лечения авитаминоза, для лечения нарушения проницаемости сосудов и поражения капилляров.
27
Определение качества лекарственных средств из группы производных индола
Лекарственные препараты, производные индола
резерпин, индометацин, триптофан, серотонина адипинат, ондансетрон, трописетрон, суматриптана сукцинат, арбидол, винпоцетин.
Производные эрголина (алкалоиды спорыньи и их производные) – дигидроэрготамин, дигидроэргокристин, ницерголин, эргометрин, эрготамин, метилэргометрин, бромокриптин.
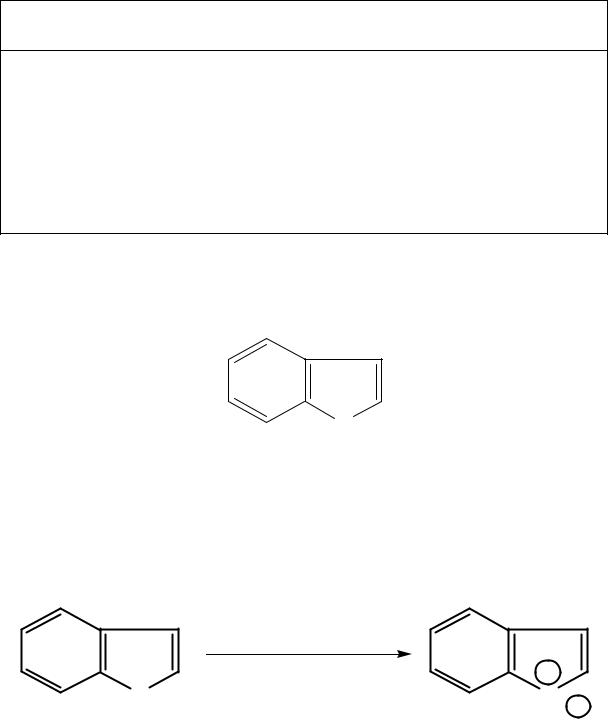
Индол – гетероциклическое ароматическое соединение, содержащее конденсированные системы пиррола и бензола.
N
H
Индол π-избыточная 10π-электронная ароматическая система, которая включает в себя неподеленную пару электронов атома азота. В связи с этим индол представляет собой слабую NH-кислоту (рКа = 16,97), способную образовывать соли, например:
|
NaNH2 в жидк. NH3 |
|
- |
N |
N |
H |
Na + |
1. Аналогично пирролу индол ацидофобен и очень чувствите-
лен к окислителям, поэтому выбор условий электрофильного замещения требует тех же самых предосторожностей, что и в случае пиррола.
28
