
- •Вопрос 16 Кинетика ферментативных реакций. Зависимость скорости ферментативных реакций от температуры, рН среды, концентрации фермента и субстрата. Уравнение Михаэлиса-Ментен, Кm.
- •1. Зависимость скорости ферментативной реакции от количества ферментов.
- •2. Зависимость скорости ферментативной реакции от температуры среды.
- •3. Зависимость скорости ферментативной реакции от рН среды.
- •4. Зависимость скорости ферментативной реакции от количества субстрата.
- •Выражается уравнением Михаэлиса-Ментена
- •Vmах и Km – кинетические характеристики эффективности фермента.
- •Вопрос 17 Кофакторы ферментов: ионы металлов их роль в ферментативном катализе. Коферменты как производные витаминов. Коферментные функции витаминов в6, рр и в2 на примере трансаминаз и дегидрогеназ.
- •1. Роль металлов в присоединении субстрата в активном центре фермента
- •2. Роль металлов в стабилизации третичной и четвертичной стр-ры фермента
- •3. Роль металлов в ферментативном катализе.
- •Коферментные функции витаминов в6, рр и в2 на примере трансаминаз и дегидрогеназ
- •Вопрос 18 Ингибирование ферментов: обратимое и необратимое; конкурентное и неконкурентное. Лекарственные препараты как ингибиторы ферментов
- •Специфические и неспецифическиеингибиторы
- •2. Необратимые ингибиторы ферментов как лекарственные препараты
- •Вопрос 20 Регуляция каталитической активности ферментов ковалентной модификацией путем фосфорилирования и дефосфорилирования.
- •Вопрос 21 Ассоциация и диссоциация протомеров на примере протеинкиназы а и ограниченный протеолиз при активации протеолитических ферментов как способы регуляции каталитической активности ферментов.
Специфические и неспецифическиеингибиторы
Специфические ингибиторы – вещества, блокирующие определённые группы активного центра ферментов. Ряд соединений легко вступает в реакции с определенными химическими группами. Если эти группы участвуют в катализе, то происходит полная инактивация фермента
Например: диизопропилфторфосфат (ДФФ) специфический ингибитор, т.к взаимодействует с ОН-гр. в остатке Серина в АУ, связывается с ней, происходит инактивация фермента
Монойодуксусная кислота легко вступает в реакции с SH-гр. остатков цистеина белков (но не явл. специфическим ингибитором, т.к. взаимод с любыми свободными
SH-гр, не только в АЦ)
2. Необратимые ингибиторы ферментов как лекарственные препараты
Аспирин обеспечивает фармакологическое действие за счёт ингибирования фермента циклооксигеназы, катализирующего реакцию образования простагландинов из арахидоновой кислоты. В результате хим. реакции ацетильный остаток аспирина присоединяется к свободной концевой NH2-группе одной из субъединиц циклооксигеназы Это вызывает снижение образования продуктов реакции простагландинов, которые обладают широким спектром биолог. функций, в т.ч. явл. медиаторами воспаления
Вопрос 19 Аллостерическая регуляция активности ферментов. Роль аллостерических ферментов в метаболизме клетки. Аллостерические эффекторы и ингибиторы. Особенности строения и функционирования аллостерических ферментов и их локализация в метаболических путях. Регуляция активности ферментов по принципу отрицательной обратной связи. Привести примеры.
Аллостерические ферменты – ферменты, активность которых регулируется не только количеством молекул субстрата, но и другими веществами (эффекторами)
Роль аллостерических ферментов в метаболизме клетки: ферменты
чрезвычайно быстро реагируют на малейшие изменения внутреннего состояния клетки.
Аллостерическая регуляция имеет большое значение в следующих ситуациях:
При анаболических процессах. Ингибирование конечным продуктом
метаболического пути и активация начальными метаболитами позволяют осуществлять регуляцию синтеза этих соединений;
При катаболических процессах. В случае накопления АТФ в клетке происходит
ингибирование метаболических путей, обеспечивающих синтез энергии. Субстраты при этом расходуются на реакции запасания резервных пит. веществ;
Для координации анаболических и катаболических путей. АТФ и АДФ –
аллостерические эффекторы, действующие как антагонисты;
Для координации параллельно протекающих и взаимосвязанных метаболических
путей (например, синтез пуриновых и пиримидиновых нуклеотидов, используемых для синтеза нуклеиновых кислот). Т.о., конечные продукты одного метаболического пути могут быть аллостерическими эффекторами другого метаболического пути.
Эффекторы – клеточные метаболиты часто именно того пути, регуляцию которого они осуществляют.
Ингибитор – эффектор, вызывающий снижение (ингибирование) активности ф.
Активатор – эффектор, вызывающий повышение (активацию) акт. активности ф.
Особенности строения и функционирования аллостерических ферментов:
1. Это олигомерные белки, состоящие из нескольких протомеров или
имеющие доменное строение. Они имеют аллостерический центр, пространственно удалённый от каталитического активного центра;
2. Эффекторы присоединяются к ферменту нековалентно в аллостерических
(регуляторных) центрах, которые так же, как и каталитические, могут проявлять различную специфичность по отношению к лигандам: она может быть абсолютной и групповой. Некоторые ферменты имеют несколько аллостерических центров, одни из которых специфичны к активаторам, другие – к ингибиторам.
3. Регуляторный протомер - протомер, на котором находится аллостерический
центр. Каталитический протомер – содержит активный центр, в котором проходит химическая реакция;
4. Аллостерические ферменты обладают свойством кооперативности:
взаимодействие аллостерического эффектора с аллостерическим центром вызывает последовательное кооперативное изменение конформации всех субъединиц, приводящее к изменению конформации активного центра и изменению сродства фермента к субстрату, что снижает или увеличивает каталитич. активность фермента
5. Регуляция аллостерических ферментов обратима: отсоединение эффектора от
регуляторной субъединицы восстанавливает исходную каталитическую активность фермента;
6. Аллостерические ф. катализируют ключевые р. данного метаболического пути.
Действие ингибитора:
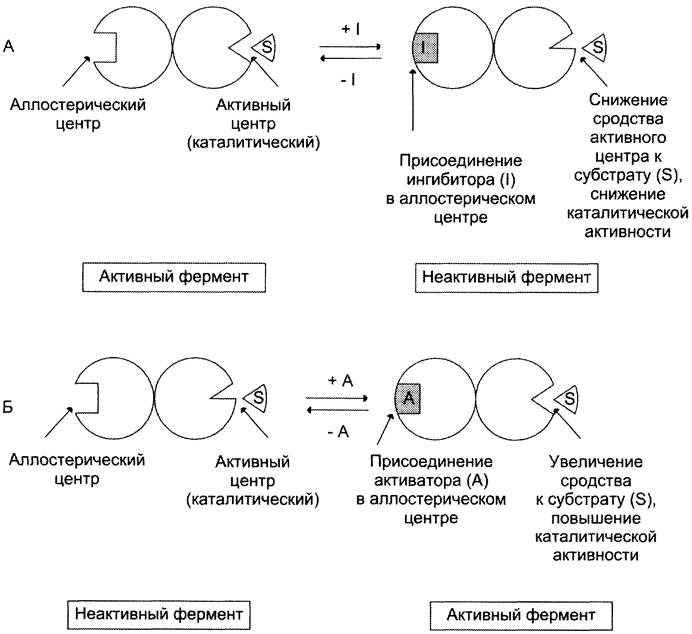
Действие активатора:
Виды аллостерическох эффектов: аллостерическими эффекторами часто служат
различные метаболиты.
Гетеротропная регуляция – субстрат не является эффектором. Чаще всего
Конечные продукты метаболит. пути – ингибиторы, а исходные – активаторы
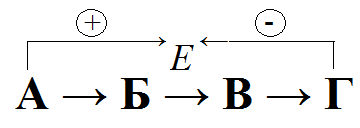
Гомотропная регуляция – субстрат является и эффектором
Эти ферменты имеют несколько центров связывания для субстрата, которые могут
выполнять двойную функцию: каталитическую и регуляторную. Аллостерические ферменты такого типа используются в ситуации, когда субстрат накапливается в избытке и должен быстро преобразоваться в продукт.
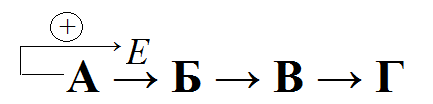
Локализация аллостерических ферментов в метаболическом пути: скорость
метаболических процессов зависит от конц. веществ, использующихся и образующихся в данной цепи реакций
Фермент, катализирующий превращение субстрата А в продукт В, имеет
аллостерический центр для отрицательного эффектора, которым служит конечный продукт метаболического пути
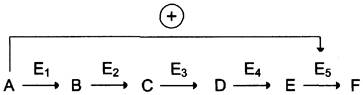
Отрицательная обратная связь (ретроингибирование) может происходить в тех
случаях, если концентрация F увеличивается (т.е. вещество F синтезируется быстрее, чем
расходуется), то им ингибируется активность одного из начальных ферментов.
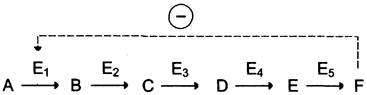
В центральных метаболических путях исх. вещества могут быть
активаторами ключевых ферментов метаболического пути. Как правило, при этом аллостерической активации подвергаются ферменты, катализирующие ключевые реакции заключительных этапов метаболического пути:
В качестве примера можно рассмотреть принципы регуляции гликолиза
Один из конечных продуктов распада глюкозы – молекула АТФ. При избытке в
клетке АТФ происходит ретроингибирование аллостерических ферментов фосфофруктокиназы и пируваткиназы.
При образовании большого количества фруктозо-1,6-бисфосфата наблюдают
аллостерическую активацию фермента пируваткиназы.

