
- •1. Иммунология, цели и задачи
- •2. Иммунная система организма, строение и функции
- •3. Иммунологическая реактивность
- •4. Формы проявление иммунологической реактивности
- •5. Роль тимуса в становлении иммунологической реактивности
- •6. Роль макрофагов и системы комплимента в иммунных реакциях
- •7. Понятие об антителах, их структуре и видах
- •8. Понятие об антигенах, их свойствах и видах
- •9. Тимусзависимые и независ. АГ
- •10. Первичный и вторичный гуморальный ответ
- •11. Понятие аллергия. Типы аллергических реакций
- •12. Экзо и эндогенные аллергены
- •13. Общая характеристика реакций гиперчувствительности немедленного типа
- •14. Виды и механизмы сенсебилизации
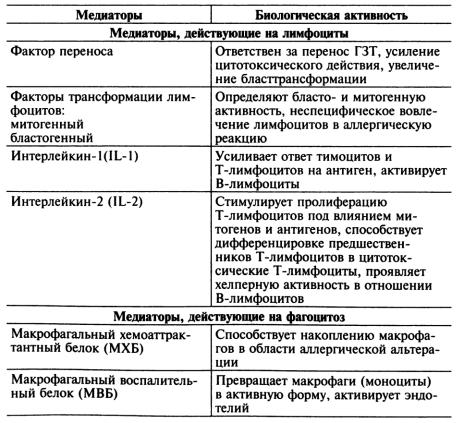
- •15. Стадии и медиаторы аллергии
- •III. Стадия клинических проявлений (патофизиологическая).
- •16. Понятие об анафилаксии, ее виды, механизмы развития. Атопия. Основные феномены местной анафилаксии.
- •17. Анафилактический шок: этиология, патогенез, основные проявления, принципы терапии.
- •18. Сывороточная болезнь: этиология, патогенез, основные проявления.
- •19. Специфическая и неспецифическая десенсибилизация, ее практическое значение.
- •20. Понятие о парааллергии, гетероаллергии и идиосинкразии. Причины и механизмы развития.
- •21. Общая характеристика, виды, этиология реакций гиперчувствительности замедленного типа (РГЗТ).
- •22. Роль Т-лимфоцитов и макрофагов в развитии РГЗТ.
- •23. Стадии РГЗТ. Медиаторы и гормоны клеточного иммунитета.
- •32. СПИД, этиология, патогенез.
- •31. Иммунодефицитные состояния, классификация, механизмы развития, примеры.
- •30. Современные представления об аутоиммунных процессах. Принцип выявления и терапии аутоиммунных заболеваний.
- •29. Пути гипосенсебилизации при РГЗТ. Понятие об иммуносупрессии.
- •28. Иммунологическая толерантность, виды и механизмы развития.
- •27. Причины и механизмы развития реакции трансплантата против реципиента. Виды реакций.
- •26. Механизм первичного и вторичного отторжения трансплантата. Феномен «белый трансплантат»
- •25. Представление о главном комплексе гистосовместимости.
- •24. Основы трансплантационного иммунитета. Виды трансплантатов.
22. Роль Т-лимфоцитов и макрофагов в развитии РГЗТ.
Макрофаг контактирует с антигеном и обрабатывает аг, а после в переработанном виде отдается Th1.
Th1 распознают антиген, а потом с помощью интерлейкинов запускают пролиферацию эффекторных Т-клеток воспаления с фенотипами CD4+ и CD8+, клеток памяти, которые позволяют сформировать быстрый иммунный ответ (если в организм вновь попадет тот же самый антиген).
23. Стадии РГЗТ. Медиаторы и гормоны клеточного иммунитета.
I.Стадия иммунных реакций.
1.антиген взаимодействует с макрофагом
2.макрофаг обрабатывает антиген
3.макрофаг предоставляет обработанный антиген Th1
4.Th1 распознает антиген и при помощи интерлейкинов запускает пролиферацию эффекторных Т-клеток воспаления с фенотипами CD4+ и CD8+, клеток памяти, которые позволяют сформировать быстрый иммунный ответ (если в организм вновь попадет тот же самый антиген).
5.пролиферацию лимфоцитов и их бластотрансформация
II.Стадия – патобиохимическая.
1.Антигенная стимуляция и бласттрансформация лимфоцитов сопровождается выделением медиаторов – цитокинов.
2.медиаторы действуют на клетки-мишени (макрофаги, нейтрофилы, лимфоциты, фибробласты, остеокласты, стволовые клетки костного мозга, опухолевые клетки)
3.биологический эффект медиаторов:
•изменение клеточной подвижности
•активация клеток, участвующие в воспалении
•регуляция кооперации иммунокмопетентных клеток
III.Стадия клинических проявлений.
•повышается проницаемость микроциркуляторного канала
•появление отека
•в воспалительном инфильтрате преобладает количество мононуклеарных клеток
•активируется свертывающая система крови

32. СПИД, этиология, патогенез.
СПИД (синдром приобретенной иммунной недостаточности)
Этиология: возбудитель болезни – вирус иммунодефицита человека (ВИЧ).
Патогенез: Ведущим звеном патогенеза является поражение лимфоцитов - Т-хелперов (Т4). ВИЧ проникает в клетки через рецепторы на их внешней мембране. С помощью обратной транскриптазы РНК генома ВИЧ входит в геном клетки-мишени, где представляет собой провирус. Таким образом возникает латентная инфекция.
Латентная инфекция способна превращаться в активную, что влечет болезнь. ВИЧ поражает также макрофаги и другие клетки, имеющие рецепторы, общие с Т4. В макрофагах вирус может сохраняться длительное время. С макрофагами,
преодолевают гематоэнцефалический барьер, ВИЧ попадает в спинной и головной мозг, вызывая их поражение. Вследствие разрушения Т4 изменяется соотношение хелперы / супрессоры - коэффициент Т4/Т8. Поражение
Т4 сопровождается повышением активности Т8, что характерно для иммунодефицита. Одновременно это вызывает
активацию В-лимфоцитов, увеличение количества иммунных комплексов.
Клиника (она скорее всего не нужна, но пусть будет, вдруг запомнишь:)
Условно можно выделить 4 стадии болезни:
1)мононуклеозоподобный синдром - острая инфекция;
2)генерализованную лимфаденопатию;
3)пре-СПИД;
4)стадию развернутой клиники.
Отдельно следует выделить бессимптомную форму ВИЧ-инфекции, которую можно обнаружить только с помощью специфических методов исследования.
Из учебника:
бессимптомная стадия:
1.в течение некоторого времени защитные системы организма сдерживаюит репродукцию возбудителя.
2.гуморальная реакция - синтез ат различных типов, не способные оказать протективный эффект.
3.клеточные реакции – либо блокируют репродукцию возбудителя, либо предовтращают проявления инфекции.
4.уменьшение количества циркулирующих CD4+-клеток.
31. Иммунодефицитные состояния, классификация, механизмы развития, примеры.
Иммунодефици́ты — нарушения иммунологической реактивности, обусловленные выпадением одного или нескольких компонентов иммунного аппарата или тесно взаимодействующих с ним неспецифических факторов.
Подразделяются по происхождению: первичные и вторичные по клинической выраженности: манифестные и минорные.
по локализации дефекта: дефициты антител, комбинированные дефициты Т- и В-клеток, дефекты NK-клеток, фагоцитоза, дефициты адгезивных молекул, комплемента.
Первичные иммунодефициты: обусловлены дефектами в отдельном гене или целых кластерах генов:

•нарушение образования иммуноглобулинов
-агаммаглобулинемия с дефицитом В-клеток
-общая вариабельная иммунная недостаточность
-агаммаглобулинемия с гипер-IgM
-селективный дефицит IgA
-транзиторная младенческая гипогаммаглобулинемия
•клеточные иммунодефициты: факторы такого рода иммунодефицитов:
-аплазия или дисплазия тимуса
-дефицит внутриклеточных ферментов
-дефицит синтеза цитокинов
-нарушение пролиферации Т-лимфоцитов
-дефицит CD45
-снижение экспрессии TCR
•комбинированные иммунодефициты
-синдром тяжелой комбинированной иммунной недостаточности – Х-сцепленное или аутосомно-рецессивное
генетическое заболевание, характеризующееся лимфоцитопенией, отсутсвтие антительного ответа принормальном содержании иммуноглобулинов и В-клеток.
-синдром Вискота-Олдрича – х-сцепленное заболевание. Проявляется экземой, возвратными инфекциями, тромбоцитопенией, снижение уровня Igm при увеличении содержания А, Е
•дефицит системы фагоцитов, механизм формирования:
-дефицит молекул адгезии
-утрата нейтрофилами способности к килингу
-нарушения хемотаксиса нейтрофилов
-нейтропения
•дефицит системы комплементов
Манифестные формы ПИБ проявляются на первом году жизни (ну или на втором) гнойничковыми поражениями кожи и слизистых оболочек, рецидивирующие инфекции
Вторичные иммуноднфициты: обусловлены количественным и качественным голоданием, эндокринопатиями, потерей иммунокомпетентных клеток при кровопотери, травмах, операциях, ионизирующей радиацией, гипертоксическими инфекциями (ВИЧ).


