
1547
.pdf
Cp i 2.
CV i
Задание к лабораторной работе
Данная программа предназначена для проведения лабораторных работ по термодинамике для студентов технических вузов. Она позволяет моделировать и получать количественные характеристики любого термодинамического (квазистатического) процесса. Также имеется возможность увидеть графики этих процессов при любой функциональной зависимости координатных осей.
Лабораторная установка представляет собой цилиндр с подвижным поршнем, заполненный двухатомным идеальным газом (молярную массу можно выбирать произвольно). Газ в установке можно нагревать (охлаждать). В программе предусмотрена возможность помещения установки в термостат. Для начала эксперимента необходимо ввести начальные значения необходимых вам параметров. Невведенные параметры вычисляются через известные или им присваиваются (в случае нехватки параметров для вычисления) значения параметров при нормальных условиях.
Изотермический процесс
1.Выберите в окне программы значение массы газа, степень свободы и молярную массу газа (рис.2). Занесите в табл.1 начальные параметры газа.
2.Для проведения с газом изотермического процесса необходимо рядом с буквой Т установить флажок.
3.Уменьшите объём газа перетаскиванием бегунка полосы прокрутки, расположенного справа от рисунка.
4.Занесите в табл. 1 конечные параметры газа, а также количество теплоты, сообщенное газу, изменение внутренней энергии
исовершенную газом работу.
5.Рассчитайте теплоемкость газа в данном процессе.
6.Зарисуйте графики изотермического процесса в координатах
рV, рТ, VT.
20
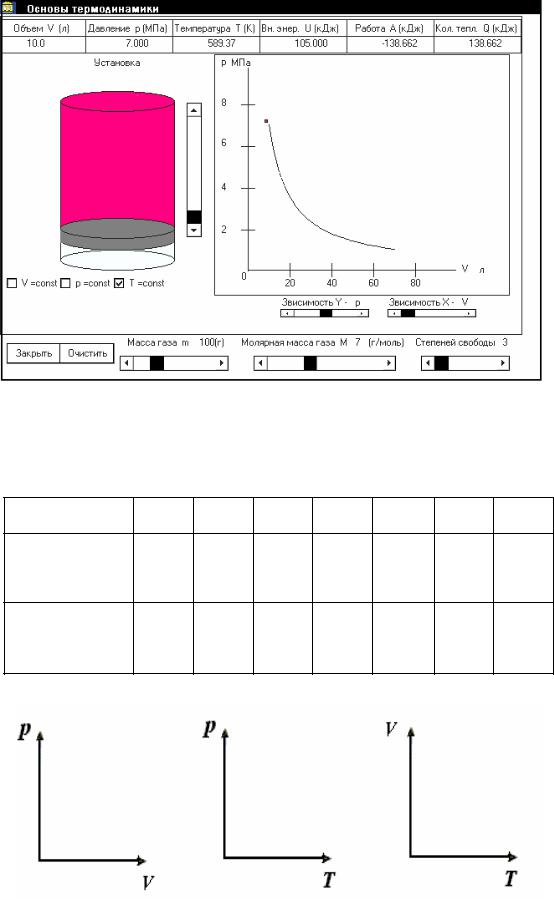
Рис.2. Рабочее окно программы
Таблица 1
Результаты измерений
Параметры |
V |
p |
T |
A |
∆U |
Q |
C |
В начале процесса
В конце процесса
21

Изохорный процесс
1.Выберите в окне программы значение массы газа, степень свободы и молярную массу газа (рис. 3). Занесите в табл.2 начальные параметры газа. Для проведения с газом изохорного процесса необходимо рядом с буквой V установить флажок.
2.Для проведения с газом изохорного процесса необходимо выбрать мощность нагревателя нажатием клавиши «Обогреватель».
3.Нажатием клавиши «Начать эксп.» нагрейте газ примерно на 100 К. Выключите нагреватель, нажав клавишу «Остановить эксп.»
4.Занесите в табл. 2 конечные параметры газа, а также количество теплоты, сообщенное газу, изменение внутренней энергии
исовершенную газом работу.
5.Рассчитайте теплоемкость газа в данном процессе.
6.Зарисуйте графики изохорного процесса в координатах pV, pT,
VT.
Таблица 2
Результаты измерений
Параметры |
V |
p |
T |
A |
∆U |
Q |
C |
В начале процесса
В конце процесса
Изобарный процесс
22

1.Для проведения с газом изобарного процесса необходимо рядом с буквой Р установить флажок. Выбор мощности нагревателя производится нажатием клавиши «Обогреватель».
2.Выберите в окне программы значение массы газа, степень свободы и молярную массу газа (см. рис. 3). Занесите в табл.3 начальные параметры газа.
3.Нажатием клавиши «Начать эксп.» нагрейте газ примерно на 100 К. Выключите нагреватель, нажав клавишу «Остановить эксп.»
4.Занесите в табл.3 конечные параметры газа, а также количество теплоты, сообщенное газу, изменение внутренней энергии и совершенную газом работу.
5.Рассчитайте теплоемкость газа в данном процессе.
6.Зарисуйте графики изобарного процесса в координатах pV, pT,
VT.
Таблица 3
Результаты измерений
Параметры |
V |
p |
T |
A |
∆U |
Q |
C |
В начале процесса
В конце процесса
Адиабатный процесс
1. Выберите в окне программы значение массы газа, степень свободы и молярную массу газа (см. рис. 3). Занесите в табл.4 начальные параметры газа.
23

2.Уменьшите объём газа перетаскиванием вниз бегунка полосы прокрутки, расположенного справа от рисунка.
3.Занесите в табл.4 конечные параметры газа, а также количество теплоты, сообщенной газу, изменение внутренней энергии и совершенную газом работу.
4.Рассчитайте теплоемкость газа в данном процессе.
5.Зарисуйте графики адиабатного процесса в координатах pV, pT,
VT.
Таблица 4
Результаты измерений
Параметры |
V |
p |
T |
A |
∆U |
Q |
C |
В начале процесса
В конце процесса
Проверка первого начала термодинамики
Вычислите работу, изменение внутренней энергии и количество теплоты с помощью теоретических формул и сравните с полученными значениями. Заполните табл. 5.
Найдите значение отношения Ср / CV.
24
|
|
Результаты измерений |
|
Таблица 5 |
|||||
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
Процесс |
А |
|
∆U |
|
Q |
А |
∆U |
|
Q |
|
|
|
|
|
|
|
|
|
|
|
|
Теоретические |
|
Экспериментальные |
|||||
Изохорный |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Изобарный |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Изотермический |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Адиабатный |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Заключение
При защите ЛР вы должны уметь зарисовать график любого из процессов в любых координатах, знать и уметь показать по формулам особенности поведения Q, A, U в любом из процессов, уметь подсчитать и сравнить теплоёмкости газов.
25
ЛАБОРАТОРНАЯ РАБОТА №3
Термодинамика циклических процессов
Цели работы: исследовать некоторые циклические процессы. Определить их энергетические характеристики, а также коэффициент полезного действия.
Основы теории
Особое место среди термодинамических процессов занимают циклические, т.е. такие, при которых состояние газа изменяется так, что первоначальное значение параметров реализуется снова. При этом подобные процессы могут быть проведены несколько раз, периодически.
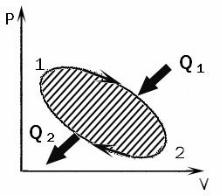
Очевидно, что графики подобных процессов должны иметь вид замкнутой кривой (рис.1). Рассмотрим некоторый циклический процесс в координатах pV. Первоначально газ находится в состоянии, соответствующем точке 1 на диаграмме, далее параметры газа изменяются, и его состояние описывается точкой 2. При этом, как видно из графика процесса, его объем увеличивается, т.е. газ будет совершать некоторую работу над внешними телами, обозначим A12. При возвращении газа из состояния 2 в состояние 1 объем его уменьшается, следовательно, в данном случае газ совершает работу против действия внешних сил, поэтому она отрицательна. Обозначим модуль данной работы А21. Как известно, работа, совершенная в процессе, равна площади под кривой процесса в координатах pV. Как видно из графика, площадь под кривой процесса 1–2 больше площади под кривой процесса 2–1, следовательно, A12 > А21 по модулю. Полная работа, совершенная по всему циклу, будет равна в данном случае:
Рис.1. Циклический процесс
26
А = А12 – A21 > 0. Графически она будет представляться площадью, ограниченной кривой циклического процесса. Получаем очень важное свойство циклического процесса: в результате проведения циклического процесса газ совершает некоторую механическую работу над внешними телами. Такой цикл называется прямым. При проведении процессов в противоположном направлении работа цикла отрицательна. Это означает, что над газом совершают работу внешние тела. Такой обратный цикл используется, например, в холодильных машинах.
По закону сохранения энергии работа не может совершаться просто так, при ее совершении должно происходить изменение энергии некоторых тел, т.е. должен быть некоторый источник энергии. В данном случае энергия дается системе при проведении процесса 1–2 в виде количества теплоты Q1. Рассмотрим теперь процесс 2–1. Так как проведение его невозможно без передачи системой внешним телам некоторой энергии, то он будет сопровождаться выделением системой количества теплоты Q2.
Согласно закону сохранения энергии (1-е начало), эти величины будут связаны следующим соотношением:
A = Q1 – Q2. (1)
Каждый циклический процесс можно также характеризовать
коэффициентом полезного действия (КПД). По его определению он должен быть равен отношению полезной работы, совершенной в циклическом процессе, к количеству теплоты, переданной системе:
|
A |
, или |
|
Q1 Q2 |
. |
(2) |
|
|
|||||
|
Q1 |
|
Q1 |
|
||
На практике циклические |
процессы используются в |
так |
||||
называемых тепловых машинах, которые состоят из нагревателя, передающего системе количество теплоты Q1, рабочего тела – некоторого газа, совершающего работу А, и холодильника, которому
передается количество теплоты Q2 (рис. 2). |
действия при |
||
Максимальным коэффициентом |
полезного |
||
заданных |
температурах нагревателя |
и холодильника обладают |
|
машины, работающие по циклу Карно, который представлен на рис. 3.
Процесс 1–2 представляет собой изотермическое расширение газа, процесс 2–3 – адиабатическое расширение, процесс 3–4 – изотермическое сжатие и, наконец, процесс 4–1 – адиабатическое сжатие.
27

Рис.2. Схема тепловой машины
Так как для адиабатического процесса Q = 0, то Q1 равно количеству теплоты, полученному системой при изотермическом расширении, a Q2 равно количеству теплоты, отданному системой при изотермическом сжатии. Обозначим температуру первого изотермического процесса (и нагревателя) Т1, а температуру второго изотермического процесса (и холодильника) Т2, тогда:
Q |
m |
RT ln |
V2 |
, а |
Q |
m |
RT ln |
V3 |
. |
|
|
|
|
||||||||
|
|
|
|
|||||||
1 |
1 |
V |
2 |
2 |
V |
|||||
|
|
|
1 |
|
|
|
|
4 |
|
|
Рис. 3. Цикл Карно
28

Подставив данные соотношения в формулу (2), получим для коэффициента полезного действия цикла Карно
|
T1 T2 |
. |
(3) |
|
|||
|
T1 |
|
|
При анализе цикла Карно удобно использовать представление процесса в координатах температура – энтропия (TS). В этом случае график цикла Карно представляет собой прямоугольник. Энтропия – это термодинамическая функция состояния, определяемая соотношением
dS Q . T
Задание к лабораторной работе
Упражнение 1. Цикл Карно
1. Нажатием кнопки «Выбрать процесс» в раскрывающемся списке выберите пункт «Цикл Карно». Задайте начальное и конечное значение температуры газа. Выберите оси координат.
2.Проведите изотермический процесс. Для этого кликните левой клавишей «мыши» на кнопке «Начать эксперимент».
Запишите количество теплоты, переданное газу, и работу им совершенную.
3.Проведите адиабатический процесс, для этого кликните левой клавишей «мыши» на кнопке «Продолжить эксперимент».
Запишите количество теплоты, переданное газу, и работу им совершенную.
4.Проведите изотермический процесс, для этого кликните левой клавишей «мыши» на кнопке «Продолжить эксперимент».
Запишите количество теплоты, переданное газу, работу им совершенную.
5.Проведите адиабатический процесс, для этого кликните левой клавишей «мыши» на кнопке «Продолжить эксперимент».
Запишите количество теплоты, переданное газу, и работу им совершенную.
6.Подсчитайте по формулам (2) и (3) КПД цикла, сравните их значения.
7.Занесите все данные в табл. 1.
29
