
Белозеров В.И. Учебное пособие по курсу Техническая термодинамика (оригинал)
.pdf
|
|
|
|
§ wS1 |
· |
|
|
|
|
|
|
|
|
|
|
|
|
|
§ wS1 · |
|
|
|
|
|
|
|
|
|
|
|
|
§ wS1 |
· |
dG1. |
|
|||||||||||||||||||||||||
dS1 |
¨ |
|
|
|
|
|
¸ |
|
|
|
|
dU1 ¨ |
|
|
|
|
|
|
|
¸ |
|
|
|
dV1 |
¨ |
|
|
|
|
¸ |
(9.4.1) |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
© wU1 ¹V1 ,G1 |
|
|
|
|
|
|
|
|
|
© wV1 ¹U1 ,G1 |
|
|
|
|
|
|
|
|
|
© wG1 ¹U1 ,V1 |
|
|||||||||||||||||||||||||||||||||||
Åñëè |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§ wS |
· |
|
|
|
|
|
1 |
|
§ wS |
· |
|
|
|
|
|
|
|
|
|
|
|
|
P |
§ wS |
|
|
· |
|
|
|
|
M |
|
|||||||||||||||||||||||||||
¨ |
1 |
|
¸ |
|
|
|
|
|
|
|
|
|
; ¨ |
|
1 |
¸ |
|
|
|
|
|
|
|
|
|
|
|
1 |
; ¨ |
|
1 |
|
|
¸ |
|
|
|
|
1 |
, |
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
© wU1 ¹V1 ,G1 |
|
T1 |
© wV1 ¹U1 ,G1 |
|
T1 |
|
© wG1 ¹U1 ,V1 |
|
T1 |
|
||||||||||||||||||||||||||||||||||||||||||||||||||
то в соответствии с этим |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
dS |
|
|
|
1 |
|
dU |
1 |
|
|
P1 |
|
|
dV |
|
M1 |
dG . |
|
|
|
(9.4.2) |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
T1 |
|
|
|
|
|
|
|
T1 |
|
|
1 |
|
|
|
|
T1 |
|
|
1 |
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
Аналогично для второй фазы: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
dS |
2 |
|
|
|
1 |
dU |
2 |
|
P2 |
|
dV |
|
M2 |
|
|
dG . |
|
|
|
(9.4.3) |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
T2 |
|
|
|
|
|
|
|
|
T2 |
|
|
2 |
|
|
|
|
|
T2 |
|
|
|
|
|
|
2 |
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
Подставляя (9.4.2), (9.4.3) в (*) и учитывая (а), получим |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
§ 1 |
|
|
1 · |
|
|
|
|
|
§ P |
P |
· |
|
|
|
|
|
§ M |
|
|
|
|
M |
· |
|
|
|
|
||||||||||||||||||||||||||||||||
|
¨ |
|
|
|
|
|
|
¸dU1 |
¨ |
|
1 |
|
|
|
|
2 |
¸dV1 ¨ |
1 |
|
|
|
|
|
2 |
¸dG1 |
0. |
(9.4.4) |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
©T1 |
|
T2 ¹ |
|
|
|
|
|
©T1 |
|
|
|
|
T2 ¹ |
|
|
© |
T1 |
|
|
|
|
T2 ¹ |
|
|
|
|
|||||||||||||||||||||||||||||||||
Поскольку дифференциалы dU, dV, dG взаимно независимы, то |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
1 |
|
1 |
0, |
|
|
|
P1 |
|
|
|
P2 |
|
0, |
|
M1 |
|
M2 |
|
0 |
|
|
(9.4.5) |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
T1 |
|
T2 |
|
|
|
|
|
|
|
|
T1 |
|
|
|
T2 |
|
|
|
|
T1 |
|
|
|
T2 |
|
|
|
|
||||||||||||||||||||||||||
èëè |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
T |
|
; P |
|
|
|
|
P |
; M |
|
|
|
|
M |
. |
|
|
|
|
|
|
|
|
|
|
(9.4.6) |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
2 |
|
|
1 |
|
2 |
|
|
1 |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
Таким образом, если две (и более) фазы находятся в равновесии, то температуры, давления и химические потенциалы этих фаз равны между собой.
Химическим потенциалом M вещества называется удельный изо- барно-изотермический потенциал
M h TS, Äæ .
êã
9.3. Условия устойчивости и равновесия в
изолированной однородной системе
Термодинамический анализ позволяет показать, что из соображений термодинамической устойчивости системы для любого вещества должны выполняться условия
C > 0, |
(9.3.1) |
v |
|
§ wP ·
¨ ¸ 0, (9.3.2)
© wV ¹T
т.е., во-первых, изохорная теплоемкость C всегда положительна и,
v
во-вторых, в изотермическом процессе увеличение давления всегда приводит к уменьшению объема вещества. Условие (9.3.1) называется условием термической устойчивости, а условие (9.3.2) – условием механической устойчивости.
Условия (9.3.1) и (9.3.2) можно объяснить так называемым принципом смещения равновесия (принцип Ле Шателье–Брауна), смысл которого заключается в том, что если система, находившаяся в равновесии, выводится из него, соответствующие параметры системы изменяются таким образом, чтобы система вернулась в состояние равновесия.
Рассмотрим условие равновесия в изолированной термодинамической системе.
Мысленно разделим эту систему на две подсистемы 1 и 2 и выясним, при каких условиях существует равновесие между этими подсистемами (рис. 9.3.1).
Поскольку система изолированная, то
V= const и U = const. Можно пред-
ставить себе такой бесконечно малый про-
Ðèñ. 9.3.1
124 |
121 |
123 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
1 |
1 |
|
|
1 |
|
)ивсоответствиисэтим |
G |
, |
,U |
f(V |
= |
ДляпервойфазыS |
||||||
|
|
|
.0 |
|
2 |
|
|
1 |
|
ñèñò |
|
|
|
|
|
|
|
|
dSdS |
dS |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
òî |
|
|
2 |
|
1 |
|
ñèñò |
|
|
ñèñò |
||||
(*) |
, |
|
|
|
|
|
è |
0 |
|
|
|||
|
S |
|
S |
|
|
S |
|
|
dS |
||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Поскольку |
|
2 |
|
1 |
|
|
|
2 |
|
|
1 |
2 |
|
1 |
(à). dU – = dU , dG – = dG , dV – = dV
|
|
|
|
гдеиндексами1и2обозначеныфазы,отсюда |
|||||||||||||||||||
|
2 |
1 |
|
ñèñò |
2 |
|
|
|
1 |
|
|
ñèñò |
|
2 |
|
|
1 |
ñèñò |
|
||||
|
, |
=U+U |
;U |
=G+G |
G |
=V+V; |
V |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
нымпаром,следовательно, |
||||||
теплоизолированнымистенкамизаполненаводой,адругая–водя- |
|||||||||||||||||||||||
Пример.Одначастьсосудапостоянногообъемасидеально |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ñèñò |
ñèñò |
|
–полноеколичествовеществав.системе) |
=const(G |
U |
|||||||||||||||||||||
|
ñèñò |
|
|
ñèñò |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
=const, |
=const,G |
Рассматриваетсясистема,длякоторойV |
|||||||||||||||||||||
|
|
|
|
|
ствотеперьнаходитсявразличных.фазах |
||||||||||||||||||
отпредыдущегослучая(двеподсистемы)состоитвтом,чтовеще- |
|||||||||||||||||||||||
более).фазНайдемобщиеусловияфазового.равновесияОтличие |
|||||||||||||||||||||||
Рассмотримизолированныесистемы,состоящиеиздвух(или |
|||||||||||||||||||||||
|
.4.9Условияфазовогоравновесия |
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тях.системы |
|
рованнойсистемевсостоянииравновесияодинаковывовсехчас- |
|||||||||||||||||||||||
Итак,мыпришликвыводу,чтотемпературыидавлениявизоли- |
|||||||||||||||||||||||
|
|
|
|
|
2 |
|
|
|
|
1 |
|
2 |
1 |
|
|
|
|
|
|
||||
|
|
|
|
|
|
P=P. |
, |
|
=T |
T |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.å.ò |
|
|
|
|
|
2 |
|
|
|
|
1 |
|
|
|
|
|
2 |
|
1 |
|
|
|
||
|
|
|
|
0, |
|
T |
|
|
T |
|
|
0 |
T |
|
|
T |
|
|
|
||||
|
|
|
|
|
2 |
1 |
|
è |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
1 |
|
|
|
||
|
|
|
|
|
|
P |
|
|
P |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тогда |
|
ренняяэнергиясистемы,аобъемостаетсяпостоянныминаоборот, |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
1 |
|
|
|
|
dVнезависимы,.е.тможетменятьсявнут- |
ДифференциалыdUи |
||||||||||||||||||||||
|
|
|
|
≠ |
2 |
|
|
|
1 |
|
♥ |
|
|
≠ |
2 |
|
1 |
♥ |
|
|
|||
|
|
|
1 |
|
T |
|
|
T |
|
|
1 |
|
|
T |
|
|
T |
|
|
|
|||
.3.(97) |
|
.0 |
÷dV |
2 |
|
|
1 |
|
♦ |
|
÷dU |
1 |
|
1 |
♦ |
|
|
||||||
|
|
|
|
∙ |
P |
|
♣P |
|
|
∙ |
|
♣ |
|
|
|||||||||
122
|
|
|
|
|
|
|
|
|
|
|
|
|
èëè |
|
|
|
|
2 |
|
|
|
2 |
|
1 |
|
|
|
1 |
|
|
0 |
2 |
T |
|
2 |
|
T |
1 |
T |
|
1 |
|
T |
|
.3.(96) |
dV |
2 |
|
|
dU |
1 |
dV |
1 |
|
|
dU |
1 |
|
|
|
|
|
P |
|
|
|
|
P |
|
|
|
|
||
Всоответствиисуравнением.3.(94)получаем |
||||||||||||||||||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
2 |
|
|
|
|
|
T |
|
2 |
|
|
T |
2 |
|
|||||||
|
|
dV. |
|
2 |
|
|
|
|
|
|
|
dU |
1 |
|
|
|
dS |
|||||
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дляподсистемы2 |
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
1 |
|
|
|
|
|||
|
|
1 |
|
|
|
|
|
T |
|
|
1 |
|
|
T |
1 |
|
||||||
|
|
, |
dV |
|
1 |
|
|
|
|
|
|
dU |
1 |
|
|
dS |
||||||
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
Такимобразом,дляподсистемы1 |
|||||||||||
.3.(95) |
|
|
|
|
|
T |
|
|
|
|
|
|
T |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dV. |
|
|
|
|
dU |
|
|
dS |
|
||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
P |
|
|
|
|
|
|
|
1 |
|
|
|
|
|
||||
ИзуравненияTdS=dU+PdVследует,что |
||||||||||||||||||||||
|
.0 |
2 |
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
ñèñò |
dS |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
.3.(94) |
|
dSdS |
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
авсоответствиис.3.(93) |
|
|
|
|
, |
2 |
S |
|
1 |
|
|
ñèñò |
S |
|
|||||||||
|
|
|
|
|
|
|
S |
|
|
|
|
|||||||||||
Энтропияявляетсяаддитивнойвеличинойи |
||||||||||||||||||||||
|
|
|
|
|
|
|
0. |
|
|
|
ñèñò |
|
|
|
|
|
||||||
.3.(93) |
|
|
|
|
|
|
|
|
|
|
|
dS |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
янное(максимальное)значение,.е.т |
|||||||||
термодинамическогоравновесияэнтропиясистемысохраняетпосто- |
||||||||||||||||||||||
Ранеемыустановили,чтовизолированнойсистемевсостоянии |
||||||||||||||||||||||
. |
2 |
|
|
|
|
|
|
|
1 |
|
|
|
|
|
è |
2 |
|
|
|
1 |
||
|
dU |
|
|
|
|
|
|
|
dU |
|
dV |
dV |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
янноезначение,поэтому |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
иdU.Объемивнутренняяэнергиявсейсистемысохраняютпосто- |
||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
навеличинуdUидлявторойподсистемы–соответственнонаdV |
||||||||||||||||||||||
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
системыобъемменяетсянавеличинуdV,авнутренняяэнергия– |
||||||||||||||||||||||
каждойизподсистемостается.неизменным)Пустьдляпервойпод- |
||||||||||||||||||||||
систем,либотоидругоевместе(приэтомколичествовеществав |
||||||||||||||||||||||
объемкаждойизподсистем,либоменяетсявнутренняяэнергияпод- |
||||||||||||||||||||||
цессвнутриизолированнойсистемы,прикоторомлибоменяется |
||||||||||||||||||||||

Μ1 P,T v1dP S1dT Μ2 P,T v2dP S2dT. (9.6.4)
Учитывая, что Μ (P, T) = Μ (P, T), уравнение кривой фазового пе-
12
рехода (уравнение Клапейрона–Клаузиуса) принимает вид
dP |
|
S2 |
S1 |
. |
(9.6.5) |
|
|
|
|
|
|
dT |
|
v2 |
v1 |
|
|
Это уравнение однозначно связывает наклон линии фазового перехода на PT-диаграмме с величинами разности энтропий сосуще-
ствующих фаз (S и S ) и разности удельных объемов этих фаз (v и v ).
2 1 2 1
Уравнение второго закона термодинамики для обратимых процессов
TdS dh vdP
применительно к данному случаю (для P=const), следующее:
TdS dh.
Интегрируя это соотношение между точками 1 и 2, получаем
T S2 S1 h2 h1 . |
(9.6.6) |
Применительно к процессу фазового перехода разность энтальпий сосуществующих фаз представляет собой теплоту фазового перехода, т.е. количество тепла, которое поглощается (или выделяет-
ся) 1 кг вещества в процессе фазового перехода. |
|
||
Обозначая теплоту фазового перехода через r = h |
– h , получа- |
||
|
2 |
1 |
|
åì èç (9.6.6) |
|
|
|
S2 S1 |
r |
|
|
|
. |
|
|
|
|
||
|
T |
|
|
Подставляя это значение в уравнение (9.6.5), получаем уравне-
ние Клапейрона-Клаузиуса в следующем виде:
dP |
|
r |
|
. |
|
|
|
|
|
|
|
(9.6.7) |
|
dT |
|
T v |
v |
|
||
|
2 |
1 |
|
|
|
|
Фазовый переход «жидкость – пар»
Применительно к фазовому переходу «жидкость – пар» уравнение (9.6.7) можно записать таким образом:
9.5. Фазовые переходы
Фазовым переходом называется переход вещества из одной фазы в другую, сосуществующую с первой. Говоря о фазах чистого вещества, обычно имеют в виду агрегатные состояния вещества и поэтому говорят о газовой, жидкой и твердой фазах. Однако понятие фазы несколько уже понятия агрегатного состояния: некоторые вещества (например, лед) в твердом состоянии имеют несколько фаз. Тем не менее, мы в дальнейшем будем подразумевать под фазовым переходом переход вещества из одного агрегатного состояния в другое.
Фазовый переход из твердой фазы в газообразную, происходящий при очень низких давлениях, называется сублимацией. Из сказанного очевидно, что теплота сублимации должна быть больше, чем теплота плавления или теплота парообразования. При фазовом переходе резко изменяется плотность вещества, в случаях парообразования и сублимации плотность газовой фазы всегда меньше, чем плотность жидкой или твердой фаз.
Принята следующая классификация точек фазового перехода: точка перехода «жидкость–пар» называется точкой кипения (она же точка конденсации), точка перехода «твердое тело–жидкость» называется точкой плавления (она же точка затвердевания), а точка перехода «твердое тело–пар» называется точкой сублимации.
С повышением температуры в веществе происходит некоторое дробление молекулярных ассоциаций (в твердой фазе – разрыхление кристаллов). Этот процесс заметно ускоряется вблизи точек перехода, в которых изменение молекулярной структуры происходит скач- кообразно.
Твердые вещества могут образовывать не одну, а несколько кристаллических модификаций (например, лед), каждая из которых существует при определенных параметрах состояния.
При анализе фазовых равновесий и процессов фазовых переходов важную роль играет так называемое правило фаз Гиббса. Оно устанавливает зависимость между числом независимых переменных, определяющих состояние термодинамической системы, находящейся в равновесии (эти независимые переменные часто называют степенями свободы системы), числом фаз и числом компонентов системы.
128 |
125 |

127 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1),.6.(9получаем |
||||
Подставляяэтовыражениевлевуюиправуючастиуравнения |
||||||||||||||||||||||||||||||
.6.(93) |
vdPSdT. |
MP,T |
|
MPdP,TdT |
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
следующимобразом: |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
©wT¹ |
|
|
T |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S, |
|
|
v |
©wP¹ |
|||||||
торяд.6.(92)можетбытьзаписан |
|
¸ |
|
¨ |
è |
¸ |
|
.ê.ò¨ |
||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§wM· |
|
|
§wM· |
||||
|
|
P |
©wT¹ |
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
dT; |
|
dP |
©wP¹ |
MP,T |
MPdP,TdT |
|
|||||||||||||||||||||||
.6.(92) |
|
¸ |
|
¨ |
¸ |
|
|
|
|
|
¨ |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
§wM· |
|
§wM· |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
рядМаклорена(используемтолькопервоеслагаемоеразложения): |
||||||||||||||||||||||||||||||
)можетбытьразложенав |
dT |
+ |
dPT |
+ |
P |
( |
M |
Очевидно,чтофункция |
||||||||||||||||||||||
|
|
|
|
|
, |
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
PdP,TdT. |
2 |
M |
|
TdT |
|
|
1 |
|
|
|
|
||||||||||||||||||
.6.(91) |
|
|
|
PdP, |
M |
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
равновесии,тоипотенциалыфазбудутравны: |
||||||||||||||||||||||||
ние–навеличинуdP.Еслифазыиприновыхусловияхостаютсяв |
||||||||||||||||||||||||||||||
ИзменимтемпературувкаждойизфазнавеличинуdT,адавле- |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
P,T. |
2 |
M |
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
MP,T |
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
ленииPитемпературеT;условиеравновесия |
||||||||||||||||||||||||
Рассмотримдвефазы(1и2),находящиесявравновесиипридав- |
||||||||||||||||||||||||||||||
|
.6.9УравнениеКлаузиуса–Клапейрона |
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
положительный,такиотрицательный.наклон |
||||||||||||||||||||||||
.шаетсяЛинияплавлениядляразличныхвеществможетиметькак |
||||||||||||||||||||||||||||||
ниятемпературафазовогоперехода(сублимацияикипение)повы- |
||||||||||||||||||||||||||||||
имеютположительный.наклонЭтоозначает,чтосростомдавле- |
||||||||||||||||||||||||||||||
Линиясублимацииилиниянасыщения,каквидноиз.рис1,.5.9 |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
критической.точкой |
||||||
называемой |
.фер)ЛиниянасыщенияОКоканчиваетсявточкеК, |
|||||||||||||||||||||||||||||
присверхвысокихдавлениях(порядкадесяткаисотентысячатмос- |
||||||||||||||||||||||||||||||
уходитвверх,всторонубольшихдавлений,онанеоканчиваетсядаже |
||||||||||||||||||||||||||||||
должаетсявнизвсторонунизких.температурКриваяплавленияОА |
||||||||||||||||||||||||||||||
пературе0,01°Сидавлению610,8.ПаКриваясублимацииОВпро- |
||||||||||||||||||||||||||||||
агрегатных.состоянияхДляводытройнаяточкасоответствуеттем- |
||||||||||||||||||||||||||||||
етсобойтройнуюточку,вкоторойвеществососуществуетвтрех |
||||||||||||||||||||||||||||||
.нияТочкаОпредставлявой(илилинией)насыще- обычноназываетсякри- .стоянияКриваякипения КО–областьжидкогосо- амеждулиниямиАОи ногосостояниявещества, КОВ–областьгазообраз- ства,справаотлинии твердогосостояниявещерасположенаобласть СлеваотлинииАОВ
|
|
|
|
|
126 |
|
|
.Ðèñ1.5.9 |
|
||
T |
|
ôàçà |
|
сублим |
|
|
|
|
|
B |
|
|
|
|
|
|
|
|
|
Газообразная |
|
Ê |
|
|
|
|
|
ацииривая |
|
|
|
|
|
O |
|
|
(конденсация) |
|
|
|
|
|
|
Кипение |
|
(затвердевание) |
|
|
|
|
|
||
P=const |
|
D |
|
Плавление |
|
|
|
|
|
|
|
|
|
ôàçà |
C |
Твердаяфаза |
|
|
|
Жидкая |
|
|
|
|
K |
A |
|
|
P |
|
|
|
|
|
|
|
|
|
|
минанейкривымифазовых.переходов |
|||||
Hа.рис1.5.9изображенаPT-диаграммавеществаснанесенны- |
|||||||||
рахTидавленииP,характерныхдляданногоконкретного.вещества |
|||||||||
ходитьсявравновесиилишьпривполнеопределенныхтемперату- |
|||||||||
Этоозначает,чтоводнокомпонентнойсистеметрифазымогутна- |
|||||||||
=.0 |
\ |
Длятрехфазнойсистемыr=3ичислостепенейсвободы |
|||||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
рамфазового.перехода |
||||
еслинанестисостояния,соответствующиедавлениямитемперату- |
|||||||||
ЛиниюфазовогопереходаможноизобразитьнаPT-диаграмме, |
|||||||||
|
|
|
системы,например,давлениеPилитемператураT. |
||||||
.е.тлюбойпараметропределяетравновесноесостояниекаждойфазы |
|||||||||
=1, |
\ |
Длядвухфазнойсистемы,находящейсявравновесии,r=2, |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
темыбудутопределены.однозначно |
|||||
извольнозадать,например,PиT,товсеостальныепараметрысис- |
|||||||||
=.2Этоозначает,чтоеслидлятакойсистемыпро- |
\ |
нейсвободы |
|||||||
|
|
|
|
|
|
|
|
|
|
Длячистыхвеществводнофазнойсистеме(r=1)числостепе- |
|||||||||
.5.(92) |
|
3r. |
\ |
|
|
|
|
||
|
|
|
|
|
|
|
|
||
|
|
|
Длячистыхвеществ(однокомпонентнаясистема,n=1) |
||||||
|
|
|
|
|
|
|
.намике |
||
компонентов,играетособенноважнуюрольвхимическойтермоди- |
|||||||||
Правилофаз,справедливоедлясистемслюбымколичеством |
|||||||||
|
|
|
числокомпонентовсистемы;r–числофазв.системе |
||||||
–числостепенейсвободытермодинамическойсистемы;n– |
\ |
ãäå |
|||||||
|
|
|
|
nr2 |
\ |
|
|
|
|
.5.(91) |
, |
|
|
|
|
||||
|
|
|
Правилофазформулируетсяследующимобразом: |
||||||

щенному пару (M ). Точка S, где кривые 1 и 2 пересекаются и имеет
ï
место равенство M = M , есть точка фазового равновесия данного
12
вещества (давление P).
Очевидно, что выражение для изобарно-изотермического потенциала двухфазной системы в соответствии с правилом аддитивности можно представить в виде
)ñèñò MæGæ MïGï . |
(9.7.1) |
Рассмотрим систему, состоящую из двух фаз, находящихся при одном и том же давлении и одинаковой температуре (точки a и b на
изобаре P ). Если система не находится в состоянии равновесия, то
æ
в этой изобарно-изотермической системе возможен процесс, который приводит к изменению потенциала системы Ф. Поскольку P и T
постоянны, то M и M сохраняются постоянными и dM = 0, dM = 0.
Следовательно, изменение величины ) может происходить только
ñèñò
за счет изменения G и G и тогда получаем
æï
d) |
Μ dG |
Μ dG . |
(9.7.2) |
|
ñèñò |
æ æ ï |
ï |
|
|
В то же время известно, что G |
= G + G = const è |
|
||
|
ñèñò |
æ |
ï |
|
dG |
dG , |
|
|
|
|
æ |
ï |
|
|
тогда уравнение (9.7.2) принимает вид |
|
|
||
d)ñèñò |
Mï |
Mæ dGï . |
(9.7.3) |
|
В процессе установления равновесия в изобарно-изотермической системе потенциал Ф всегда уменьшается, стремясь к минимуму,
т.е. ) < 0, и знак у дифференциала dG определяется знаком раз-
ñèñò ï
ности (M – M ):
ïæ
• если M > M , то dG < 0, следовательно, устойчивым состояни-
ï |
æ |
ï |
ем системы является жидкое состояние; |
||
• åñëè M |
< M , то dG > 0 и устойчивым состоянием системы |
|
ïæ ï
является парообразное состояние.
Вышесказанное позволяет сделать однозначный вывод о том, что из двух фаз устойчивой при данных P и T является та фаза, у которой химический потенциал имеет меньшее значение.
dPS |
|
r |
, |
(9.6.8) |
dT |
|
T vcc vc |
где r – теплота парообразования; vs – удельный объем пара на линии насыщения; vc– удельный объем жидкости на линии насыщения;
P – равновесное давление в точках фазового перехода «жидкость –
S
ïàð».
Поскольку vcc > vc, то из уравнения (9.6.8) следует, что dPS >0, ò.å. dT
с ростом температуры давление насыщения увеличивается.
Если давление пара мало, то vs >> vc и поэтому (vs – vc) можно заменить величиной vs. Кроме того, если давление пара мало, то этот пар можно рассматривать как идеальный газ, т.е.
vcc RT .
PS
Подставляя это выражение в уравнение (9.6.8) и выполняя несложные преобразования, получаем
|
d ln PS |
|
|
r |
, |
|
|
|
dT |
|
RT 2 |
|
|||
откуда |
|
|
|
|
|
|
|
ln PS ³ |
r |
|
dT const. |
(9.6.9) |
|||
RT |
2 |
||||||
При низких давлениях величина теплоты парообразования практически не зависит от температуры, тогда в уравнении (9.6.9) r можно вынести за интеграл:
ln P |
r |
const. |
(9.6.10) |
S |
RT |
|
Обычно константу интегрирования определяют по величине тем-
пературы нормального кипения T |
(ïðè P = 760 ìì ðò. ñò.). Èç óðàâ- |
H.Ê |
S |
нения (9.6.10) |
|
|
PS |
|
r § |
1 |
|
1 · |
|
||
ln |
|
|
|
¨ |
|
|
¸, |
(9.6.11) |
|
P |
|
R |
T |
T |
|||||
|
|
© |
|
¹ |
|
||||
ôèç.àòì |
|
|
í.ê |
|
|
|
|||
132 |
129 |
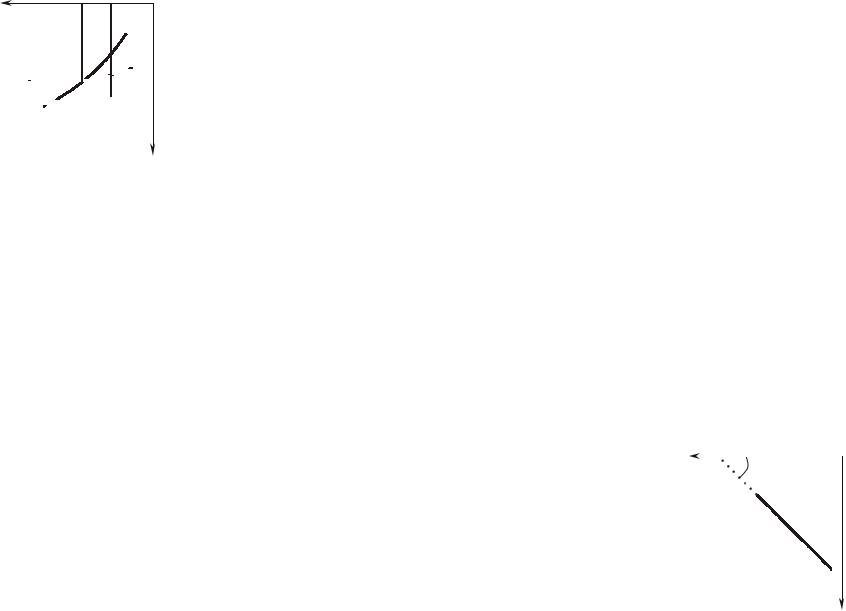
131 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.Ðèñ1.7.9 |
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
S |
æ |
|
|
|
|
|
|
|
||||||||
P |
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
P |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
b |
|
|
|
||||||
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
a |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
æ |
|
,акривая2–кеенасы- |
M |
жидкости |
|
|
êотносится 1 кривая что Положим,
.плотностью меньшей с фазе
ê– 2 кривая плотностью, большей
ñфазе к относится 1 кривая рисунке
|
|
|
T |
|
|
|
|
|
v, |
©wP¹ |
|||
|
òîíà |
¸ |
|
рис..1.7.9Поскольку¨ |
||
|
|
|
||||
|
|
|
§wM· |
|||
|
мостьпредставленаввидеграфикана |
|||||
|
.температуреТакогородазависи- |
|||||
Μ |
вкаждойиздвухфазприпостоянной |
|||||
когопотенциалавеществаотдавления |
||||||
|
||||||
|
Рассмотримзависимостьхимичес- |
|||||
|
.7.9Устойчивостьфаз |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
проинтегрироватьэто.уравнение |
||||
Знаятемпературнуюзависимостьтеплотысублимации,можно |
||||||||||||||
.6.(914) |
|
|
. |
2 |
RT |
|
|
dT |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
L |
|
|
dlnP |
|||||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
иуравнение.6.(913)приводитсяквиду |
|||||||||
|
|
|
|
|
, |
P |
ïàð |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
v |
||||
|
|
|
|
|
RT |
|||||||||
|
|
|
|
|
|
|
|
|
|
|||||
ньюточностиописываетсяуравнениемКлапейрона–Менделеева |
||||||||||||||
.речьУдельныйобъемпараналиниисублимациисвысокойстепе- |
||||||||||||||
|
|
|
|
|
|
|
|
òâ |
|
|
|
|
||
вуравнении.6.(913)можнопренеб- |
дойфазы,итогдавеличинойv |
|||||||||||||
лимациинанесколькопорядковбольше,чемудельныйобъемтвер- |
||||||||||||||
лениявтройнойточке);приэтомудельныйобъемпараналиниисуб- |
||||||||||||||
Обычносублимацияпроисходитпринизкихдавлениях(нижедав- |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
гдеL–теплота.сублимации |
||
|
|
|
òâ |
|
ïàð |
Tv |
|
|
|
|
||||
.6.(913) |
, |
|
v |
|
dT |
|
||||||||
|
|
|
L |
|
|
|
|
dP |
||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||||||
|
Вэтомслучаеуравнение.6.(97)можнозаписатьввиде |
|||||||||||||
|
Фазовыйпереход«твердоепар»–тело |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
130 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ìåð,ó.âîäû) |
|||||
.е.тсростомдавлениятемператураплавленияуменьшается(напри- |
|||||||||||||||||||||||||
<0, |
dT |
|
тураплавленияувеличивается;вовторомслучаевеличина |
||||||||||||||||||||||
dP |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
dT |
|
|
|
|
|
|
|
|
|
|||||
>0,т..есростомдавлениятемпера- |
видно,чтовпервомслучае |
||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||
dP |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
òâ |
æ |
|
òâ |
|
|
æ |
|
|
|
|
|
|||
Изуравнения.6.(912)оче- |
èv<v. |
|
>v |
|
возможныдваслучая:v |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
òâ |
|
æ |
|
|
|
|
|
||
обычноблизкимеждусобой;приэтом |
Удельныеобъемыvиv |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
òâ |
|
|
|
|
|
–удельныйобъемтвердойфазыналинииплавления. |
плавления;v |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
æ |
|
|
|
|
|
|
|
O |
|
||
–удельныйобъемжидкостиналинии |
–теплотаплавления;v |
ãäå |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
òâ |
v |
æ |
|
|
dT |
|
|
|
|
|
|
|
|
||
.6.(912) |
|
|
|
|
|
|
, |
|
Tv |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
Ο |
|
|
|
dP |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
(плавление)уравнение.6.(97)можнозаписатьввиде |
||||||||||||||||||
Применительнокфазовомупереходу«твердоежидкость»–тело |
|||||||||||||||||||||||||
|
|
|
|
|
Фазовыйпереход«твердоетело–жидкость» |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
S |
|
||
|
|
|
|
|
|
|
действительноимеетместо.(рис6.9..1) |
|
îò |
lnP |
|||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
S |
|
|
||
длябольшогочиславеществ,линейнаязависимость |
–T |
мостиP |
|||||||||||||||||||||||
Какпоказываетобработкаэкспериментальныхданныхзависи- |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
иметьлинейный.характер |
||||||||
|
|
|
©T¹ |
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
f |
lnP |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
должна |
¸ |
¨ |
.е.тприневысокихдавленияхзависимость |
||||||||||||||||||||||
|
|
|
§1· |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
.Ðèñ1.6.9 |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1/T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
=r/R |
tg |
S
lnP

áîð | 12 |
êÄæ |
). Кроме того, этот закон не учитывает темпера- |
кмоль К
турную зависимость PC от температуры. При малых температурах
v
этот закон качественно неверен.
Зависимость C от температуры для низких температур твердых
v
тел была получена с помощью методов квантовой статистики голландским физиком П. Дебаем в 1912 г.
Уравнение Дебая имеет вид
|
|
|
§ T |
· |
|
|
|
|
||
|
|
Cv |
3RF ¨ |
|
¸ |
, |
(10.1.7) |
|||
|
|
|
||||||||
|
|
|
© 4 |
¹ |
|
|
|
|
||
§ T · |
|
|
|
|
|
T |
||||
ãäå F ¨ |
|
¸ – сложная функция приведенной температуры |
|
|
, íå |
|||||
4 |
4 |
|||||||||
© |
¹ |
|
|
|
|
|
||||
зависящая от свойств веществ и одинакова для них. Величина 4
носит название характеристической дебаевской температуры и является постоянной для данного вещества.
Для твердых тел разность (С – C ) обычно мала, примерно со-
Pv
ставляет 3–5% от C , поэтому при не очень точных расчетах можно
v
считать, что С | C .
Pv
Относительно С известно, что
P
|
|
|
|
|
§ wP · |
§ wv |
·2 |
|
||||||
CP |
Cv |
T ¨ |
|
|
¸ |
¨ |
|
¸ |
|
|||||
|
|
|
|
|||||||||||
|
|
|
|
|
© wv ¹T |
© wT |
|
¹P |
|
|||||
или (что то же самое) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
C |
|
|
D2vT |
|
|
9Dl2vT |
|
, |
(10.1.8) |
|||
P |
v |
|
E |
|
|
E |
|
|||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||||
E – коэффициент изотермической сжимаемости.
В 1908 г. немецким физиком Э. Грюнайзеном для металлов была
экспериментально найдена зависимость между C и коэффициентом
P
объемного расширения D. При любых температурах
D |
;, |
(10.1.9) |
|
CP
где ; – константа, индивидуальная для каждого вещества.
Это соотношение имеет приближенный характер. Первоначально оно было установлено эмпирическим путем, а затем обосновано методами статистической физики.
Глава 10
ТЕРМОДИHАМИЧЕСКИЕ СВОЙСТВА
ВЕЩЕСТВ
Используя дифференциальные уравнения термодинамики можно рассмотреть термодинамические свойства веществ, обращая основное внимание на анализ характера зависимостей, связывающих одни свойства вещества с другими.
10.1. Термические и калорические свойства
твердых тел
Характерной особенностью твердых тел с точки зрения их физи- ческих свойств является их чрезвычайно малая сжимаемость.
Эксперимент показывает, что для большинства веществ в твердом состоянии коэффициент изотермической сжимаемости
1 § wv · E ¨ ¸ v © wP ¹T
обычно не превышает 10-10–10-12 Ïà-1, т.е. для большинства техни- ческих расчетов сжимаемостью твердых тел можно пренебречь.
Удельный объем твердых тел существенно изменяется лишь при сжатии до огромных давлений (порядка тысяч и десятков тысяч мегапаскалей). Зависимость изменения объема для различных веществ от давления при комнатной температуре
|
P |
§ wv · |
|
||
'v |
êãñ³ |
¨ |
|
¸ |
dP |
|
|||||
1 |
© wP ¹T |
|
|||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
ñì |
|
|
|
|
приведена на рис. 10.1.1 ('v/v – относительная величина, где v –
объем при нормальном атмосферном давлении).
Интересно отметить аномально малую сжимаемость алмаза – при увеличении давления до 104 МПа его удельный объем уменьшается лишь на 1,5 %.
136 |
133 |
135 |
|
|
|
|
|
|
|
| |
|
|
v |
P |
|
7,3; |
Cзначительнониже25(алмаз |
торыхлегкихэлементов |
||||
|
|
|
|
|
||
ЗаконДюлонгаиПтиимеетприближенный.характерДлянеко- |
||||||
|
|
|
ситназваниезаконаДюлонгаи.Пти |
|||
азатемметодамимолекулярно-кинетическойтеориивещества,но- |
||||||
Соотношение6),.1.(10установленноевначалеэкспериментально, |
||||||
|
|
|
|
лярную,анаатомную.массу |
||
Rнужноделитьненамолеку- |
P |
атомарномсостоянии,товеличину |
||||
|
|
|
|
|
|
|
âнаходятся фазе твердой в элементы химические Поскольку
Êкмоль v
.1.(106) |
|
|
|
. |
|
|
|
|
|
|
|
25 |
|
PC |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
êÄæ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лоемкостьтвердоготела |
||||||
гдеR–газоваяпостоянная.веществаСоответственномольнаятеп- |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
3R, |
|
|
v |
|
|
|
|
|
|
|
|
|
|
|
||
.1.(105) |
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
среднихивысокихтемпературах(вышекомнатных) |
||||||||||||||||||||||
Теплоемкостьтвердыхтел,какпоказываетэксперимент,при |
|||||||||||||||||||||||||||
.1.(104) |
|
|
|
|
|
|
|
. |
0 |
|
|
|
0 |
|
v |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
ve |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
TT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
Получаемэкспоненциальнуюзависимость |
|||||||||||||||||||||
|
|
|
|
|
|
|
P |
¹ |
|
wT |
© |
|
|
P |
¹ |
v©wT |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
.1.(103) |
|
|
|
. |
|
¸ |
|
|
|
|
¨ |
|
|
|
¸ |
|
|
¨ |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
wlnv· |
§ |
|
|
|
1§wv· |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
=const,òî |
D |
Еслисчитать |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
0,91 |
|
|
|
|
|
|
Алмаз |
|
|
|
|
72 |
|
|
|
|
атрий |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|||||
|
|
4,3 |
|
|
|
|
Вольфрам |
|
|
|
|
84 |
|
|
|
|
Калий |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
28,3 |
|
|
|
|
|
|
Свинец |
|
|
|
12,5 |
|
|
|
|
икель |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
||||||
|
18,3 |
|
|
|
|
|
|
Серебро |
|
|
|
11,7 |
|
|
|
|
Железо |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
2,3 |
|
|
|
|
|
Кремний |
|
|
|
16,1 |
|
|
|
|
Ìåäü |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
5,5 |
|
|
|
|
|
Германий |
|
|
|
|
23 |
|
|
|
|
Алюминий |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
101/K |
, |
l |
|
Вещество |
|
|
|
|
|
,101/K |
l |
|
|
Вещество |
|
|||||||||||
|
|
-6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
твердыхвеществ(притемпературе0С) |
|
|||||||||||||||||||||
|
|
|
|
|
|
θ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Температурныекоэффициентылинейногорасширениянекоторых |
||||||||||||||||||||||||||
1.1.10 |
Таблица |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
134 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.пературы |
||||||||||||||||||||||
величинойпостоянной,независящейоттем- |
D |
|
кихрасчетовсчитать |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D |
|
|
||||||
длятвердыхтелобычнослаба,чтопозволяетдлятехничес- |
íèÿ |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Температурнаязависимостькоэффициентаобъемногорасшире- |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
часовыхмеханизмови.д.т |
|||||||||||||||||||||||||||||||||||||||||||||
.лов)Инвариспользуетсядляизготовленияэталоновдлин,деталей |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
рическихрегуляторов(свойстворазностиудлиненийдвухматериа- |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
и.Ni)Этосвойствоиспользуетсявтехникедлясозданиядилатомет- |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
,чтопримернов20разменьше,чемдляFe |
|
K |
|
10 |
|
0,6 |
D| |
0150°Ñ |
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-1 |
|
|
|
|
-6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
y |
|||||||||||||
мер,дляинвара[сплавжелезаFeиникеляNi]притемпературе |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ствамаломеняютсвоиразмерысизменениемтемпературы(напри- |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
l |
D |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.еэтивеще- |
ìàëî,ò. |
Видно,чтодлянекоторыхтвердыхтел |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l |
3D |
D |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
.1.(102) |
|
|
|
|
|
|
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ропныхтел |
||||||||||||||||||||||
взависимостиот.температурыHетруднопоказать,чтодляизот- |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
которыйхарактеризуетизменениелинейныхразмеров(длины)тела |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l©wT¹ |
l |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
.1.(101) |
|
|
|
|
|
|
|
, |
¸ |
|
¨ |
|
|
D |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
§wl· |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
частопользуютсякоэффициентомлинейногорасширения |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D |
Hарядустемпературнымкоэффициентомобъемногорасширения |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
сверхпроводникии.д.т |
|||||||||||||||||||||||||||||||||||||||||
вблизиихточек,например,ферромагнетики,сегнетоэлектрики, |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
местофазовыепревращения |
|
|
|
|
|
|
|
|
|
|
|
|
.Ðèñ1.1.10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
твердыхтел,вкоторыхимеют |
|
|
|
|
|
|
|
|
|
|
|
|
10ÌÏà |
|
|
υ |
P, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
мерностьневыполняетсядля |
|
|
|
|
10 |
|
8 |
|
|
|
|
6 |
|
|
|
|
|
|
|
4 |
|
|
2 |
|
|
|
|
|
|
|
0 |
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
.Этазаконо- |
-1 |
Ê |
-5 |
етпримерно10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
составля- |
D |
Порядоквеличины |
|
|
|
Cs |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,6 |
||||||||||||
ноанизотропных.кристаллов) |
|
|
|
Rb |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
всегдаположителен(кромесиль- |
Ba |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
Na |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,4 |
|||
|
¹ |
wT |
v© |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
¸ |
|
|
¨ |
|
D |
|
|
|
|
|
|
Bi |
Se |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
wv· |
1§ |
|
|
|
|
|
|
|
|
|
Li |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,2 |
|||||||
фициентобъемногорасширения |
|
|
|
Sb |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
тельно,ихтемпературныйкоэф- |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,0 |
|||||||||||
теларасширяютсяи,следова- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Принагреваниивсетвердые |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
v/v |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||

пературой, поэтому при оценочных расчетах вполне допустимо при-
§ wP ·
нять ¨ ¸ постоянной и вынести за интеграл. Причиной столь силь-
© wT ¹v
ного роста давления при сравнительно небольшом повышении температуры является малая сжимаемость жидкости.
Жидкости заметно расширяются при нагревании. Так, например,
температурный коэффициент объемного расширения D |
1 |
§ wv · |
||||||||
|
¨ |
|
¸ |
|||||||
|
|
|||||||||
|
|
|
|
|
|
|
v |
© wT ¹P |
||
при комнатной температуре для |
|
|
|
|
|
|
|
|
|
|
азотной кислоты равен 124 10 |
5 |
K |
1 |
|
|
|
|
|||
|
, |
|
|
|
|
|||||
ацетона – 143 10 |
5 |
K |
1 |
|
|
|
|
|
|
|
|
, |
|
|
|
|
|
|
|
||
бензола – 110 10 |
5 |
K |
1 |
|
|
|
|
|
|
|
|
, |
|
|
|
|
|
|
|
||
ртути – 18,1 10 5 K 1 .
Для некоторых жидкостей, например, для воды, имеет место аномалия в значениях D. При t = 3,98°С наблюдается максимальное зна-
§ wv · |
0 . При нагревании от 0 до 3,98°С |
||
чение плотности воды и ¨ |
|
¸ |
|
|
|||
© wT ¹P |
|
||
плотность воды увеличивается, затем уменьшается.
Что касается теплоемкости жидкости, то к настоящему времени физически обоснованной статистической теории не существует, и
какие-либо теоретические оценки C и C для жидкости не могут
P v
быть сделаны даже приближенно, поэтому значения теплоемкости для жидкости определяют экспериментально или расчетным путем с помощью термодинамических соотношений по значениям других термических или калорических свойств – h-, P-, v-,T- зависимости и т.д.
Теплоемкость жидкости мало изменяется с изменением давле-
ния. В табл. 10.2.1 представлена зависимость C воды от давления
P
при t = 20°С. Как видно, при увеличении давления от 0,1 до 100 МПа
C изменяется на 5%. Для технических расчетов зависимостью теп-
P
лоемкости от давления можно пренебречь, для точных расчетов нужно учитывать. Однако нет необходимости в прямом эксперимен-
Таблица 10.2.1
P, ÌÏà |
0,1 |
20 |
40 |
60 |
80 |
100 |
||
|
|
|
|
|
|
|
|
|
CP , |
êÄæ |
|
4,183 |
4,128 |
4,074 |
4,040 |
4,007 |
3,973 |
|
||||||||
êã Ê |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Можно показать, что
D |
1 |
|
. |
(10.1.10) |
||
|
|
|
||||
CP |
|
§ wP · |
|
|||
|
|
vT ¨ |
|
¸ |
|
|
|
|
|
||||
|
|
© wT ¹S |
|
|||
Это соотношение справедливо для любого вещества в любом агрегатном состоянии.
|
D |
|
Поскольку для металлов |
|
const, òî |
|
||
CP
§ wP ·
vT ¨ ¸ const,
© wT ¹S
ò.å.
ωP ;vT. (10.1.11) wT
Это уравнение показывает, что для металлов, в отношении кото-
|
D |
§ wT · |
|
||
рых выполняется |
|
const , величина ¨ |
|
¸ |
пропорциональна v и |
|
CP |
© wP ¹S |
|||
T и показывает степень повышения температуры вещества при адиабатном сжатии.
Вещество в твердой фазе может существовать в виде различ- ных аллотропических модификаций, которые отличаются друг от друга своими физическими свойствами (кристаллическая структура, удельный объем, теплоемкость и т.д.). При этом каждая модификация существует лишь в определенной области параметров состояния, и переход из одной области в другую (т.е. от одной модификации к другой) обладает всеми признаками обычного фазового перехода: при переходе точно так же, как и в случае плавления, испарения или сублимации, скачкообразно меняются удельный объем и энтропия (т.е. существует теплота перехода), хотя в обеих фазах вещество находится в твердом состоянии. Hаклон пограничной кривой, разделяющей на РT-диаграмме области существования этих модификаций, определяется уравнением Клапейрона – Клаузиуса
dP |
|
L |
|
, |
dT |
|
T v v |
|
|
|
|
I II |
|
|
140 |
137 |
139 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
v |
|
|
©wT |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
¹ |
|
|
|
|
|
|
|
|||||
ужидкостейнеоченьсильноменяетсястем- |
¸ |
|
|
¨ |
Величина |
||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§wP· |
|
|
|
|
|
|
|||||
¹ |
2 |
© |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
v |
©wT¹ |
|
|
|
v |
¹ |
©wT |
50 |
|
|||||||||
¸. |
ñì |
¨102,6 |
|
10,06 |
|
|
|
|
|
1,006107 |
|
|
'T |
|
¸ |
|
|
|
dT|¨ |
|
¸ |
³¨ |
'P |
||||||||||||||||||||||||||
|
|
|
|
ÌÏà |
|
|
|
|
|
|
|
Ïà |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
· |
êãñ |
§ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§wP· |
|
|
|
|
§wP· |
60 |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
сосудевозрастаетна |
|||||||||||||||
=10°Сдавлениеводывэтом |
T |
' |
гососудапостоянногообъемана |
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
начает,чтопринагревезаполненноговодойгерметическизакрыто- |
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
v |
|
|
©wT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
Ê |
|
|
|
|
|
|
¹ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
.Этооз- |
|
1,006106 |
|
|
¸ |
|
|
|
|
Hапример,дляводыприT=50°С¨ |
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
Ïà |
|
|
|
|
|
|
· |
|
§wP |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
©wP¹ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
¸ |
|
|
|
¨ |
|
|
|
T¹v |
© |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§wv· |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
. |
|
|
|
|
¸ |
|
|
w |
¨ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
P |
©wT¹ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
wP· |
§ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
¸ |
|
|
|
|
¨ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§wv· |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
©wP |
|
|
|
|
|
|
|
|
|
|
|
|
v |
¹ |
|
©wT |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
¹ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
уравнением |
¸ |
|
|
¨ |
|
связанас |
|
|
¸ |
|
|
|
Величина¨ |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§wv· |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§wP· |
|
|
|
|
|
|
||||||||
нениядавлениясизменениемтемпературыприv=const.жидкости |
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
v |
©wT |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
¹ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
характеризующееинтенсивностьизме- |
, |
¸ |
|
|
|
|
|
¨ |
новеликозначение |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
©wP |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§wP· |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
¹ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
ужидкостейобыч- |
¸ |
|
|
|
Благодарямаломузначениювеличины¨ |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
§wv· |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4,45610 |
|
|
v©wP¹ |
|
|
E |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
. |
-1 |
Ïà |
|
|
|
|
|
¸ |
|
|
|
¨ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
wv· |
1§ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ческойсжимаемости |
|||||||||||||||
Hапример,дляводыприt=20°Свеличинакоэффициентаизотерми- |
|||||||||||||||||||||||||||||||||||||||||||||||||
слабосжимаемы,ноихсжимаемостьвыше,чемутвердых.тел |
|||||||||||||||||||||||||||||||||||||||||||||||||
Подобнотвердымтеламжидкостивобычномсостояниивесьма |
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
жидкостей |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
.2.10Термическиеикалорическиесвойства |
|
||||||||||||||||||||||||||||||||||||||||||||||
138
|
|
|
2500°Свприсутствии.катализатора |
| |
èt |
|
|
| |
|
|
|
|
|
10000ÌÏà |
Ð |
щего.алмазПолучениеборазонаосуществлялосьпри |
||||
|
|
|
|
|
|
|
называемыйборазон)–вещества,посвоейтвердостипревосходя- |
||||||
кубическуюкристаллическуюмодификациюнитридабораBN(так |
||||||
Аналогичнымспособомв1957.гискусственносинтезировали |
|
|||||
|
|
|
|
.цесса) |
||
кимдавлениемсиспользованиемкатализаторов(дляускоренияпро- |
||||||
чаютжидкийуглеродспоследующимегоохлаждениемподвысо- |
||||||
Чтобыполучитьискусственноалмазизграфита,сначалаполу- |
|
|||||
|
|
|
лическую.структуру |
|||
тожнойскоростью,.е.тпрактическиалмазсохраняетсвоюкристал- |
||||||
рахпроцесспревращенияалмазавграфитидетссовершеннонич- |
||||||
етсявграфитпривысоких.температурахПриобычныхтемперату- |
||||||
алмазженаходитсявметастабильномсостоянииилегкопревраща- |
||||||
Приобычныхусловияхустойчивоймодификациейявляетсяграфит, |
||||||
фитиалмаз,резкоотличающиесяпосвоимфизическим.свойствам |
||||||
Твердыйуглеродимеетдвекристаллическиемодификации–гра- |
|
|||||
|
|
|
циюльда.I |
|||
вратившисьвпорошок,которыйимелкристаллическуюмодифика- |
||||||
ся,егообъемувеличилсяпримернона20%,ибрусокраспался,пре- |
||||||
.духПомереповышениятемпературыэтотбрусокначалвздувать- |
||||||
лениевустановкедоатмосферногоиизвлекбрусокльдаIIнавоз- |
||||||
пературыжидкоговоздуха–(193°С),азатембыстроуменьшилдав- |
||||||
кеподдавлениемпримерно200МПаледII,онохладилегодотем- |
||||||
поставилинтересныйопыт:получиввэкспериментальнойустанов- |
||||||
циисуществуютпридавлениях,превышающих200МПа..ГТамман |
||||||
модификаций–обычнымльдомI,посколькуостальныемодифика- |
||||||
Впрактикемы,какправило,сталкиваемсялишьсоднойизэтих |
|
|||||
льданеподтвердилось,анумерацияльдов–курьезэтой.ошибки |
||||||
етпоиной.причинеПоявившеесясообщениеобэтоймодификации |
||||||
ЧтокасаетсяльдаIV,тообластьегосуществованияотсутству- |
|
|||||
|
|
|
типовльда(VII–выше2000.МПа) |
|||
фазевода(лед)имеетшестькристаллическихмодификаций–шесть |
||||||
пограничнойкривой,аL–теплота.переходаHапример,втвердой |
||||||
|
|
|
II |
I |
|
|
–удельныеобъемымодификацийIиIIвданнойточке |
èv |
ãäåv |
||||
