
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •ГЛАВА 1. Колонизационная резистентность – универсальный биологический механизм противоинфекционной защиты
- •ГЛАВА 2. Колонизационная резистентность кожи и слизистых оболочек у хирургических больных
- •ГЛАВА 3. Колонизационная резистентность кожи и слизистых оболочек у онкологических больных
- •3.1.Колонизационная резистентность кожи и слизистой оболочки полости рта у больных раком легкого
- •3.2.Колонизационная резистентность кожи и слизистой оболочки полости рта у больных раком молочной железы
- •ГЛАВА 4. Колонизационная резистентность слизистых оболочек репродуктивного тракта женщин при гинекологических заболеваниях
- •4.1. Колонизационная резистентность репродуктивного тракта женщин при эрозиях шейки матки
- •4.2. Колонизационная резистентность репродуктивного тракта женщин при вагинитах и вагинозах
- •ГЛАВА 5. Колонизационная резистентность у детей в условиях Севера
- •5.1. Особенности микробного статуса у детей в условиях Севера
- •5.2. Иммунологические параметры слюны у детей в условиях Севера
- •ГЛАВА 6. Новые подходы к коррекции нарушений колонизационной резистентности
- •6.1. Коррекция нарушений колонизационной резистентности природными иммуномодуляторами
- •6.2. Влияние кислородо- и озонотерапии на колонизационную резистентность
- •ЗАКЛЮЧЕНИЕ
- •ЛИТЕРАТУРА

ГЛАВА 5
КОЛОНИЗАЦИОННАЯ РЕЗИСТЕНТНОСТЬ У ДЕТЕЙ В УСЛОВИЯХ СЕВЕРА
В современных условиях резко возросло число стрессовых воздействий и неблагоприятных экологических факторов, сопровождающихся глубокими нарушениями микробной экологии организма человека. Особую актуальность это имеет для северных регионов.
Республика Саха (Якутия) и г. Якутск имеют ряд специфических климатогеографических особенностей. Климат в регионе резкоконтинентальный, он характеризуется длинной, холодной зимой и коротким жарким летом. Зимой много снега, а летом бывает мало влаги. Загрязненность воздуха в Якутске выше, чем в других северных городах России. Вода реки Лены и почва в районе Якутска считаются средне загрязненными, но из-за холодного климата медленно очищаются. Все северные экосистемы обладают пониженной способностью к самоочищению и микробиологической утилизации вредных веществ из-за вечной мерзлоты и низких температур в почве и водоемах.
В условиях Севера на организм человека действуют не только суровые природно-климатические условия, но и усиливающееся с каждым годом загрязнение окружающей среды, социально-экономические условия жизни и особенности питания населения, приобретающие на современном этапе характер стрессовых факторов. При постоянных или интенсивных воздействиях внешней среды выведенные из строя барьерные и адаптационные системы в свою очередь приводят к росту заболеваемости населения по целому ряду нозологий. Появляется много бессимптомных и стертых форм различных заболеваний в группах людей, относящихся к практически здоровым [1].
Изучение состояния КР организма и механизмов ее нарушений у детей, проживающих в условиях Севера, не проводилось. Учитывая высокий уровень общей заболеваемости детей на Севере, изучение данной проблемы является актуальным.
74

5.1. ОСОБЕННОСТИ МИКРОБНОГО СТАТУСА У ДЕТЕЙ В УСЛОВИЯХ СЕВЕРА
Здоровье детей – наиболее чувствительный показатель, отражающий состояние окружающей среды. Многочисленные данные свидетельствуют о том, что в экологически неблагоприятных регионах регистрируется повышенная заболеваемость детского населения. Так, нашими исследованиями показано, что преморбидные состояния (дисфункции желудочно-кишечного тракта, эпизоды пищевой аллергии, частые респираторные инфекции) выявляются более чем у трети (33,9%) детей дошкольного возраста, проживающих в г. Якутске и относящихся к группе «практически здоровых».
Установлена патогенетическая роль нарушений микробного пейзажа кишечника и иммунологической реактивности организма в развитии преморбидных состояний, особенно у детей. Нарушения в микробиоценозе кишечника наступают задолго до клинических проявлений, ведут к формированию состояния предболезни и являются факторами риска для развития аллергических заболеваний, болезней органов дыхания, пищеварения, формирования иммунодефицитных состояний.
Нашими исследованиями показано, что более чем у 90% организованных детей г. Якутска обнаружены дисбиотические отклонения в составе микрофлоры толстого кишечника. Если исходить из общепринятой классификации [23], то нормальный микробный пейзаж наблюдался лишь у 6 (9,7%). Нарушения 1 степени были у 17 (27,4%) детей, и дисбактериоз 2 степени имелся у 39 (62,9%) детей (рис. 12).
75

9,70%
Дисбактериоз 1 степени
27,40%
Дисбактериоз 2 степени
Нормальное состояние кишечной микрофлоры
62,90%
Рис.12. Структура дисбиотических изменений обследованных детей г. Якутска
Изменения в микробиоценозе толстого кишечника у детей нашего региона характеризуются снижением содержания лакто- и бифидофлоры, а также полноценных эшерихий (дефицит по этим показателям отмечен у 85,5%; 74,2% и 75,8% детей соответственно). На этом фоне активизируется условно-патогенная микрофлора. Так, по нашим данным у детей со 2 степенью дисбиозов в высоких титрах определялись условно-патогенные энтеробактерии - серрации, цитробактер, иерсинии (5,7 lg КОЕ/г), клостридии (5,2 lg КОЕ/г) и патогенный стафилококк (3,8 lg КОЕ/г). Кроме этого, довольно высоко было содержание эшерихий с изменёнными свойствами: палочки с низкой ферментативной активностью и лактозонегативные составляли около 40% от всего количества эшерихий, а гемолизирующие формы - от 20 до 100% (табл. 2)[13].
При этом выявленные изменения носили неспецифический характер и не зависели от анамнестических и клинических данных. На основании указанных данных все обследованные нами дети были разделены на 4 группы в зависимости от выявленных преморбидных состояний:
Здоровые дети;
Дети с множественным кариесом зубов;
76
Дети, имеющие функциональные нарушения со стороны желудочнокишечного тракта;
Дети с пищевой аллергией и атопическим дерматитом.
Таблица 2
Качественные и количественные показатели микрофлоры толстого кишечника у обследованных детей
Качественные |
Количественные показатели кишечной микрофлоры |
||
|
Норма, |
Частота |
Среднее |
показатели |
|
|
содержание, |
|
% (lg КОЕ/г) |
высева, % |
|
кишечной микрофлоры |
|
|
lg КОЕ/г (M+m) |
Бифидобактерии |
100 (10-11) |
100 |
8,8+0,3 |
Лактобактерии |
100 (7-8) |
100 |
4,9+0,2 |
Полноценные эшерихии |
100 (6-8) |
100 |
6,2+0,3 |
Лактозонегативные |
30 (3-5) |
28,8 |
5,0±0,01 |
эшерихии (lac-) |
|
|
|
Гемолитические эшерихии |
0 |
7,5 |
5,0±0,01 |
(hly+) |
|
|
|
Условно-патогенные |
30 (3-4) |
15,2 |
6,2+0,2 |
энтеробактерии |
|
|
|
Клостридии |
30 (3-4) |
11,5 |
3,5+0,1 |
S. aureus |
0 |
2,2 |
5,0±0,01 |
Дрожжи и дрожжеподобные |
30 (3-4) |
- |
- |
грибы |
|
|
|
Нашими исследованиями показано, что наиболее выраженные изменения кишечной микрофлоры были выявлены у детей, имеющих в анамнезе гастроэнтерологические нарушения. В этой группе зафиксированы наиболее низкие показатели содержания лактобактерий и кишечной палочки - 4,6 + 0,7 lg КОЕ/г и 5,75 + 0,8 lg КОЕ/г соответственно (у здоровых - 5,1 + 0,4 lg КОЕ/г и 6,3 + 0,4 lg КОЕ/г при норме обоих показателей 7-8 lg КОЕ/г). Кроме того, именно в этой группе детей был наиболее высокий процент высева клостридий и стафилококков [12].
У детей, имеющих в анамнезе аллергические реакции, было выявлено более низкое содержание бифидобактерий - 8,1 + 0,2 lg КОЕ/г (у здоровых
77
- 8,5 + 0,5 lg КОЕ/г при норме 10-11 lg КОЕ/г), а также наибольший процент (у 65,5%) высева эшерихий с изменёнными свойствами. Кроме того, у четверти детей этой группы выявлялись клостридии в среднем титре 5,7 + 0,06 lg КОЕ/г при допустимом содержании - до 3 lg КОЕ/г.
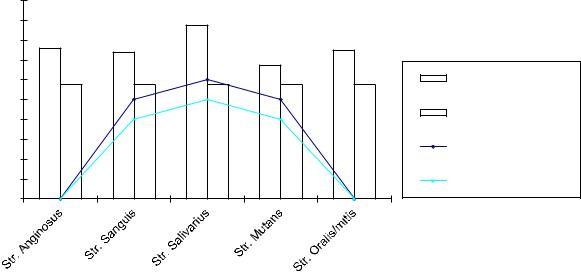
Кроме того, нами было показано, что обеднение нижних отделов желудочно-кишечного тракта сопровождается повышением уровня кариесогенной микрофлоры в полости рта (рис. 13).
10 |
|
|
|
|
|
|
9 |
|
|
8,75 |
|
|
|
|
|
|
|
|
|
|
8 |
7,6 |
7,4 |
|
|
7,5 |
|
7 |
|
|
|
6,75 |
|
|
|
|
|
|
|
|
|
6 |
5,75 |
5,75 |
5,75 |
5,75 |
5,75 |
Стрептококки |
|
|
|
|
|
||
5 |
|
|
|
|
|
|
4 |
|
|
|
|
|
Лактобактерии |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
Норма стрептококков |
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
1 |
|
|
|
|
|
Норма лактобактерий |
0 |
|
|
|
|
|
|
Рис. 13. Спектр ацидогенной флоры в слюне у детей с множественным кариесом зубов
У 20 обследованных нами детей с множественным кариесом при среднем содержании в кишечнике лактобактерий 4,7 ± 0,2 lg КОЕ/г их содержание в полости рта доходило до 7 lg КОЕ/мл (при норме 0-5). А количество стрептококков в ротовой жидкости достигало 10 lg КОЕ/мл (при норме 5- 6). Таким образом, повышенное содержание ацидогенной флоры в ротовой полости может рассматриваться как биологический фактор риска развития кариеса.
В результате микробиологического исследования носоглоточного отделяемого только у 28,7% детей выявлено нормальное состояние
78

микрофлоры, у 8,5% обнаружены дисбиотические изменения ротоглотки, что проявлялось в повышении количества зеленящих стрептококков (более 105 КОЕ) и катаральных нейссерий (более 103 КОЕ), а также появлении единичных клеток условно патогенных микроорганизмов: энтеробактерий
(E. coli, Klebsiella spp.), Enterococcus faecium, дрожжей и дрожжеподобных грибов, эпидермальных стафилококков с гемолитическими свойствами (S. epidermidis hly+).
S. aureus
|
|
3,30% |
2,50% |
|
|
|
|
|
|
|
5,50% |
|
|
S. pneumoniae |
|
|
|
|
|
|
|
|
27,60% |
E. faecium |
|
|
|
|
|
10,50% |
|
|
|
M. catarrhalis |
|
|
|
|
|
|
|
|
|
E. coli |
|
|
14,10% |
|
дрожжи |
|
|
|
|
Рис. 14. Спектр микрофлоры носоглотки у обследованных детей (% высева)
У остальных обследованных детей носоглотка была колонизирована различными патогенными и условно-патогенными возбудителями. Наиболее часто, почти у трети маленьких пациентов, выявлялись S. aureus
(27,6%), у 14,1% выявлялись Str. pneumoniae, и у 10,5% – E. faecium. У
остальных обследованных детей выявлялись M. catarrhalis, E. coli и дрожжевые грибы, что составило 5,5%, 3,3% и 2,5% соответственно. Этиологическая структура показана на рис. 14.
Таким образом, видно, что более чем 40% детей являются носителями S. aureus et S. pneumoniae. Высокая распространенность данных возбудителей вызывает беспокойство, т.к. у таких детей снижена колонизационная резистентность и повышена восприимчивость к инфекционным
79
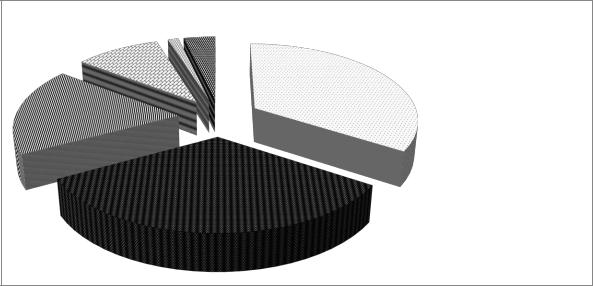
заболеваниям дыхательных путей, что имеет особую актуальность для жителей Севера.
При микробиологическом исследовании кожи здоровых детей нами был установлен следующий качественный и количественный состав микрофлоры: у 70% детей обнаруживались сарцины, у 67,5% - Staphylococcus saprophyticus, у 37,5% - Escherichia coli в количестве от 10 до 103 KOE. У 20 % детей обнаруживались Staphylococcus epidermidis
гемолитический (hly+) в количестве от 10 до 106 KOЕ, у 2,5% – нейссерии в количестве 103 KOЕ, у 7,5% - единичные клетки плесени и в 5% случаев бактериальный рост не наблюдался. При этом практически не встречалось монокультур, сочетание микроорганизмов на коже здоровых детей было разнообразным как в качественном, так и в количественном отношении
(рис. 15).
Бактерицидность кожи по отношению к кишечной палочке составила 86,7%, что является нормой (70-90%).
2,5 7,5
20
|
70 |
|
Sarcina |
37,5 |
S. saprophyticus |
|
|
|
E. coli |
|
S. epidermidis |
|
Neisseria spp |
|
плесневые грибы |
|
67,5 |
Рис. 15. Спектр эпидермальной микрофлоры у обследованных детей
Поскольку в патогенезе атопического дерматита, а также воспалительных заболеваний кожи и подкожной клетчатки основную роль играют патогенные стафило- и стрептококки, можно сказать, что резистентность кожного барьера у наблюдаемых нами детей достаточно высока.
80
