
okv-16
.pdf
Спиновое гиромагнитное отношение для электрона
Экспериментально было доказано, что гиромагнитное соотношение для спиновых моментов в два раза больше, чем для орбитальных:
|
|
|
Ms |
|
= − |
e |
|
|||
|
|
|
Ls |
me |
|
|
||||
Так как Ls = ~√ |
|
/2, то |
|
|
|
|
|
|||
3 |
|
|
|
|
|
|||||
|
|
|
|
e |
|
|
|
√ |
|
|
|
|
|
|
|
|
|
|
|||
Ms = − |
|
Ls = −µБ 3 |
||||||||
m2 |
||||||||||
Проекции собственного (спинового) магнитного момента может принимать два значения:
e
Msz = − me Lsz = ±µБ
Квантование атомов. Таблица Менделеева
Спин электрона
Полный момент импульса электрона в атоме
Магнитные
моменты
электрона
Орбитальное
гиромагнитное отношение и магнитный момент атома
Спиновое
гиромагнитное отношение для электрона
Полный
магнитный момент атома
Спин-орбитальное взаимодействие
Правила отбора
Многоэлектронные
атомы
Опыт Штерна Герлаха
Эффекты Зеемана и

Спиновое гиромагнитное отношение для электрона
Экспериментально было доказано, что гиромагнитное соотношение для спиновых моментов в два раза больше, чем для орбитальных:
|
|
|
Ms |
|
= − |
e |
|
|||
|
|
|
Ls |
me |
|
|
||||
Так как Ls = ~√ |
|
/2, то |
|
|
|
|
|
|||
3 |
|
|
|
|
|
|||||
|
|
|
|
e |
|
|
|
√ |
|
|
|
|
|
|
|
|
|
|
|||
Ms = − |
|
Ls = −µБ 3 |
||||||||
m2 |
||||||||||
Проекции собственного (спинового) магнитного момента может принимать два значения:
e
Msz = − me Lsz = ±µБ
Квантование атомов. Таблица Менделеева
Спин электрона
Полный момент импульса электрона в атоме
Магнитные
моменты
электрона
Орбитальное
гиромагнитное отношение и магнитный момент атома
Спиновое
гиромагнитное отношение для электрона
Полный
магнитный момент атома
Спин-орбитальное взаимодействие
Правила отбора
Многоэлектронные
атомы
Опыт Штерна Герлаха
Эффекты Зеемана и
Спиновое гиромагнитное отношение для электрона
Экспериментально было доказано, что гиромагнитное соотношение для спиновых моментов в два раза больше, чем для орбитальных:
|
|
|
Ms |
|
= − |
e |
|
|||
|
|
|
Ls |
me |
|
|
||||
Так как Ls = ~√ |
|
/2, то |
|
|
|
|
|
|||
3 |
|
|
|
|
|
|||||
|
|
|
|
e |
|
|
|
√ |
|
|
|
|
|
|
|
|
|
|
|||
Ms = − |
|
Ls = −µБ 3 |
||||||||
m2 |
||||||||||
Проекции собственного (спинового) магнитного момента может принимать два значения:
e
Msz = − me Lsz = ±µБ
Квантование атомов. Таблица Менделеева
Спин электрона
Полный момент импульса электрона в атоме
Магнитные
моменты
электрона
Орбитальное
гиромагнитное отношение и магнитный момент атома
Спиновое
гиромагнитное отношение для электрона
Полный
магнитный момент атома
Спин-орбитальное взаимодействие
Правила отбора
Многоэлектронные
атомы
Опыт Штерна Герлаха
Эффекты Зеемана и

Полный магнитный момент атома
Так как гиромагнитные соотношения для орбитального и спинового моментов разные, то полный магнитный момент вычисляется более сложным образом:
p
Mj = µБg j(j + 1)
g = 1 + j(j + 1) + s(s + 1) − ℓ(ℓ + 1) 2j(j + 1)
где g фактор магнитного расщепления или множитель Ланде.
Проекции полного момента:
Mjz = −µБgmj
Квантование атомов. Таблица Менделеева
Спин электрона
Полный момент импульса электрона в атоме
Магнитные
моменты
электрона
Орбитальное
гиромагнитное отношение и магнитный момент атома
Спиновое
гиромагнитное отношение для электрона
Полный
магнитный момент атома
Спин-орбитальное взаимодействие
Правила отбора
Многоэлектронные
атомы
Опыт Штерна Герлаха
Эффекты Зеемана и

Полный магнитный момент атома
Так как гиромагнитные соотношения для орбитального и спинового моментов разные, то полный магнитный момент вычисляется более сложным образом:
p
Mj = µБg j(j + 1)
g = 1 + j(j + 1) + s(s + 1) − ℓ(ℓ + 1) 2j(j + 1)
где g фактор магнитного расщепления или множитель Ланде.
Проекции полного момента:
Mjz = −µБgmj
Квантование атомов. Таблица Менделеева
Спин электрона
Полный момент импульса электрона в атоме
Магнитные
моменты
электрона
Орбитальное
гиромагнитное отношение и магнитный момент атома
Спиновое
гиромагнитное отношение для электрона
Полный
магнитный момент атома
Спин-орбитальное взаимодействие
Правила отбора
Многоэлектронные
атомы
Опыт Штерна Герлаха
Эффекты Зеемана и

Полный магнитный момент атома
Так как гиромагнитные соотношения для орбитального и спинового моментов разные, то полный магнитный момент вычисляется более сложным образом:
p
Mj = µБg j(j + 1)
g = 1 + j(j + 1) + s(s + 1) − ℓ(ℓ + 1) 2j(j + 1)
где g фактор магнитного расщепления или множитель Ланде.
Проекции полного момента:
Mjz = −µБgmj
Квантование атомов. Таблица Менделеева
Спин электрона
Полный момент импульса электрона в атоме
Магнитные
моменты
электрона
Орбитальное
гиромагнитное отношение и магнитный момент атома
Спиновое
гиромагнитное отношение для электрона
Полный
магнитный момент атома
Спин-орбитальное взаимодействие
Правила отбора
Многоэлектронные
атомы
Опыт Штерна Герлаха
Эффекты Зеемана и

|
Квантование |
|
атомов. Таблица |
|
Менделеева |
|
Спин электрона |
|
Полный момент |
|
импульса |
|
электрона в атоме |
|
Магнитные |
|
моменты |
|
электрона |
|
Спин-орбитальное |
4. Спин-орбитальное взаимодействие |
взаимодействие |
Дублетная |
|
|
структура |
|
спектральных |
|
линий |
|
Дублетная |
|
структура и спин- |
|
орбитальное |
|
взаимодействие |
|
Квантовое число |
|
спин- |
|
орбитального |
|
взаимодействия |
|
Правила отбора |
|
Многоэлектронные |
|
атомы |
|
Опыт |
|
Штерна Герлаха |
|
Эффекты |
|
Зеемана и |
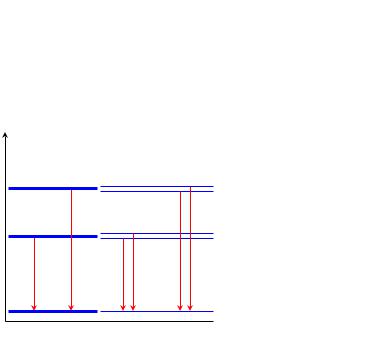
Дублетная структура спектральных линий
Исследование спектральных линий атомов щелочных металлов приборами с высоким разрешением показало, что почти все линии имеют дублетную структуру состоят из двух очень близких друг к другу линий.
низкое |
высокое |
разрешение |
разрешение |
n = 3 |
|
n = 2 |
|
n = 1 |
|
Квантование атомов. Таблица Менделеева
Спин электрона
Полный момент импульса электрона в атоме
Магнитные
моменты
электрона
Спин-орбитальное взаимодействие
Дублетная
структура
спектральных
линий
Дублетная структура и спинорбитальное взаимодействие
Квантовое число спинорбитального взаимодействия
Правила отбора
Многоэлектронные
атомы
Опыт Штерна Герлаха
Эффекты Зеемана и

Дублетная структура и спин-орбитальное взаимодействие
Существование дублетной структуры объясняется тем, что орбитальный и собственный магнитные моменты электронов взаимодействуют друг с другом. Точнее взаимодействуют магнитные поля, возникающие из-за орбитального движения электрона и из-за наличия у него спина.
В результате этого состояния электронов с разными ориентациями спинов имеют разную энергию, но отличие в энергии очень мало.
Поэтому в спектрах это проявляется не как появление новых отдельных линий, а как слабо заметное раздвоение линий. Взаимодействие спиновых и орбитальных моментов называется спин-орбитальным.
Квантование атомов. Таблица Менделеева
Спин электрона
Полный момент импульса электрона в атоме
Магнитные
моменты
электрона
Спин-орбитальное взаимодействие
Дублетная
структура
спектральных
линий
Дублетная структура и спинорбитальное взаимодействие
Квантовое число спинорбитального взаимодействия
Правила отбора
Многоэлектронные
атомы
Опыт Штерна Герлаха
Эффекты Зеемана и

Дублетная структура и спин-орбитальное взаимодействие
Существование дублетной структуры объясняется тем, что орбитальный и собственный магнитные моменты электронов взаимодействуют друг с другом. Точнее взаимодействуют магнитные поля, возникающие из-за орбитального движения электрона и из-за наличия у него спина.
В результате этого состояния электронов с разными ориентациями спинов имеют разную энергию, но отличие в энергии очень мало.
Поэтому в спектрах это проявляется не как появление новых отдельных линий, а как слабо заметное раздвоение линий. Взаимодействие спиновых и орбитальных моментов называется спин-орбитальным.
Квантование атомов. Таблица Менделеева
Спин электрона
Полный момент импульса электрона в атоме
Магнитные
моменты
электрона
Спин-орбитальное взаимодействие
Дублетная
структура
спектральных
линий
Дублетная структура и спинорбитальное взаимодействие
Квантовое число спинорбитального взаимодействия
Правила отбора
Многоэлектронные
атомы
Опыт Штерна Герлаха
Эффекты Зеемана и
