
- •Бронхолегочные изменения:
- •Возрастные особенности клинических проявлений муковисцидоза:
- •B грудном возрасте
- •Потовая проба
- •Организация службы диспансерного наблюдения и лечения больных мв
- •Показания для назначения антибиотиков при мв
- •Антибактериальная терапия при высеве из бронхиального секрета Staphylococcus aureus
- •Антибактериальная терапия при высеве из бронхиального секрета Haemophilus influenzae
- •Антибактериальная терапия при высеве из бронхиального секрета Pseudomonas aeruginosa
- •Рекомендуемая схема лечения абпа
- •Терапия недостаточности поджелудочной железы
- •Диетотерапия
- •Терапия синдрома дистальной интестинальной обструкции (сдио)
- •Терапия поражения печени
- •Лечение гастроэзофагеального рефлюкса (гэр)
- •Терапия поздних и редких осложнений мв
- •Новые технологии
- •Использованная литература:
ВВЕДЕНИЕ
Муковисцидоз ( от лат «mucus» - относящийся к слизи, слизистый и «viscidus» - липкий)- наследственное заболевание, обусловленное мутацией гена МВТР (муковисцидозного трансмембранного регулятора), характеризующееся поражением экзокринных желез жизненно важных органов и систем, наследуемое по аутосомно-рециссивному типу, имеющее тяжелое течение и прогноз.
Ежегодно в России рождается около 650 больных муковисцидозом , а в мире –более 45000детей. Средняя продолжительность жизни больных муковисцидозом раньше не превышала 5 лет, в наши дни благодаря расширению знаний о МВ и разработке эффективных методов терапии, заболевание диагностируется намного раньше, а средняя продолжительность жизни больных в развитых странах увеличилась. Таким образом средняя продолжительность жизни таких больных в Москве составляет 16 лет, в Санкт-Петербурге 23.6 лет с тенденцией увеличения числа взрослых больных МВ
Данное заболевание имеет социальное значение всязи с проградиентным характером течения с последующим летальным исходом или инвалидизации значительной части больных.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Ген МВТР был изолирован в 1989году (Kommens I. et al.), а затем расшифрована его структура: он содержит 27 экзонов и 25 тысяч пар нуклеотидов и расположен в середине длинного плеча 7 хромосомы.
Наиболее распространены мутации, ответственные за развитие МВ в России: F508 (53,2%), CFTR dele 2,3 (21kb) (5,5%), N1303K (2,7%), 2184insA (1,8%), 2143delT (2%), W1282Х (1,8%), G542Х (2%), 3849+10kbC—>T (1,9%), R334W (0,7%), S1196Х (0,7%). Наиболее тяжелая и ранняя манифестация наблюдается у больных гомозигот по F508 (частота которой в среднем по России составляет 53%, а в Москве - 41%). Больные гомозиготы по отсутствию F508 - отличаются наибольшим клиническим полиморфизмом, т.е. наряду с тяжелыми формами, ранней манифестацией и ранним неблагоприятным исходом, наблюдаются относительно благоприятные формы болезни, диагностируемые в старшем детском и подростковом возрастах.
Мутации гена МВТР следует подразделять на классы в зависимости от типа и тяжести первичного повреждающего эффекта.
Типы мутаций МВТР (по Tsui, 1992, Welsh and Smith, 1993, Kerem, 1996)
|
Классификация мутаций МВТР по тяжести фенотипического проявления (Kerem, 1996)
|
Мутация гена МВТР в гомозиготном состоянии приводит к нарушению структуры, функции и синтеза белка (его называют муковисцидозным трансмембранным регулятором), формирующего хлорный канал в апикальной части мембраны эпителиальных клеток, выстилающих выводные протоки поджелудочной железы, кишечника, бронхолегочной системы, урогенитального тракта, через который происходит электролитный транспорт (преимущественно пассивный транспорт ионов хлора).
Белок-регулятор состоит из регуляторного R-домена с большим числом сериновых остатков, являющихся мишенью для протеинкиназы А, которая осуществляет фосфорилирование этого белка. Кроме того, белок имеет 2АТФ-связывающих участка и 2 гидрофобных трансмембранных домена, каждый из которых представляет собой 6 витков спирали, пронизывающих клеточную мембрану. Специальные исследования показали, что данный белок является собственно хлорным каналом, а не его регулятором, как предполагалось раньше; для активации этого канала необходимы цАМФ (стимулирует протеинкиназу А)и АТФ. Патологический белок становится не способен выполнять роль хлорного канала в апикальной части мембраны клетки и ионы хлора накапливаются внутри нее, изменяется электрический потенциал в просвете выводных протоков, способствуя повышенному выходу из просвета внутрь клетки ионов натрия, что ведет к повышенному «всасыванию» перицеллюлярного водного компонента, следствием чего является сгущение секретов желез внешней секреции, затруднение их эвакуации и вторичные изменения в этих органах.
Бронхолегочные изменения:
Железы слизистой, выстилающей респираторные пути, вырабатывают большое количество вязкого секрета, который, скапливаясь в просвете бронхов, приводит к полной обтурации мелких бронхиол. В результате инфицирования неподвижной и вязкой слизи патогенной микрофлорой развивается гнойное воспаление. Соответственно слизистый секрет замещается гнойным. Вследствие нарушения естественного пассажа мокроты, который осуществляется движениями реснитчатого эпителия ("цилиарного эскалатора"), нарастает обструкция, что ведет к интенсификации инфекционного процесса и формированию порочного круга: обструкцияинфекция-воспаление.
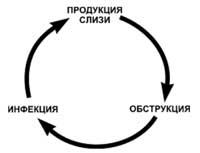
Рис. 1. Порочный круг, лежащий в основе бронхолегочного поражения при МВ
В стенках бронхов выявляются признаки воспаления различной степени тяжести. Клеточные структуры, обеспечивающие прочность бронхиальной стенки, разрушаются, что приводит к формированию бронхиолоэктазов и бронхоэктазов. Поскольку процесс полной облитерации мелких бронхов происходит достаточно быстро, задержка воздуха в респираторных путях происходит уже на ранних стадиях заболевания. Прогрессирующая обструкция бронхов и задержка воздуха может сопровождаться образованием ателектазов и эмфиземы. По мере нарастания тяжести заболевания выявляются распространенные бронхоэктатические изменения и признаки разрушения паренхимы легких, нарастает гипоксемия, развивается легочная гипертензия и легочное сердце. Соответственно, продолжительность жизни больного муковисцидозом определяется в первую очередь состоянием бронхолегочной системы.
Инфекция: В условиях мукостаза и бронхиальной обструкции у детей с МВ уже в течение первого года жизни или позднее, часто на фоне вирусной инфекции, снижающей эффективность локальных механизмов противомикробной защиты, в нижние отделы респираторного тракта проникает большое количество различных патогенных микроорганизмов. Наиболее распространенными являются палочка инфлюэнции (Haemophilius influenzae), золотистый стафилококк (Staphylococcus aureus) и синегнойная палочка (Pseudomonas aeruginosa). Как правило, в первую очередь респираторные пути инфицируются St. aureus, а затем часто присоединяется P. aeruginosa. Если возбудитель (P. aeruginosa или St. aureus и др.) регулярно более 6 месяцев высевается из бронхиального секрета, применяется термин хронической синегнойной или стафилококковой инфекции. Развитие хронической синегнойной инфекции нижних дыхательных путей обычно сопровождается нарастанием респираторной симптоматики и прогрессивным ухудшением функции легких. При этом P.aeruginosa может трансформироваться в мукоидные (слизистые) формы. Мукоидные формы P. aeruginosa окружены слизистой капсулой (алгинатом), защищающей их от действия антибиотиков, антител и других факторов иммунной защиты. При хронической синегнойной инфекции санация бронхиального дерева от P. aeruginosa практически невозможна. В последнее время возросла роль Burkholderia cepacia и обсуждается роль Stenotrophomonas maltophilia. Инфекция, обусловленная Burkholderia cepacia, вызывает большую озабоченность из-за ее мультирезистентности к антибиотикам и трансмиссивности некоторых ее штаммов.
Изменения в поджелудочной железе: Сгущение секрета поджелудочной железы плода часто приводит к обструкции ее протоков еще до рождения ребенка. В результате, панкреатические ферменты, которые продолжают вырабатываться в ацинусах в обычном количестве, не достигают двенадцатиперстной кишки. Накопление активных ферментов приводит к аутолизису ткани поджелудочной железы. На более отдаленных стадиях этого процесса, часто уже на первом месяце жизни, тело поджелудочной железы представляет собой скопление кист и фиброзной ткани — отсюда другое название заболевания: "кистофиброз". Неминуемым следствием разрушения поджелудочной железы становится нарушение переваривания и всасывания в желудочно-кишечном тракте прежде всего жиров и белков. При отсутствии соответствующего лечения эти процессы приводят к задержке физического развития ребенка. Некоторые мутации гена МВ (IY и Y класса) связаны с медленным развитием описанного выше хронического панкреатита и наличием сравнительно сохранной функции поджелудочной железы в течение многих лет.
Тонкая кишка: Примерно у 20% новорожденных, страдающих МВ, нарушения транспорта натрия, хлора и воды в тонкой кишке сопровождаются развитием мекониального илеуса, развивающегося в результате закупорки дистальных отделов тонкой кишки густым и вязким меконием. При этом в ряде случаев развивается атрезия тонкой кишки. Стенка чрезмерно расширенной кишки может разрываться еще до рождения ребенка, что приводит к мекониальному перитониту. За редким исключением наличие мекониального илеуса свидетельствует о муковисцидозе. "Синдром дистальной интестинальной обструкции" (СДИО) или "эквивалент мекониального илеуса" - термин, используемый для обозначения острой, подострой или хронической обструкции дистальных отделов тонкой и проксимальных отделов толстой кишок клейким секретом слизистой и каловыми массами. СДИО является клиническим признаком муковисцидоза у детей и взрослых. Другой причиной интестинальной обструкции у детей, больных муковисцидозом, может служить инвагинация тонкой кишки.
Печень: В редких случаях в качестве клинического признака муковисцидоза выступает длительная неонатальная желтуха, связанная с "синдромом сгущения желчи". Фиброз печени, развивающийся в той или иной степени почти у всех больных МВ, в 5-10% наблюдений прогрессирует до тяжелого заболевания печени с билиарным циррозом и портальной гипертензией.
Кожные покровы: Секрет потовых желез у больных муковисцидозом характеризуется повышенными концентрациями натрия и хлора: содержание соли превышает нормальный показатель примерно в 5 раз. Такая аномалия функции потовых желез выявляется уже при рождении и сохраняется на протяжении всей жизни пациента. Измерение концентрации соли лежит в основе потовой пробы-основного лабораторного теста для диагностики МВ. В условиях жаркого климата чрезмерная потеря соли через кожные покровы приводит к электролитным расстройствам, метаболическому алкалозу и подверженности тепловому удару.
Репродуктивная система: Почти у всех больных муковисцидозом мужского пола (97%) развивается азооспермия, связанная с врожденным отсутствием, атрофией или обструкцией семенного канатика. Соответственно большинство мужчин, больных муковисцидозом, не способно иметь потомство. Указанные аномалии встречаются и у части лиц мужского пола из числа носителей гена муковисцидоза. У пациентов женского пола МВ сопровождается снижением фертильности: повышенная вязкость отделяемого цервикального канала матки затрудняет миграцию сперматозоидов. Однако многие женщины, страдающие МВ, сохраняют детородную функцию.
КЛИНИЧЕСКАЯ КАРТИНА Клиническая картина разнообразна, зависит от типа мутации (или мутаций), возраста ребенка, тяжести поражения отдельных органов и систем, продолжительности заболевания и наличия осложнений, а также адекватности терапии.
Основные формы муковисцидоза:
-
смешанная, с поражением желудочно-кишечного тракта и бронхолегочной системы (75-80%)
-
преимущественно легочная (15-20%)
-
преимущественно кишечная (5%)
Некоторые авторы выделяют также печеночную с явлениями цирроза, портальной гипертензии и асцитом, изолированную электролитную (псевдосиндром Баррета); мекониевую непроходимость, атипичные и стертые формы муковисцидоза.
