
- •1 Реферат
- •2 Содержание
- •3 Обозначения и сокращения
- •4 Введение
- •5 Обзор литературы
- •5.1 Ауксины
- •5.1.1.1 Синтез 4х
- •5.1.2 Имк [гамма-(индолил-3)-масляная кислота]
- •5.1.2.1 Синтез имк
- •5.1.3 Нук (α-нафтилуксусная кислота)
- •5.1.4 Ноук (β-нафтоксиуксусная кислота)
- •5.2 Гиббереллины
- •5.3 Цитокинины
- •5.3.1 Дифенилмочевина и ее производные
- •5.3.1.1 Синтез дифенилмочевины
- •5.3.1.2 Синтез тидиазурона [n-фенил-n'-(1,2,3-тиадиазол-5-ил)мочевины]
- •5.4 Другие стимуляторы роста растений
- •5.4.1 Фурановые соединения
- •5.4.1.1 Синтез гидрофуранона:
- •5.4.2 Натриевые соли нафтеновых кислот
- •6 Экспериментальная часть
- •6.1 Биологические испытания
- •7 Заключение
- •8 Список использованных источников
5.3.1 Дифенилмочевина и ее производные
Впервые цитокининовая активность была обнаружена у дифенилмочевины. С тех пор цитокининовая активность была обнаружена у большого числа ее производных. [1]
5.3.1.1 Синтез дифенилмочевины
В колбу загружают анилин, триметилсилиловый эфира диэтилкарбаминовую кислоту и нагревают в перегонной колбе при температуре 150-170°C. Затем отгоняют фракцию при температуре 55-113°C. В колбе выпадает осадок, имеющий т. пл. 236-238°C, что соответствует дифенилмочевине. [11]
5.3.1.2 Синтез тидиазурона [n-фенил-n'-(1,2,3-тиадиазол-5-ил)мочевины]
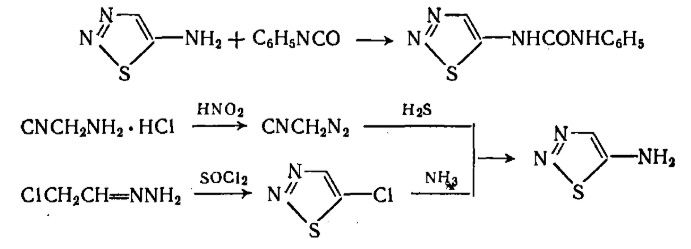
Тидиазурон практически с количественным выходом получают по реакции фенилизоцианата с 5-амино-1,2,3-тиадиазолом. Реакция протекает легко в присутствии третичных аминов в качестве катализатора. Необходимый 5-амино-1,2,3-тиадиазол можно синтезировать из нитрила аминоуксусной кислоты или из гидразона монохлорацетальдегида с образованием 5-хлор-1,2,3-тиадиазола и последующим его аминированием. [12]
5.4 Другие стимуляторы роста растений
5.4.1 Фурановые соединения
Некоторые фурановые соединения также являются стимуляторами роста растений.[13]
5.4.1.1 Синтез гидрофуранона:
Реакцию проводят в анодной ячейке, фурфурол смешивают с 30 %-ным Н2О2 и раствором перхлората лития при силе тока 0,01 – 0,03 А.
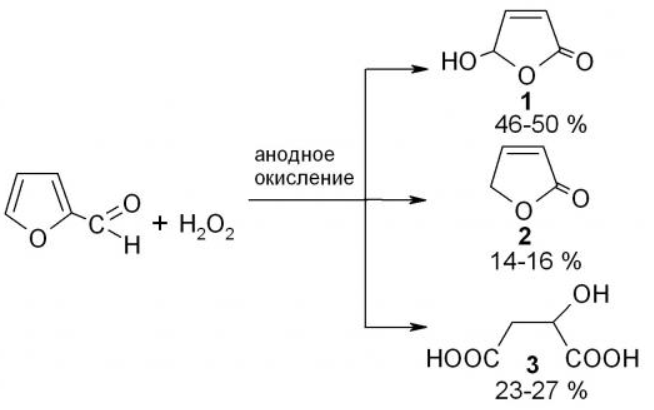
По окончании реакционную смесь нейтрализуют NaHCO3 до рН около 7, удаляют 70-80% воды, удаляют 2(5Н)-фуранон 2 экстракцией CCl4, остаток подкисляют раствором HCl до рН около 2, упаривают досуха, из сухого остатка извлекают 5-гидрокси-2(5Н)-фуранон 1 методом постоянной жидкостной экстракции бензолом в аппарате Сокслета.[14]
5.4.2 Натриевые соли нафтеновых кислот
Водный раствор натриевых солей нафтеновых кислот, содержащий, по-видимому, примеси натриевых солей фенолов, под маркой «НРВ» в настоящее время используется как эффективный стимулятор роста растений. [15]
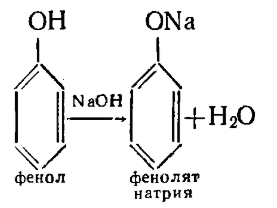
Рис. 7. Схема синтеза фенолята натрия
6 Экспериментальная часть
Было смоделировано следующее соединение в качестве стимулятора: этиловый эфир 4-пиридинкарбоновой кислоты. По предварительной оценке биологической активности соединение обладает следующими свойствами: ингибитор монодегидроаскорбат редуктазы, нитратредуктазы, метилентетрагидрофолатредуктазы, сахарофосфатазы, сульфитоксидазы, регулирует липидный обмен. Все эффекты представлены в таблице 1.
|
Pa |
Pi |
Воздействие |
|
0,897 |
0,004 |
Monodehydroascorbate reductase (NADH) inhibitor |
|
0,885 |
0,003 |
Nitrate reductase (cytochrome) inhibitor |
|
0,874 |
0,009 |
Methylenetetrahydrofolate reductase (NADPH) inhibitor |
|
0,854 |
0,009 |
Sugar-phosphatase inhibitor |
|
0,835 |
0,003 |
Sulfite oxidase inhibitor |
|
0,821 |
0,003 |
Laccase inhibitor |
|
0,817 |
0,005 |
Lipid metabolism regulator |
|
0,813 |
0,008 |
Membrane permeability inhibitor |
|
0,798 |
0,007 |
Ribulose-phosphate 3-epimerase inhibitor |
|
0,775 |
0,006 |
Peroxidase inhibitor |
|
0,750 |
0,007 |
Mitochondrial processing peptidase inhibitor |
|
0,717 |
0,015 |
NADPH-cytochrome-c2 reductase inhibitor |
Таблица 1 — Активности этилового эфира 4-пиридинкарбоновой кислоты в PassOnline
Был предложен и проведен синтез данного соединения:
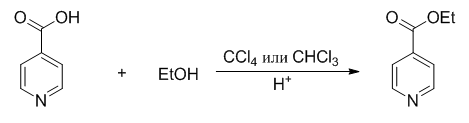
Методика:
В круглодонную колбу (V = 250 мл), снабженную делительной насадкой и обратным холодильником, помещают 30.78 г (0.250 моль) 4-пиридинкарбоновой кислоты, 0.3 мл конц. серной кислоты, 12.67 г (0.275 моль, 10 мл) этанола в 50 мл четыреххлористого углерода или хлороформа. Реакционную массу кипятят на водяной бане до полной отгонки воды. После чего, смесь охлаждают, переносят в делительную воронку и промываю последовательно 100 мл воды, 25 мл насыщенного водного раствора бикарбоната натрия и снова водой до нейтральной реакции. Избыток растворителей упаривают, а остаток перегоняют в вакууме. Получают 23.43 г (62%) продукта в виде маслянистой жидкости, т. кип = 160-162°С при 15 мм. рт. ст. (лит. данные [16]: т. кип = 220°С при 765 мм. рт. ст.).
