
- •1 Реферат
- •2 Содержание
- •3 Обозначения и сокращения
- •4 Введение
- •5 Обзор литературы
- •5.1 Ауксины
- •5.1.1.1 Синтез 4х
- •5.1.2 Имк [гамма-(индолил-3)-масляная кислота]
- •5.1.2.1 Синтез имк
- •5.1.3 Нук (α-нафтилуксусная кислота)
- •5.1.4 Ноук (β-нафтоксиуксусная кислота)
- •5.2 Гиббереллины
- •5.3 Цитокинины
- •5.3.1 Дифенилмочевина и ее производные
- •5.3.1.1 Синтез дифенилмочевины
- •5.3.1.2 Синтез тидиазурона [n-фенил-n'-(1,2,3-тиадиазол-5-ил)мочевины]
- •5.4 Другие стимуляторы роста растений
- •5.4.1 Фурановые соединения
- •5.4.1.1 Синтез гидрофуранона:
- •5.4.2 Натриевые соли нафтеновых кислот
- •6 Экспериментальная часть
- •6.1 Биологические испытания
- •7 Заключение
- •8 Список использованных источников
5.1.1.1 Синтез 4х
В реактор объемом 0,5 л загружают ФУК следующего состава: ФУК 87,0; NaCl 4,8; влага 8,0; фенол 0,2; ледяную уксусную кислоту и уксусный ангидрид. Реакционную массу подогревают до 50°C и начинают подачу хлора. Охлаждают реакционную массу при перемешивании до 11°C и отфильтровывают выпавшую 4-хлорфеноксиуксусную кислоту. Тщательно отжимают уксусную кислоту и промывают 4-хлорфеноксиуксусную кислоту водой, высушивают. [5]
5.1.2 Имк [гамма-(индолил-3)-масляная кислота]
Не содержащаяся в высших растениях ИМК во многих случаях влияет на физиологические процессы так же, как ИУК, но отличается от последней относительно высокой персистентностью.
Представляет собой белое кристаллическое вещество с температурой плавления 124°C, хорошо растворимое в этиловом спирте и многих других органических растворителях. [1]
5.1.2.1 Синтез имк
А. Получение кетокислоты. Реакция протекает по схеме:
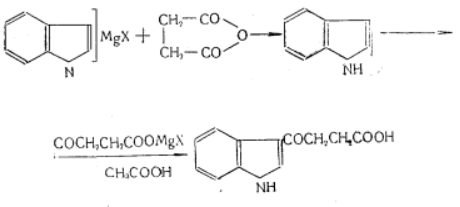
В сухую трехгорлую круглодонную колбу емкостью 500 мл, снабженную мешалкой с затвором, обратным шариковым холодильником и капельной воронкой, помещают магниевую стружку и анизол и затем медленно приливают в течение 1,5-2 час. иодистый этил. В полученный этил магний-иодид при охлаждении в ледяной воде вводят по каплям раствор индола.
K приготовленному раствору индолил магний-иодида, охлажденному до комнатной температуры, быстро приливают горячий раствор янтарного ангидрида.
Затем к смеси приливают разбавленную уксусную кислоту. Выделившуюся кетокислоту отфильтровывают, тщательно отжимают и промывают несколько раз водой. Фильтрат переносят в делительную воронку, где довольно быстро отделяется анизольный слой, из которого анизол может быть легко и с хорошим выходом регенерирован.
Перед восстановлением продукт подвергают щелочному переосаждению и обработке активированным углем.
Б. Восстановление кетокислоты в гамма-(индолил-3)-масляную кислоту.
Реакция протекает по схеме:

К цинковой пыли (амальгамированной) приливают раствор кетокислоты. Смесь нагревают до кипения при хорошем перемешивании и медленно прибавляют по каплям соляную кислоту. Бутанольный раствор ИМК помещают в прибор для перегонки с паром, смешивают с раствором едкого натра и через смесь пропускают водяной пар до полной отгонки бутанола. Оставшийся щелочной раствор, обычно содержащий небольшое количество бурого хлопьевидного осадка, нагревают до кипения с углем и фильтруют. Фильтрат охлаждают и подкисляют разбавленной соляной кислотой. Затем медленно при перемешивании прибавляют соляную кислоту. Осадок после отжимания на воронке промывают несколько раз холодной водой до удаления соляной кислоты в промывных водах и затем высушивают сначала на воздухе, а потом в эксикаторе.
Для очистки технический продукт перекристаллизовывают из бензола и получают чистую гамма-(индолил-3)-масляную кислоту. [6]
5.1.3 Нук (α-нафтилуксусная кислота)
Физиологический аналог фуксина. Используется в качестве эффективного регулятора роста растений. Производится в виде калиевой соли, амида или метилового эфира. Наибольшее значение имеет калиевая соль α-нафтилуксусной кислоты (КАНУ).
Белое кристаллическое вещество с температурой плавления 131-132°C. Растворимость в 100 мл воды при 25°C 41-42 мг.
