
- •1 Реферат
- •2 Содержание
- •3 Обозначения и сокращения
- •4 Введение
- •5 Обзор литературы
- •5.1 Ауксины
- •5.1.1.1 Синтез 4х
- •5.1.2 Имк [гамма-(индолил-3)-масляная кислота]
- •5.1.2.1 Синтез имк
- •5.1.3 Нук (α-нафтилуксусная кислота)
- •5.1.4 Ноук (β-нафтоксиуксусная кислота)
- •5.2 Гиббереллины
- •5.3 Цитокинины
- •5.3.1 Дифенилмочевина и ее производные
- •5.3.1.1 Синтез дифенилмочевины
- •5.3.1.2 Синтез тидиазурона [n-фенил-n'-(1,2,3-тиадиазол-5-ил)мочевины]
- •5.4 Другие стимуляторы роста растений
- •5.4.1 Фурановые соединения
- •5.4.1.1 Синтез гидрофуранона:
- •5.4.2 Натриевые соли нафтеновых кислот
- •6 Экспериментальная часть
- •6.1 Биологические испытания
- •7 Заключение
- •8 Список использованных источников
5 Обзор литературы
На рост растений могут оказывать влияние как эндогенные, так и экзогенные вещества. Ниже будут рассмотрены и те, и другие: их строение, функции, механизм (если он известен), а также синтез.
Фитогормоны — это вещества, которые принадлежат к эндогенным регуляторам роста растений, они образуются в растении и участвуют в регуляции обмена веществ на всех этапах его жизни. [1]
Фитогормоны делят на 5 больших групп: ауксины, гиббереллины,
цитокинины, этилен, абсцизовая кислота. [2]
Под действием фитогормонов и экзогенных соединений, стимулирующих рост растений, происходит быстрое удлинение стебля растений, усиление роста, стимуляция цветения и увеличение числа завязей. К активным стимуляторам роста относятся гибберелловые кислоты (гиббереллины) — см. рис. 1, ауксины и гетероауксины. [3]
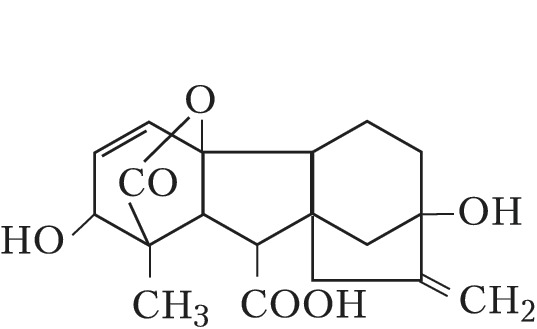
Рис. 1 — Гибберелловая кислота
5.1 Ауксины
Ауксин — первый обнаруженный и наиболее изученный фитогормон. Попытку химической идентификации ауксина впервые предпринял голландский исследователь Кегль, который обнаружил в моче, фекалиях и дрожжах 3-индолилуксусную кислоту. [1]
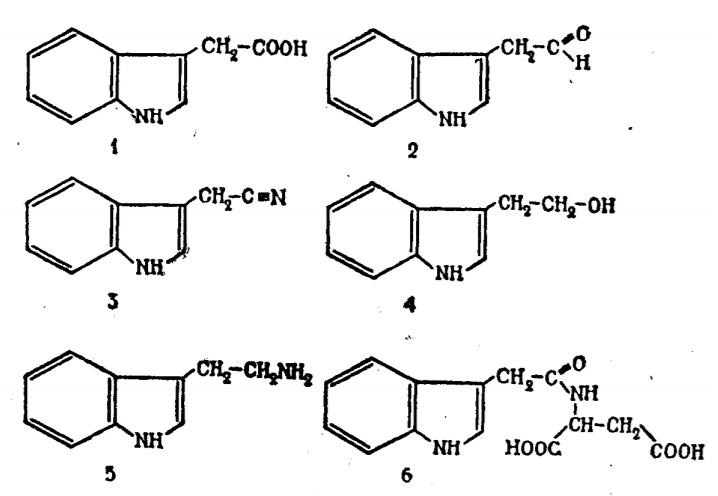
Рис. 2 — Индолилуксусная кислота и ее производные
1 — индолил-3-уксусная кислота; 2 — индолил-3-ацетальдегид; 3 — индолил-3-ацетонитрил; 4 — индолил-3-этанол; 5 — триптамин; 6 — индолил-3-ацетил-N-аспарагиновая кислота.
Наибольшее значение приобрел гетероауксин, представляющий по строению p-индолилуксусную кислоту (рис. 3, а). В настоящее время его готовят в промышленном масштабе и используют в сельском хозяйстве.

Рис. 3 — Гетероауксин и родственные ему соединения
Получены различные аналоги гетероауксина и родственные ему соединения. Например, альфа-нафтилуксусная кислота (рис. 3, б), которая отличается от него по своему действию — задерживает цветение растений, что позволяет уберечь их от гибели при заморозках. [4]
Ауксиновая активность обнаружена у большого числа соединений, среди которых можно отметить производные фенилуксусной, феноксиуксусной, бензойной кислот, 1-нафтилуксусную кислоту и другие.
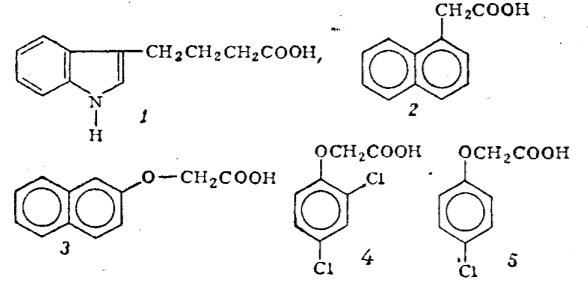
Рис. 4 — Некоторые синтетические аналоги ауксина.
1 — γ-(индолил-3)-масляная кислота; 2 — альфа-нафтилуксусная кислота; 3 — бета-нафтоксиуксусная кислота; 4 — 2,4-дихлорфеноксиуксусная кислота; 5 — 4-хлорфеноксиуксусная кислота.
Помимо участия в тропизмах, для ауксина были установлены и другие эффекты, такие как стимуляция камбиальной активности, роста партенокарпических плодов, образование корней и каллуса, задержка распускания боковых почек и опадания листьев и т. д.
Среди различных гомологов ИУК соединения с четным числом углеродных атомов в боковой цепи обладали более высокой активностью, чем соединения с нечетным числом этих атомов, а индолилкарбоновая кислота вообще не активна. Один из гомологов — индолилмасляная кислота (ИМК) — нашел широкое практическое применение, обладая более высокой активностью в качестве стимулятора образования корней, чем ИУК. Считается, что такой характер зависимости активности от длины боковой цепи определяется тем, что при четном числе углеродных атомов в боковой цепи в результате бета-окисления происходит превращение гомологов в соответствующие уксусные кислоты, а при нечетном числе такое превращение осуществляется с трудом или же приводит к образованию неактивных карбоновых кислот.
Замена одного атома водорода
в боковой цепи ИУК, НУК или 2,4-Д на CH3
приводит к образованию соответствующих
α-пропионовых кислот. При этом возможны
два оптических изомера этих кислот.
Было установлено, что ауксиновая
активность зависит от оптической
изомерии. Например, (+)-изомер
индолил-α-пропионовой кислоты обладал
примерно в 30 раз более высокой активностью,
чем (—)-изомер. При замене обоих атомов
водорода в
 -группе
боковой цепи образуются изомасляные
гомологи ИУК, НУК, 2,4-Д и других синтетических
аналогов ауксина. Эти соединения либо
не обладают ауксиновой активностью,
либо действуют как антиауксины.
-группе
боковой цепи образуются изомасляные
гомологи ИУК, НУК, 2,4-Д и других синтетических
аналогов ауксина. Эти соединения либо
не обладают ауксиновой активностью,
либо действуют как антиауксины.
Введение галогена вместо водорода в ароматическом кольце ИУК, приводящее к образованию 4-хлор-ИУК или 6-хлор-ИУК, также значительно повышает ауксиновую активность. При этих замещениях важное значение имеет взаимное расположение заместителей и ацетильной группы. Например, 2,4-Д и 2,4,5-Т очень активны как ауксины и гербициды, тогда как 2-хлорфеноксиуксусная кислота, 3,5-Д и 2,4,6-Т либо неактивны, либо действуют как антиауксины. [1]
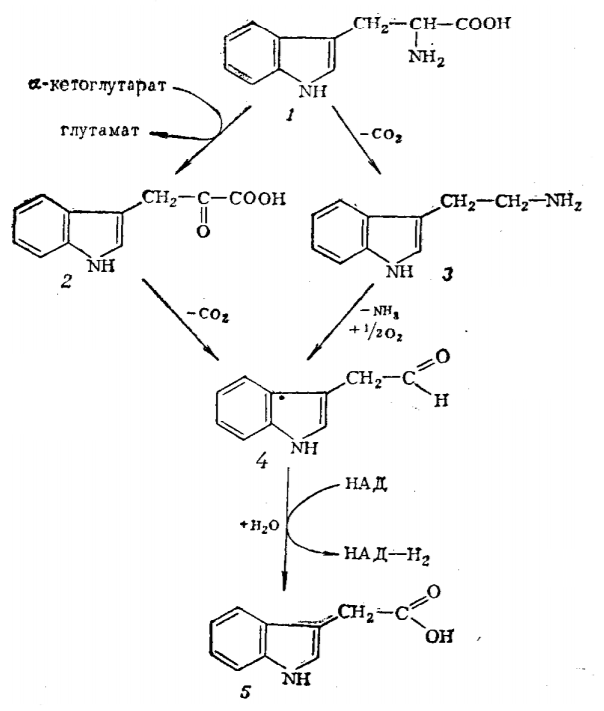
Рис. 5 — Схема путей биосинтеза ИУК
1 — триптофан; 2 — индолил-3-ПВК; 3 — триптамин; 4 — индолил-3-ацетальдегид; 5 — индолил-3-уксусная кислота, НАД и НАД*H2 — окисленный и восстановленный никотинадениннуклеотид.
Есть несколько путей биосинтеза ИУК из триптофана. В основном пути L-Trp под действием трансаминазы превращается в индол-2-пируват, который после декарбоксилирования и окисления превращается в ИУК. Часть ИУК в растениях может иметь бактериальное происхождение. Такое наблюдается в случае заражения бактериями корончатого галла (Agrobacterium tumefaciens). В ходе заражения происходит трансформация растительных клеток плазмидой, несущей гены, отвечающие за неконтролируемый растениями синтез ИУК.
5.1.1 2,4-Д, 4Х и другие феноксикислоты
В качестве регулятора роста используют обычно соли 2,4-Д, хорошо растворимые в воде. Он является физическим аналогом эндогенного ауксина, отличаясь от последнего более высокой персистентностью. Однако эксперименты показали, что применение 2,4-Д в дозах, необходимых для проявления росторегулирующей способности, является фитотоксичным.
В некоторых ситуациях все-таки удается реализовать росторегулирующую активность без фитотоксичности (например, для предотвращения предуборочного опадения цитрусовых).
4-хлорфеноксиуксусная кислота (4Х) обладает гораздо меньшей по сравнению с 2,4-Д фитотоксичностью, что позволяет использовать ее для улучшения плодообразования у томатов. [1]
