
- •Бабичев р.К., синявский г.П. Физика Практикум
- •Содержание
- •Введение
- •Лабораторные работы по механике. Лабораторная работа № 1. Изучение движения тела в поле силы тяжести. Краткая теория.
- •Порядок выполнения работы.
- •Изучение движения тела, брошенного вертикально.
- •Изучение движения тела, брошенного горизонтально.
- •Изучение движения тела, брошенного с земли под углом к горизонту.
- •Изучение движения тела, брошенного с некоторой высоты под углом к горизонту.
- •Контрольные вопросы.
- •Лабораторная работа № 2. Упругие и неупругие соударения.
- •Типы соударений.
- •Опыт 1.
- •Опыт 2.
- •2. Контрольное задание.
- •Контрольные вопросы.
- •Лабораторная работа № 3. Изучение пружинного маятника.
- •1 . Краткая теория.
- •2. Изучение силы упругости и потенциальной энергии пружины.
- •3. Изучение свободных колебаний пружинного маятника.
- •4. Изучение затухающих колебаний пружинного маятника.
- •Контрольные вопросы.
- •Лабораторная работа № 4. Исследование продольных и поперечных механических волн
- •1. Краткая теория.
- •2. Исследование поперечных волн.
- •Контрольное задание 1.
- •Задание повышенной сложности.
- •3. Исследование продольных волн в твердом теле и жидкости.
- •Контрольное задание 2.
- •Задание повышенной сложности.
- •4. Исследование продольных волн в газе.
- •Контрольное задание 3.
- •Задание повышенной сложности.
- •5. Определение Сp/Сv по скорости звука в газе.
- •Факультативное задание.
- •Контрольные вопросы.
- •Лабораторные работы по термодинамике и статистической физике Лабораторная работа № 5. Основные термодинамические процессы.
- •1. Изобарный процесс.
- •2. Изучение изобарного процесса.
- •Контрольное задание.
- •Контрольные вопросы.
- •3. Изохорный процесс.
- •4. Изучение изохорного процесса.
- •Контрольное задание.
- •Контрольные вопросы.
- •5 . Изотермический процесс.
- •При изотермическом расширение работа определяется выражениями
- •6. Изучение изотермического процесса.
- •Контрольное задание.
- •Контрольные вопросы.
- •7. Адиабатный процесс.
- •8. Изучение адиабатного процесса.
- •Контрольное задание.
- •Контрольные вопросы.
- •Лабораторная работа № 6. Работа газа.
- •1. Работа газа.
- •Контрольное задание.
- •Контрольные вопросы.
- •Лабораторная работа № 7. Термодинамические циклы.
- •Контрольное задание.
- •Контрольные вопросы.
- •Лабораторная работа № 8. Цикл Карно.
- •1. Краткая теория.
- •2. Исследование цикла Карно.
- •Контрольное задание 1.
- •Условия задания.
- •Данные для конкретного варианта:
- •Контрольные вопросы.
- •Лабораторная работа № 9. Изотермы реального газа.
- •Определения.
- •2. Диаграммы состояний насыщенных и ненасыщенных паров.
- •3. Критическая точка вещества
- •4. Изучение изотерм реального газа
- •Контрольное задание.
- •Контрольные вопросы.
- •Порядок выполнения работы.
- •Проведение измерений.
- •Порядок выполнения задания 1:
- •Порядок выполнения задания 2:
- •Порядок выполнения задания 3:
- •Порядок выполнения задания 4:
- •Лабораторная работа № 10 (часть 2). Напряженность, силовые линии и потенциал электрического поля.
- •Краткая теория
- •Ознакомительная часть.
- •Проведение измерений.
- •Порядок выполнения задания 1:
- •Порядок выполнения задания 2:
- •Контрольные вопросы
- •Лабораторная работа № 11 (часть 1). Закона Ома для цепи постоянного тока.
- •1. Замкнутая электрическая цепь.
- •Порядок выполнения работы.
- •Опыт 1.
- •Опыт 2.
- •2. Закон Ома для всей цепи.
- •Опыт 3.
- •Опыт 4.
- •3. Закон Ома для участка цепи.
- •Задание 1.
- •Лабораторная работа № 11 (часть 2). Контрольное задание.
- •4. Зависимость между эдс источника электрической энергии и напряжением на его зажимах.
- •5. Контрольное задание.
- •Контрольные вопросы.
- •Лабораторная работа № 12. Взаимодействие параллельных токов.
- •Краткая теория
- •2. Изучение магнитного поля и силы взаимодействия двух параллельных проводников с токами
- •Контрольное задание 1
- •Контрольное задание 2
- •Контрольные вопросы
- •Лабораторная работа №13 (часть1). Движение заряда в электрическом поле.
- •1. Краткая теория.
- •2. Движение заряда в электрическом поле
- •Контрольное задание 1
- •Задание повышенной сложности.
- •Порядок выполнения работы
- •Движение заряда по окружности Контрольное задание 2
- •Движение заряда по винтовой линии Контрольное задание 3
- •Контрольные вопросы
- •Лабораторная работа №14. Генератор переменного тока.
- •Краткая теория
- •2. Исследование генератора переменного тока
- •Контрольное задание 1
- •Контрольное задание 2
- •Контрольные вопросы
- •Лабораторная работа № 15 (часть 1). Свободные колебания в rlc-контуре.
- •Краткая теория
- •2. Изучение свободных колебаний в rlc-контуре
- •Контрольное задание 1
- •Лабораторная работа №15 (часть 2). Вынужденные колебания в rlc-контуре.
- •3. Краткая теория
- •2. Изучение вынужденных колебаний в rlc-контуре Контрольное задание 2
- •Контрольные вопросы
- •2. Исследование колец Ньютона
- •Контрольное задание 1
- •Лабораторная работа № 16 (часть 2). Интерференция. Опыт Юнга
- •3. Краткая теория
- •4. Исследование интерференционной картины в опыте Юнга
- •Контрольное задание 2
- •Лабораторная работа 16 (часть 3). Контрольное задание. Контрольное задание 3 (повышенной сложности)
- •5. Контрольные вопросы
- •Лабораторная работа №17 (часть 1). Дифракция.
- •1. Краткая теория
- •2. Исследование дифракции света
- •Контрольное задание 1
- •Лабораторная работа №17 (часть 2). Зоны Френеля
- •3. Краткая теория
- •4. Исследование зон Френеля
- •Контрольное задание 2
- •Лабораторная работа № 18 (часть 1). Фотоэффект.
- •1. Краткая теория
- •2. Исследование фотоэффекта
- •Контрольное задание 1
- •Лабораторная работа № 18 (часть 2). Комптоновское рассеяние.
- •3. Краткая теория
- •4. Исследование комптоновского рассеяния
- •Контрольное задание 2
- •Контрольные вопросы
Контрольные вопросы.
1. Что называют адиабатным процессом?
2. Запишите уравнение Пуассона для адиабатного процесса.
3. Что называют адиабатой? Изобразите адиабату в координатах P,V.
4. Как определяется работа при адиабатном расширении или сжатии?
5. Как записывается первый закон термодинамики для адиабатного процесса?
Лабораторная работа № 6. Работа газа.
1. Работа газа.
В отличие от твердых и жидких тел газы могут сильно изменять свой объем. При этом совершается механическая работа.
Пусть газ находится в цилиндре с подвижным поршнем. Если нагреть газ, то он расширится и переместит поршень, действуя на него с некоторой силой F, на расстояние х. Свободное перемещение поршня позволяет внутри газа поддерживать давление, равное внешнему, то есть этот процесс изобарный. Газ при расширении совершает работу
A = Fх или A = PSх,
где S – площадь поршня, а P – давление в газе. Через изменение объема работу можно записать в виде
A = PV.
Так как газ расширяется, то V = V2 –V1 0 и работа газа положительна A 0). При сжатии газа V 0 и работа внешних силотрицательнаA 0).
Рассмотрим общий случай, когда при изменении объема давление тоже изменяется.
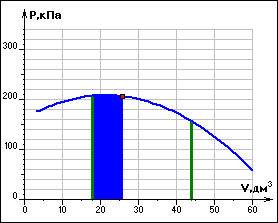
Если объем газа изменяется на очень малую величину dV, то при этом можно давление считать постоянным и определять элементарную работу по формуле для изобарного процесса: dA = PdV, а полная работа при переходе газа из некоторого начального состояния (1) в конечное состояние (2) математически выражается формулой
![]() т.е.
т.е.
![]()
Она численно равна площади под кривой, описывающей процесс на (P,V) диаграмме. Из рисунка видно, что работа расширения газа от V1 до V2 равна работе внешних сил, сжимающих газ от V2 до V1.
Величина работы зависит от того, каким путем совершался переход из начального состояния в конечное.
Компьютерная модель для моля одноатомного идеального газа, которая используется в работе, позволяет определять работу в случаях, когда кривая P(V) имеет вид прямой, параболы и экспоненты. Для установки начального или конечного состояний газа необходимо сначала подвести курсор к красному или зеленому квадратику так, чтобы курсор принял вид кисти руки. Затем следует нажать левую кнопку мыши (при этом на курсоре в виде кисти руки пальцы сожмутся) и при нажатой кнопке мыши переместить квадратик в нужное место, в случае красного квадратика контролируя в окошке заданные значения P и V, и кнопку мыши отпустить.
Контрольное задание.
Теперь вы должны выполнить указанный преподавателем вариант контрольного задания. Полученные результаты необходимо занести в лабораторную тетрадь.
Вариант 1. Моль одноатомного идеального газа совершает процесс, в ходе которого давление растет пропорционально объему. В начальном состоянии газ имеет объем V1 = 10 л и давление P1 = 100 кПа, а в конечном - объем V2 = 50 л и давление P2 = 300 кПа. Найти температуры T1 и T2, соответствующие начальному и конечному состояниям газа, и определить приращение внутренней энергии газа U, совершенную им работу A и теплоту Q, получаемую газом.
Вариант 2. Моль одноатомного идеального газа расширяется от V1 = 15 л до V2 = 45 л так, что процесс на диаграмме (P,V) имеет вид прямой линии. Исходное давление P1 = 250 кПа, конечное - P2 = 50 кПа. Найти изменение внутренней энергии газа U, совершенную им работу A и количество теплоты Q, поглощаемое газом в ходе расширения.
Вариант 3. Моль одноатомного идеального газа при неизменном давлении P = 200 кПа нагревается. Его объем увеличивается от V1 = 20 л до V2 = 40 л. Определить изменение U внутренней энергии газа, работу A, совершенную им при расширении, а также теплоту Q, сообщенную газу. Найти температуры T1 и T2, соответствующие начальному и конечному состояниям газа.
Вариант 4. Моль атомарного идеального газа переходит из состояния 1 с V1 = 10 л и P1 = 200 кПа в состояние 2 с V2 = 40 л и P2 = 300 кПа посредством процесса с параболической зависимостью P(V). Определить приращение внутренней энергии газа U, совершенную им работу A и теплоту Q, получаемую газом.
Вариант 5. Первоначально моль одноатомного газа заключен в объеме V1 = 15 л под давлением P1 = 250 кПа. Затем газ расширяется по параболе на диаграмме (P,V) и его объем становится равным V2 = 50 л, а давление - P2 = 50 кПа. Найти изменение U внутренней энергии газа, совершенную им работу A и теплоту Q, переданную газу.
Вариант 6. Моль одноатомного газа первоначально занимает объем V1 = 10 л и находится под давлением P1 = 200 кПа. Затем газ расширяется по параболе на диаграмме (P,V) до объема V2 = 50 л с давлением P2 = 200 кПа. Определить приращение внутренней энергии газа U, совершенную им работу A и теплоту Q, получаемую газом. Найти температуры T1 и T2, соответствующие начальному и конечному состояниям газа.
Вариант 7. Моль атомарного идеального газа переходит из состояния 1 с V1 = 10 л и P1 = 50 кПа в состояние 2 с V2 = 40 л и P2 = 300 кПа посредством процесса с нарастающей экспоненциальной зависимостью P(V). Определить приращение внутренней энергии газа U, совершенную им работу A и теплоту Q, получаемую газом.
Вариант 8. Первоначально моль одноатомного газа заключен в объеме V1 = 15 л под давлением P1 = 250 кПа. Затем газ расширяется по убывающей экспоненте на диаграмме P, V и его объем становится равным V2 = 50 л, а давление - P2 = 50 кПа. Найти изменение U внутренней энергии газа, совершенную им работу A и теплоту Q, переданную газу.
Вариант 9. Моль одноатомного газа первоначально занимает объем V1 = 10 л и находится под давлением P1 = 250 кПа. Затем газ расширяется по экспоненте на диаграмме (P,V) до объема V2 = 50 л с давлением P2 = 300 кПа. Определить приращение внутренней энергии газа U, совершенную им работу A и теплоту Q, получаемую газом. Найти температуры T1 и T2, соответствующие начальному и конечному состояниям газа.
Вариант 10. Моль одноатомного газа нагревался при постоянном давлении P = 100 кПа, в результате чего его объем изменился от V1 = 10 л до объема V2. При этом ему была сообщена теплота Q = 8,58 кДж. Какую работу A совершил при этом газ? Каково было изменение U внутренней энергии? Чему равен конечный объем V2?
Вариант 11. Первоначально моль одноатомного газа заключен в объеме V1 = 50 л под давлением P1 = 50 кПа. Затем газ сжимается по параболе на диаграмме (P,V) и его объем становится равным V2 = 10 л, а давление - P2 = 250 кПа. Найти изменение U внутренней энергии газа, совершенную над ним работу A и теплоту Q, переданную газом.
Вариант 12. Моль одноатомного газа первоначально занимает объем V1 = 40 л и находится под давлением P1 = 250 кПа. Затем газ сжимают по экспоненте на диаграмме (P,V) до объема V2 = 15 л с давлением P2 = 100 кПа. Определить убыль внутренней энергии газа U, совершенную над ним работу A и теплоту Q, отданную газом. Найти температуры T1 и T2, соответствующие начальному и конечному состояниям газа.
