
Наглядная химия. Арены (pdf)
.pdf
1
Особенности строения, реакционной способности и методы синтеза аренов
Ароматические соединения, или арены, — большая группа соединений карбоциклического ряда, молекулы которых содержат устойчивую циклическую группировку из тести атомов углерода (бензольное кольцо), обладающую особыми физическими и химическими свойствами.
1. Ароматические соединения с одним бензольным ядром
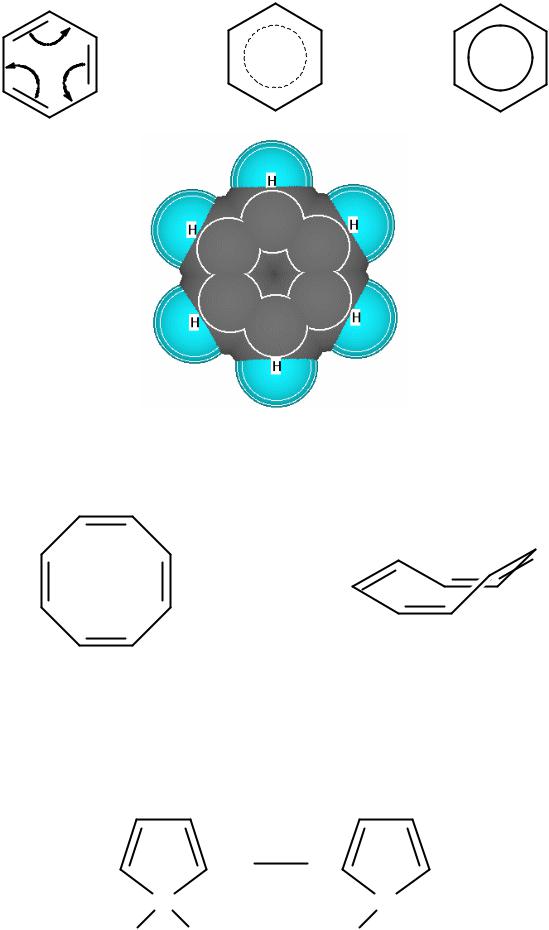
Строение молекулы бензола
Бензол (бензен) С6Н6
А. Кекуле (1865):
H
H C H
C C
C C
H C H
H

2
3
2. "Ароматичность" - совокупность особых свойств бензола
Э.Хюккель (1931):
Правило Хюккеля: плоские циклические соединения, имеющие сопряженную систему π -электронов, могут быть ароматическими. если число этих электронов равно 4п + 2 (где п = 0. 1, 2,3 и т.д.).
-H+
C C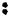 H H H
H H H
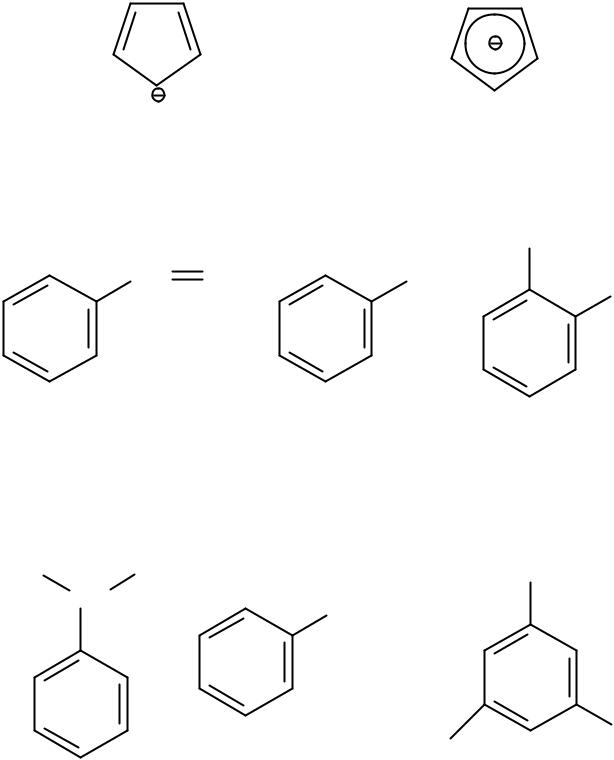
3. Номенлатура и изомерия
Арены
CH CH2 |
CH3 |
стирол |
толуол |
(винилбензол) |
(метилбензол) |
CH3 CH3
CH |
OCH3 |
|
CH3
кумол |
анизол |
4
CH3
CH3
о-ксилол
(1,2-
диметилбензол)
CH3
CH3
мезителен
(изопропилбензол) (метоксибензол) (1,3,5-триметилбензол)
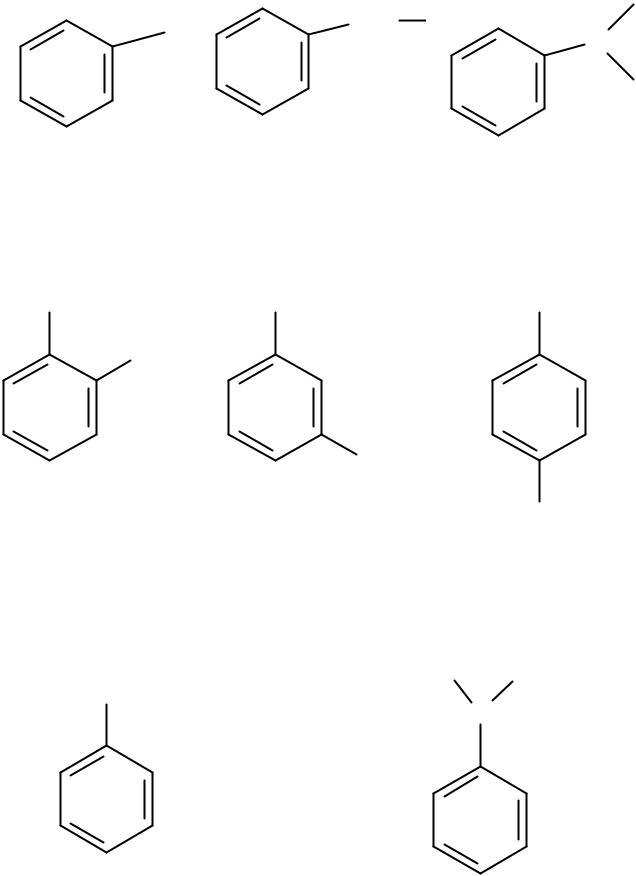
CH2
фенил |
бензил |
Изомерия |
|
CnH2n-6 |
|
CH3 |
CH3 |
|
CH3 |
CH3
о-ксилол |
м-ксилол |
(1,2-диметилбензол) |
(1,3-диметилбензол) |
5
CH
бензилиден
CH3
CH3
п-ксилол (1,4-диметилбензол)
CH3 |
CH3 |
CH2CH2CH3 |
CH |
|
пропилбензол |
изопропилбензол (кумол) |
6
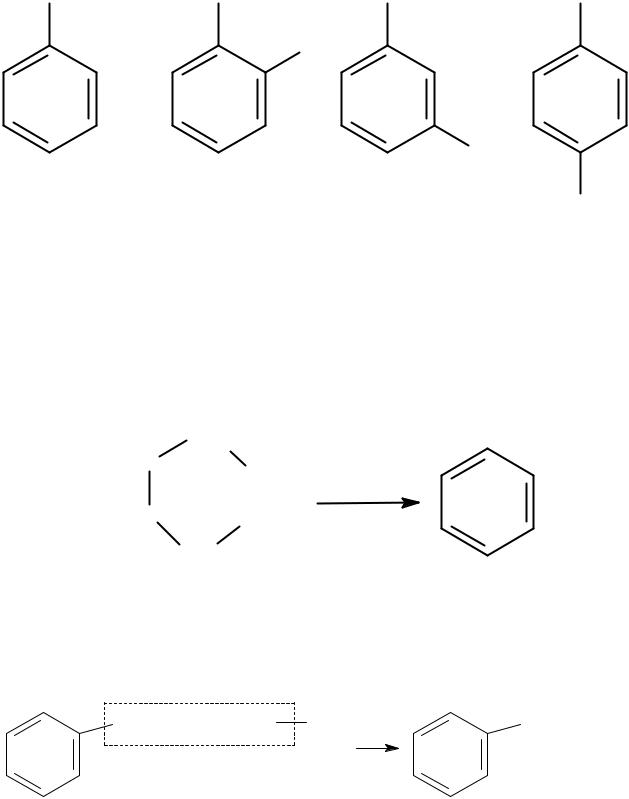
CH2CH3 |
CH3 |
CH3 |
CH3 |
|
|
C |
|
|
|
|
C |
|
|
|
CH3 |
этилбензол |
о-ксилол |
м-ксилол |
п-ксилол |
4.Способы получения
1)Ароматизация алканов:
H2C |
CH2 |
|
|
CH3 |
Cr2O3 |
||
H2C |
|||
CH |
-4H2 |
||
|
3 |
|
|
|
CH2 |
бензол |
|
|
гексан |
2) Реакция Вюрца—Фиттига
Br + 2Na + Br C2H5 |
C2H5 |
+ 2NaBr
бромбензол |
этилбензол |
7
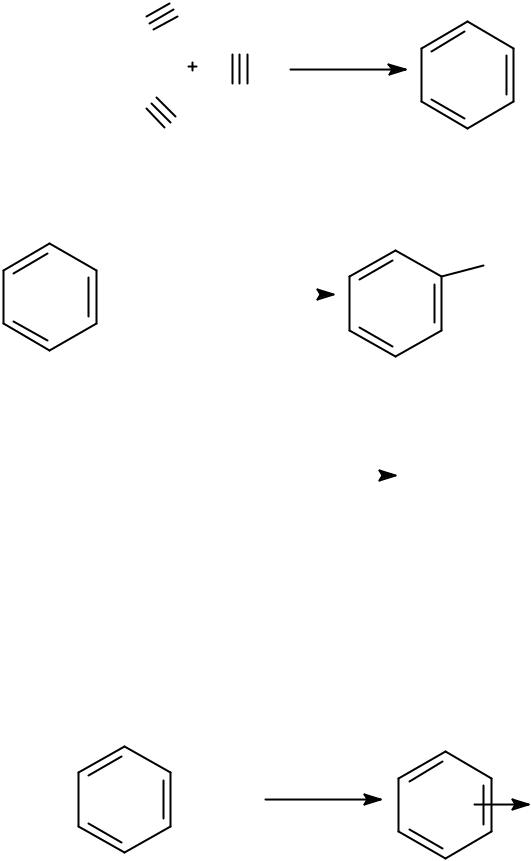
3) Синтез из ацетилена
CH
CH CH
HC CH
CH
C (актив.) 400°С
бензол
4) Реакция Фриделя—Крафтса: |
|
||
+ C2H5Cl |
AlCl3 |
C2H5 |
|
+ HCl |
|||
|
|||
этилбензол
5) Синтез из солей ароматических кислот:
C6H5 |
|
COONa + NaOH |
|
C6H5 + Na2CO3 |
|
|
|||
бензоат натрия |
|
|
||
5. Химические свойства
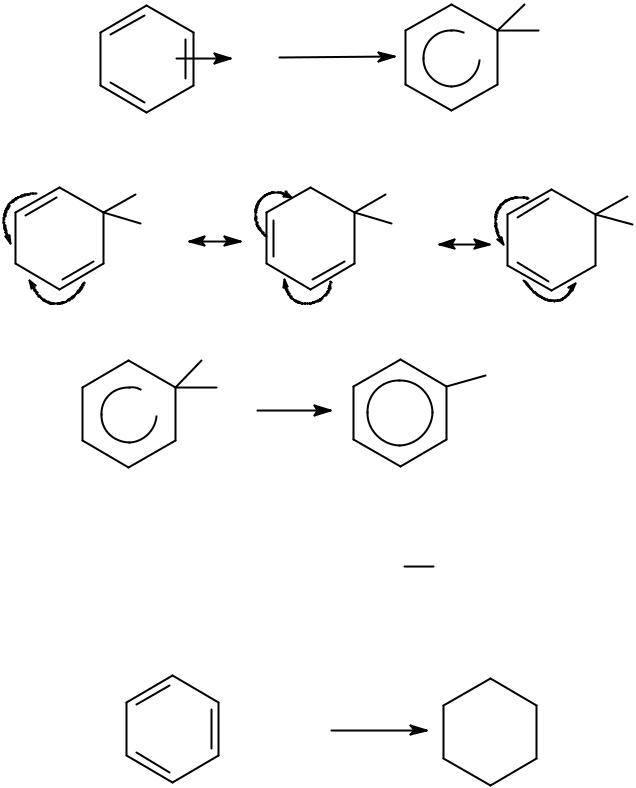
Реакции замещения (SE)
X + Y 
 X+ + Y-
X+ + Y-
+ X+ |
медленно |
X+ |
|
|
π -комплекс |
8
X
|
X+ медленно |
H |
|
|
+ |
||
π -комплекс |
|
σ -комплекс |
|
X |
+ |
X |
|
H |
H |
||
|
|||
+ |
|
+ |
|
X |
|
X |
|
H |
|
|
+ |
|
+ H+ |
|
|
быстро |
||
|
|
|
|
σ -комплекс |
|
|
замещенный |
|
|
бензол |
|
|
|
|
X H
H+ + Y- 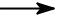 H Y
H Y
Реакции присоединения
+ 3H2 Pt, 150°C
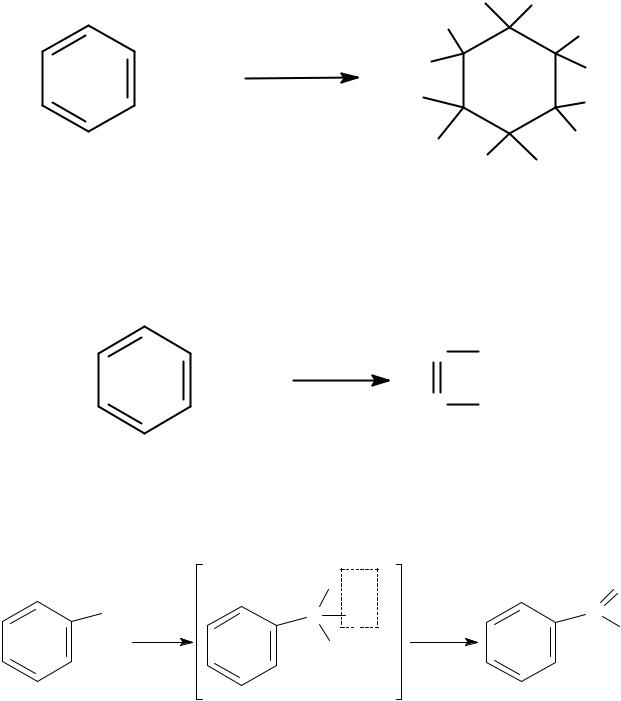
9
|
|
H Cl |
H |
|
|
|
Cl |
||
|
|
Cl |
|
|
+ 3Cl2 |
hv, -40°C |
|
H |
|
|
|
H |
|
Cl |
|
|
Cl |
H |
H |
|
|
|
Cl |
|
Реакции окисления
+ 4O V2tO5
HC COOH HC COOH
малеиновая
кислота
|
|
OH |
O |
CH3 |
[O] |
C OH |
C |
|
OH |
OH |
|
|
|
-H2O |
|
толуол |
|
|
бензойная |
|
|
|
|
|
|
|
кислота |
10
CH3 |
COOH |
[O] t
CH3 |
CH |
CH3 |
COOH |
|
п-метилизопропил- |
терефталевая |
|||
бензол (цимол) |
кислота |
|||
2C2H6 |
+ |
3O2 |
|
12C + 6H2O |
|
||||
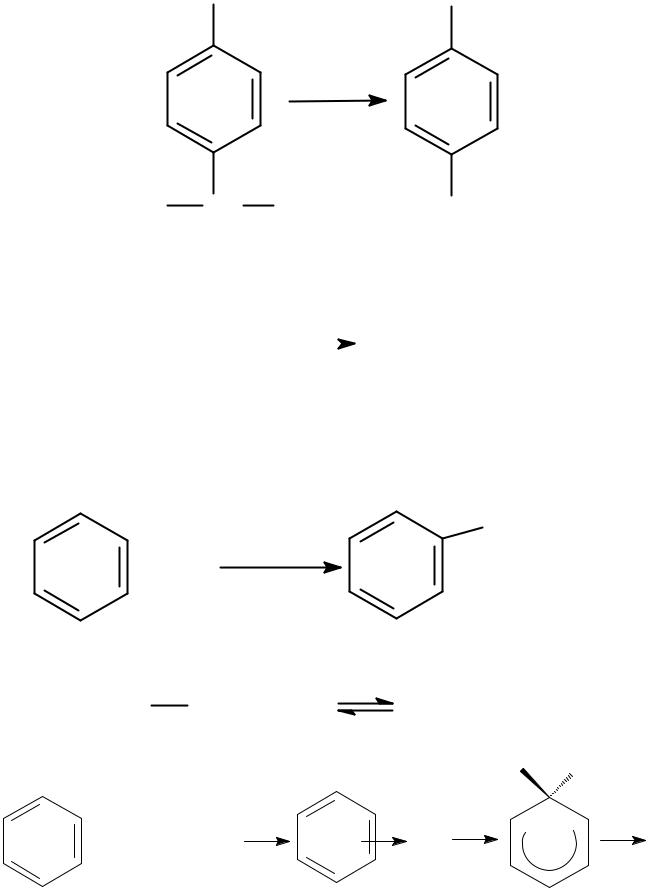
6. Реакции электрофильного замещения в ароматическом ряду
Галогенирование
|
FeCl3, 25°C |
Cl |
|
|
|
+ HCl |
|
+ Cl2 |
|
||
|
хлорбензол |
|
|
Cl |
Cl + FeCl |
Cl+[FeCl4]- |
|
|
3 |
|
|
|
|
Cl |
H |
+ Cl+[FeCl4]- |
Cl+ |
+ |
|
|
π -комплекс |
σ -комплекс |
|
