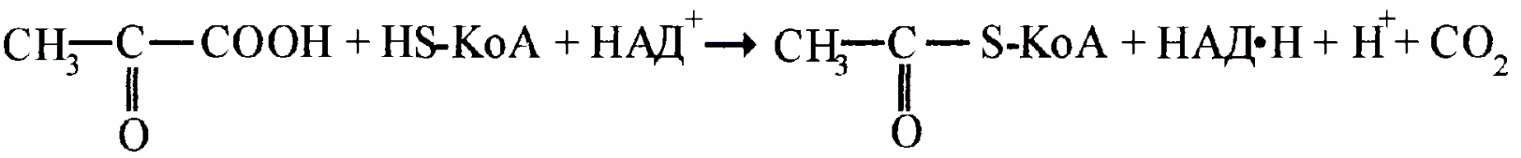- •«Молекулярные основы биоэнергетических процессов и общие пути катаболизма в организме человека . Ферменты»
- •Мультиферментные комплексы
- •Факторы, влияющие на скорость ферментативных реакций
- •Способы регуляции активности ферментов
- •Ковалентная (химическая) модификация
- •Диагностика энзима в моче
- •1. Обратимое 2. НеобратимоеА. Конкурентное а. Специфическое б. Неконкурентное б. Неспецифическое
- •Наследственные энзимопатии по типу нарушений метаболизма делят на:
- •Стадии метаболизма
- •Обмен веществ.Метаболические пути. Унификация питательных веществ.
- •Роль в организме
- •Энергетический эффект цикла Кребса Итак, при распаде 1 моль ацетил-КоА образуется 12 моль атф, следовательно, из 2 моль ацетил-КоА - 24 моль атф.
- •Механизм : Окислительное фосфорилирование
- •Специфические и общие пути катаболизма
- •Окислительное декарбоксилирование пировиноградной кислоты (пвк)
- •Окислительное декарбоксилирование пировиноградной кислоты (пвк)
Специфические и общие пути катаболизма
В катаболизме различают три стадии:
1). Полимеры превращаются в мономеры (белки – в аминокислоты, углеводы в моносахариды, липиды – в глицерол и жирные кислоты). Химическая энергия при этом рассеивается в виде тепла.
2). Мономеры превращаются в общие продукты, в подавляющем большинстве в ацетил-КоА. Химическая энергия частично рассеивается в виде тепла, частично накапливается в виде восстановленных коферментных форм (НАДН, ФАДН2), частично запасается в макроэргических связях АТФ (субстратное фосфорилирование).
1-ая и 2-ая стадии катаболизма относятся кспецифическим путям, которые уникальны для метаболизма белков, липидов и углеводов.
3). Заключительный этап катаболизма, сводится к окислению ацетил-КоА до СО2 и Н2О в реакциях цикла трикарбоновых кислот (цикла Кребса) – общий путь катаболизма. Окислительные реакции общего пути катаболизма сопряжены с цепью тканевого дыхания. При этом энергия (40-45%) запасается в виде АТФ (окислительное фосфорилирование).
В результате специфических и общих путей катаболизма биополимеры (белки, углеводы, липиды) распадаются до СО2, Н2О иNH3, которые являются основными конечными продуктами катаболизма.
КАТАБОЛИЗМ БЕЛКОВ
Белки подобно углеводам и липидам постоянно обмениваются, однако в отличии от углеводов и липидов белки прозапас не откладываются. Специфическим химическим элементом в составе белков является азот для которого характерен, т. н. азотистый баланс, у здорового человека поддерживается азотистое равновесие, т. к. количество азота поступившее с пищей равно количеству выделенного азота.
Начинается путь катаболизма белков с гидролиза (протеолиза) под действием ферментов протеазы и пептидазы.
Гидролиз белков начинается в желудке под действием фермента пепсина, этому способствует кислая среда желудочного сока рН=1-2 возникает благодаря выделению желудочных клеток соляной кислоты.
В тонком кишечнике при рН=7,8-8,4 , распад белков катализируется ферментами поджелудочной железы трипсином и химитрипсином.
АК – продукт гидролиза белков, поступающие из ЖКТ, являются важным фондом пополнения аминокислотного запаса клеток и тканей. Ограниченное поступление из вне даже одной из незаменимых АК вызывает резкий распад собственных белков тканей, АК используются в синтезе собственных белков, нуклеотидов, порфиринов и т. д.
В сутки взрослому человеку необходимо 100 г белка. Белки могут быть полноценными – в наличии все незаменимые АК и неполноценными – в наличии не все незаменимые АК. За сутки распадается и синтезируется 400 г белка. За 35 дней обновляются все белки.
О состоянии белкового обмена можно судить по азотистому балансу. Поскольку белки органов отличаются строгой видовой и тканевой специфичностью, живой организм обладает способностью использовать вводимый белок только в гидролизованном состоянии.
Всасывание АК через мембрану тонкого кишечника происходит под действием глутатиона. АК поступают в кровь воротной вены, затем в печень, где подвергаются ряду превращений.
Ацетилкофермент А, ацетил-коэнзим А, сокращённо ацетил-КоА — важное соединение в обмене веществ, используемое во многих биохимических реакциях. Его главная функция — доставлять атомы углерода с ацетил-группой в цикл трикарбоновых кислот, чтобы те были окислены с выделением энергии. По своей химической структуре ацетил-КоА — тиоэфир между коферментом А (тиолом) и уксусной кислотой (носителем ацильной группы). Ацетил-КоА образуется во время второго шага кислородного клеточного дыхания, декарбоксилирования пирувата, который происходит в матриксе митохондрии. Ацетил-КоА затем поступает в цикл трикарбоновых кислот.
Ацетил-КоА — важный компонент биологического синтеза нейротрансмиттера ацетилхолина. Холин, в соединении с ацетил-КоА, катализируется ферментом холин-ацетилтрансферазой, чтобы образовать ацетилхолин и коэнзим А.
----Обмен углеводов-Катаболизм углеводов
• Сопровождается освобождением энергии, которая может накапливаться в макроэргических связях АТФ и использоваться в дальнейшем для синтеза необходимых молекулярных компонентов клетки и совершения различных видов работы
• Образующиеся метаболиты служат исходными веществами для образования биологически важных соединений(аминокислоты, липиды, нуклеотиды),
41.Окислительное декарбоксилирование -кетокислот. Мех-м и регуляция окислительного декарбоксилирование пировиноградной кислоты.
А-кетокислота – это аминокаслота, в которой амино-группа замещена на кето-группу в а-положении. В результате окислительного декарбоксилирования пирувата образуются ацетил- КоА, восстановленный НАД и диоксид углерода: