
- •Передмова
- •Вступ до органічної хімії
- •1.1. Предмет органічної хімії
- •1.2. Короткий огляд історії розвитку органічної хімії
- •Глава 1 6
- •1.3. Розвиток теоретичних уявлень про будову органічних сполук
- •Глава 1
- •1.4. Способи зображення органічних молекул
- •Глава 1
- •2.1. Класифікація органічних сполук
- •Глава 2
- •2.2. Номенклатура органічних сполук
- •Глава 2
- •Глава 2
- •ХїмГчний зв'язок
- •3.1. Типи хімічних зв'язків
- •3.2. Хімічний зв'язок в органічних сполуках
- •3.2.1. Гібридизація атомних орбіталей
- •3.2.2. Ковалентні о- і я-зв'язки
- •3.2.3. Основні характеристики ковалентних зв'язків
- •4.1. Індуктивний ефект
- •Глава 40
- •4.2. Мезомерний ефект (ефект спряження)*
- •Глава 4
- •Глава 4
- •4.4. Надспряження (гіперкон'югація)
- •Глава 4
- •Класифікація ізомерії ізомерія
- •48 Глава 5
- •5.2. Просторова ізомерія (стереоізомерія)
- •Глава 5
- •5.3. Способи зображення просторової будови
- •Глава 5
- •6.1. Кислотність і основність за теорією бренстеда
- •Глава 6
- •6.2. Типи органічних кислот і основ
- •Глава 6
- •6.3. Кислоти і основи льюїса
- •7.1. Поняття про типи механізмів реакцій
- •Глава 7
- •7.2. Поняття про типи органічних реакцій
- •Глава 7
- •Вуглеводні
- •8.1. Електронна та просторова будова алканів
- •8.2. Номенклатура
- •8 .3. Ізомерія
- •8.4. Способи добування
- •8.4.1. Природні джерела
- •8.4.2. Синтетичні методи добування
- •8.5. Фізичні властивості
- •8.6. Хімічні властивості
- •8.6.1. Реакції радикального заміщення (5*)
- •76 Вуглеводні. Глава 8
- •8.6.2. Крекінг
- •8.7. Окремі представники. Застосування
- •1. Напишіть структурні формули наведених вуглеводнів і назвіть їх за раціональною номенклатурою:
- •2. Напишіть структурні формули таких вуглеводнів і назвіть їх за но менклатурою шрас:
- •Ц иклоалкани
- •9.1. Класифікація та номенклатура
- •9.2. Ізомерія
- •9.3. Способи добування. Фізичні властивості
- •9.4. Будова циклоалканів
- •9.5. Хімічні властивості
- •9.6. Окремі представники. Застосування
- •4 Органічна хімія
- •10.1. Номенклатура
- •Перші члени гомологічного ряду алкенів
- •100 Ненасичені вуглеводні. Глава іо
- •10.2. Ізомерія
- •10.3. Електронна і просторова будова алкенів
- •10.4. Способи добування
- •10.5. Фізичні властивості
- •10.6. Хімічні властивості
- •109 Ненасичені вуглеводні. Глава 10 108
- •1 0.6.1. Реакції електрофільного приєднання (ае)
- •10.6.2. Реакції відновлення та окиснення
- •10.6.3. Полімеризація алкенів
- •10.6.4. Алільне галогенування алкенів
- •118 Ненасичені вуглеводні. Глава ю
- •10.7. Окремі представники. Застосування. Ідентифікація
- •0 Контрольні питання та вправи
- •Алкадієни
- •11.2. Будова алкадієнів
- •11.1. Номенклатура
- •11.3. Алкадієни зі спряженими зв'язками 11.3.1. Способи добування
- •11.3.2. Хімічні властивості
- •11.3.3. Натуральний і синтетичний каучук
- •11.4 Окремі представники. Застосування
- •12.1. Номенклатура та ізомерія
- •12.2. Електронна та просторова будова молекул алкінів
- •12.3. Способи добування
- •138 Ненасичені вуглеводні. Глава т2
- •12.4. Фізичні властивості
- •12.5. Хімічні властивості
- •12.5.1. Реакції електрофільного приєднання (ае)
- •12.5.2. Реакції заміщення
- •12.6. Окремі представники. Застосування
- •Одноядерні арени
- •13.1. Будова бензену. Ароматичність
- •13.2. Номенклатура та ізомерія
- •13.3. Способи добування 13.3.1. Природні джерела
- •13.3.2. Синтетичні методи добування
- •13.4. Фізичні властивості
- •13.5. Хімічні властивості
- •13.5.1. Реакції електрофільного заміщення (5£)
- •0/1Ноядєрні аРени
- •13.5.2. Реакції приєднання
- •13.5.3. Реакції окиснення
- •13.5.4. Галогенування гомологів бензену з участю бокового ланцюга
- •165 0ДнояДерн[арени
- •13.6. Вплив замісників у бензеновому кільці на напрямок та швидкість реакцій
- •Електрофільного заміщення
- •13.7. Орієнтація в дизаміщеному бензені
- •1 3.8. Окремі представники. Застосування
- •13.9. Представники багатоядерних аренів
- •13.9.1. Нафтален
- •13.9.2. Антрацен
- •14.1. Природний та попутний нафтовий гази
- •Глава 14
- •14.2. Нафта. Нафтопродукти
- •14.3. Коксування вугілля
- •Глава 1і0у глава Глава 14 186 !
- •15.1. Класифікація та номенклатура
- •15.2. Ароматичність гетероциклів
- •Глава 15
- •15.3. Кислотно-осНбВні властивості гетероциклів
- •15.4. П'ятичленні гетероциклічні сполуки з одним гетероатомом
- •15.4.1. Способи добування
- •15.4.2. Фізичні властивості
- •15.4.3. Хімічні властивості
- •Глава 15
- •15.4.4. Найважливіші похідні піролу
- •Глава 15
- •15.5. Шестичленні гетероциклічні сполуки з одним гетероатомом
- •Глава 15
- •Глава 15
- •В. Реакції відновлення і окиснення
- •15.6. П'яти-1 шестичленні гетероцикли з двома гетероатомами
- •208 Глава 15
- •15.7. Представники конденсованих систем гетероциклів
- •16.1. Одноатомні спирти
- •16.1.1. Номенклатура
- •Глава 16
- •16.1.2. Ізомерія
- •16.1.3. Фізичні властивості
- •Глава 1
- •16.1.4. Способи добування
- •16.1.5. Хімічні властивості
- •16.1.6. Ідентифікація спиртів
- •16.1.7. Окремі представники
- •230 Глава 16
- •16.2.1. Способи добування дво- і триатомних спиртів
- •16.2.2. Фізичні властивості
- •16.2.3. Хімічні властивості
- •16.2.4. Окремі представники
- •16.3.2. Способи добування
- •16.3. Одноатомні феноли 16.3.1. Номенклатура та ізомерія
- •16.3.4. Хімічні властивості
- •16.3.3. Фізичні властивості
- •249 Гідроксильні похідні вуглеводнів
- •В. Реакції відновлення і окиснення
- •255 Гідроксильні похідні вуглеводнів
- •17.1. Номенклатура та ізомерія
- •17.2. Способи добування
- •17.3. Фізичні властивості
- •263 Цясимені альдегіди і кетони
- •269 Насичені альдегіди і кетони
- •271 ИаСйчені альдегіди і кетони
- •17.5. Окремі представники
- •Монокарбонові кислоти
- •18.1. Насичені монокарбонові кислоти
- •18.1.1. Номенклатура та ізомерія
- •18.1.3. Фізичні властивості
- •18.1.4. Хімічні властивості
- •А. Кислотні властивості
- •Г. Окиснення та відновлення
- •18.1.5. Окремі представники
- •18.2. Ненасичені монокарбонові кислоти
- •18.2.1. Номенклатура та ізомерія
- •18.2.2. Способи добування
- •18.2.4. Хімічні властивості
- •18.2.3. Фізичні властивості
- •18.2.5. Окремі представники
- •299 Монокарбонові кислоти
- •18.3. Ароматичні монокарбонові кислоти
- •18.3.1. Способи добування
- •18.3.2. Фізичні властивості
- •18.3.3. Хімічні властивості
- •18.3.4. Окремі представники. Ідентифікація
- •303 Монокарбонові кислоти
- •18.4.1. Номенклатура та ізомерія
- •Назви деяких дикарбонових кислот
- •18.4.2. Способи добування
- •18.4.3. Фізичні властивості
- •18.4.4. Хімічні властивості
- •18.4.5. Окремі представники
- •309 Мриокар6онові кислоти
- •18.5. Ароматичні дикарбонові кислоти
- •310 Карбонові кислоти. Глава и
- •313 Монокарбонові кислоти
- •19.1.2. Способи добування
- •19.1. Галогенангідриди карбонових кислот (ацилгалогеніди)
- •19.1.1. Номенклатура
- •19.1.3. Фізичні властивості
- •19.1.4. Хімічні властивості
- •19.1.5. Окремі представники
- •19.2. Ангідриди карбонових кислот
- •19.2.1. Номенклатура
- •19.2.2. Способи добування
- •19.2.3. Фізичні властивості
- •19.2.4. Хімічні властивості
- •19.2.5. Окремі представники
- •19.3. Естери карбонових кислот
- •19.3.1. Номенклатура
- •19.3.3. Фізичні властивості
- •19.3.4. Хімічні властивості
- •19.3.5. Окремі представники
- •19.4. Жири
- •19.4.1. Номенклатура та ізомерія
- •19.4.2. Способи добування
- •19.4.3. Фізичні властивості
- •19.4.4. Хімічні властивості
- •19.4.5. Воски. Твіни
- •19.5. Аміди карбонових кислот
- •19.5.1. Номенклатура
- •Ацетамщ,
- •19.5.2. Способи добування
- •19.5.3. Фізичні властивості
- •19.5.4. Хімічні властивості
- •19.5.5. Окремі представники
- •19.6. Нітрили (ціаніди)
- •19.6.1. Номенклатура
- •19.6.2. Способи добування
- •19.6.3. Хімічні властивості
- •19.6.4. Окремі представники
- •20.1. Галогенокарбонові кислоти
- •20.1.1. Номенклатура
- •20.1.2. Способи добування
- •20.1.3. Фізичні та хімічні властивості
- •20.2. Гідроксикислоти
- •20.2.2. Оптична ізомерія
- •20.2.3. Аліфатичні пдроксикислоти
- •359 Гетерофункціональні карбонові кислоти
- •Фізичні та хімічні властивості
- •361 Гетерофункціональні карбонові кислоти
- •20.3. Амінокислоти
- •II Амінокислотами називаються похідні карбонових кислот, у вуглеводневому радикалі яких один або кілька атомів Гідрогену замінені аміногрупою.
- •20.3.1. Номенклатура та ізомерія
- •20.3.2. Способи добування
- •20.3.3. Фізичні та хімічні властивості
- •367 Гетерофункціональні карбонові кислоти
- •20.3.4. Окремі представники
- •0 Контрольні питання та вправи
- •21.1. Номенклатура та ізомерія
- •Глава 21
- •Глава 21
- •21.2.1. Способи добування
- •21.2.2. Фізичні властивості. Просторова будова
- •21.2.3. Хімічні властивості
- •Глава 21 378 — —
- •21.3. Ариламіни
- •Глава 21
- •21.3.2. Фізичні та хімічні властивості
- •А. Реакції за участю атома Нітрогену
- •Глава 21
- •Глава 21
- •21.4. Окремі представники. Застосування
- •В. Окислення ариламінів
- •Глава 21
- •Глава 21
- •22.1. Моносахариди
- •22.1.1. Класифікація та номенклатура
- •Глава 22
- •22.1.2. Стереоізомерія
- •Глава 22
- •22.1.3. Будова моносахаридів
- •Глава 22
- •Глава 22 402
- •Глава 22
- •22.1.4. Способи добування
- •22.1.5. Фізичні властивості
- •22.1.6. Хімічні властивості
- •Глава 22
- •Глава 22
- •Б. Реакції за участю циклічних форм
- •Глава 22
- •22.1.7. Окремі представники
- •Глава 22 412
- •Глава 22
- •22.2. Дисахариди
- •22.2.1. Відновні дисахариди
- •Глава 22
- •22.2.2. Невідновні дисахариди
- •14 Органічна хімія
- •Глава 22 418
- •22.3. Полісахариди
- •Глава 22 н он н он н он н он
- •Глава 22 422
- •Глава 22 424
- •425 Вуглеводи
- •Глава 23
- •Глава 23
- •23.1.1. Стереоізомерія
- •23.1.2. Фізичні властивості
- •23.1.3. Способи добування
- •23.1.4. Хімічні властивості
- •Глава 23
- •23.2. Будова пептидів і білків
- •Глава 23
- •23.3. Синтез пептидів та їх властивості
- •440 Глава 23
- •23.4. Функції білків в організмі
- •Нуклеїнові кислоти
- •24.1. Будова нуклеїнових кислот
- •Глава 24
- •Глава 24
- •24.2. Рибонуклеїнові (рнк) і дезоксирибонуклеїнові (днк) кислоти
- •Глава 24
- •Глава 24
- •Глава 25
- •Неомилювані ліпіди
- •Глава 25
- •Глава 9. Циклоалкани 86
- •Глава 10. Алкени 98
- •Глава 11. Алкадієни 122
- •Глава 12. Алкіни 135
- •Глава 13. Одноядерні арени 147
- •Глава 14. Природні джерела вуглеводнів 179
- •Глава 15. Гетероциклічні сполуки 187
- •Глава 16. Гідроксильні похідні вуглеводнів 212
- •Глава 17. Насичені альдегіди і кетони 256
- •Глава 18. Монокарбонові кислоти 280
- •Глава 19. Функціональні похідні карбонових кислот 314
- •Глава 20. Гетерофункціональні карбонові кислоти 346
- •Глава 21. Аміни 371
- •Глава 22. Вуглеводи 394 о
- •Глава 23. Білки 426 •
- •Глава 24. Нуклеїнові кислоти 444
- •Глава 25. Ліпіди 453
- •Органічна хімія
- •61002, Харків, вул. Пушкінська, 53.
- •61022, Харків, пл. Свободи, 5, Держпром, 6-й під'їзд, 6-й поверх.
- •61012, Харків, вул. Енгельса, 11.
19.3.5. Окремі представники
Етилформіат НСООС2Н5. Безбарвна рідина (т. кип. 54,3 °С), розчиняється в етанолі, етері, малорозчинна у воді. Застосовується у виробництві вітаміну 6), а також як ароматизатор для мила та компонент фруктових есенцій.
Етилацетат СН3СООС2Н5. Безбарвна рідина з приємним запахом (т. кип. 77,1 °С). Малорозчинний у воді, розчиняється
функціональні похідні карбонових кислот
в органічних розчинниках. Застосовується як розчинник етерів целюлози, хлорокаучуку, вінілових полімерів, жирів, восків. Використовується в парфумерії, входить до складу харчових есенцій.
Бензилбензоат С6Н5СООСН2С6Н5. Рідина світло-жовтого кольору (т. кип. 323—324 °С). Нерозчинний у воді, розчиняється в етанолі, міститься в багатьох ефірних маслах. Використовується для лікування корости.
Вінілацетат СН3СООСН=СН2. Безбарвна рідина (т. пл. -100,2 °С; т. кип. 72,7 °С). Добре розчиняється в органічних розчинниках, спричиняє сильне подразнення та некроз шкіри тварин, а пари викликають опік рогової оболонки ока.
Н3С—СООН
+ Н2С=СН
■
" ■
Н3С—С—О—СН=СН2
3 1 -н2о 3 2
ОН
оцтова кислота вініловий спирт вінілацетат
Вінілацетат здатний полімеризуватися з утворенням поліві-
нілацетату (ПВА):
■
я сн=сн2 -І-сн—сн 1
ососн3 ососн3
вінілацетат полівінілацетат
ПВА знайшов широке застосування у виробництві лаків, фарб як основа для клеїв.
Гідролізом ПВА здобувають полівініловий спирт (ПВС), що являє собою білу аморфну речовину, яка не розчиняється в органічних розчинниках, але розчиняється в гарячій воді:
-^СН—СН24^
"Щ°
»
-І-СН—СН2-^
+ лСН3СООН
ОСОСН3 ОН
полівініловий спирт
Полівініловий спирт застосовується у виробництві штучних волокон, лікарських засобів. Зокрема, він використовується при виготовленні хірургічних ниток, які саморозсмоктуються.
Метилакрилат і метилметакрилат. Метилакрилат — безбарвна Рухлива рідина з різким запахом (т. кип. 80,5 °С), добре розчиняється в етанолі, бензені. Метилметакрилат — безбарвна прозора
Карбонові кислоти. Глава /о 326 *'
рідина (т. кип. 101 °С). Необмежено розчинна в діетиловому етері та метанолі.
|сн-сн^
лН2С=СН—С^
Х)СН3
А
метиловий естер гу ОСН
полшетилакрилат
сн, сн,
-|сн2-с-
«н2с=с-с
Т)СН3
метиловий естер /у СН
метакрилової кислоти, 3
акрилової кислоти метилакрилат
поліметилметакрилат
метилметакрилат
Поліметилакрилат застосовується у виробництві «безосколкового скла»; поліметилметакрилат — у виробництві «органічного скла».
19.4. Жири
І
Природні жири тваринного і рослинного походження - представники ліпідів*.
Загальна формула жирів:
О Пріоритет у встановленні будови жирів на-
|| лежить французькому хіміку М. Шеврелю, який
СН2 О С К у 1817 році з'ясував склад і структуру деяких
О тригліцеридів. Триацилгліцерини бувають прості
II , та змішані. Прості включають залишки однако-
9й ° С **■ вих кислот (К = К'= К"), змішані — різних.
?
. ,, г Р к„ шані триацилгліцерини.
2 За консистенцією жири можуть бути твер-
* Від грец. ліпос — жир.
дими й рідкими. Тверді жири містять переважно залишки насичених вищих жирних кислот. До складу рідких жирів, які називають
— 327
функціональні похідні карбонових кислот
маслами або оліями, входять здебільшого залишки ненасичених кислот. Жири тваринного походження зазвичай — тверді речови-нИ) рослинні жири — рідкі*. У молекулах як рослинних, так і тваринних жирів (за винятком свинячого) найчастіше залишки ненасичених кислот розташовані в положенні 2.
До складу жирів входять залишки одноосновних жирних кислот, переважно з нерозгалуженим ланцюгом і парною кількістю (від 4 до 26) атомів Карбону (найчастіше містяться ацильні залишки з 16 та 18 атомами Карбону).
Здебільшого до складу жирів організму людини входять залишки таких насичених вищих жирних кислот, як стеаринова та пальмітинова, ненасичених — арахідонової, олеїнової, лінолевої та ліноленової. Насичені жирні кислоти потрапляють в організм з їжею, а також утворюються в процесі біосинтезу. Олеїнова, лінолева, ліноленова і арахідонова кислоти не утворюються в організмі людини, вони надходять тільки з їжею, тому їх називають незамінними. Тривіальні назви, структурні формули та деякі фізичні константи біологічно важливих жирних кислот, виділених з жирів у процесі гідролізу, наведено в табл. 19.1.
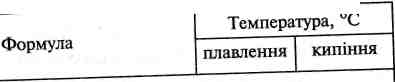
Таблиця 19.1 Насичені й ненасичені жирні кислоти, що входять до складу жирів
Назва кислоти
СН3(СН2)2СООН
СН3(СН2)4СООН
СН3(СН2)6СООН
СН3(СН2)8СООН
СНз(СН2)10СООН
СН3(СН2)і2СООН
СН3(СН2)14СООН
СН3(СН2)16СООН
СН3(СН2)18СООН
Масляна
Капронова
Каприлова
Капринова
Лауринова
Міристинова
Пальмітинова
Стеаринова
Арахінова
Насичені кислоти
І -5,3 |
164 |
||
-3,2 |
206 |
||
|
16,5 |
240 |
|
|
31,6 |
271 |
|
|
44,8 |
299 |
|
|
54,4 |
149* |
|
|
62,9 |
167* |
|
|
70,1 |
184* |
|
|
76,1 |
204* |
|
* Винятками є риб'ячий жир, що являє собою рідину, та масло какао - тверда Речовина (за звичайних умов).

Карбонові кислоти. Глава Ц
328
Закінчення табл. 19.}
Назва кислоти |
Формула |
Температура, °С |
||
плавлення |
кипіння |
|||
Ненасичені кислоти |
|
|||
Олеїнова Елаіщинова а-Лінолева Ліноленова |
СН(СН2)7СН3 СН(СН2)7СООН СН3(СН2)7СН II СН(СН2)7СООН СН3(СН2)4СН=СНСН2СН НООС—(СН2)7СН СН3СН2СН=СНСН2СН II НООС—(СН2)7СН=СНСН2СН |
13,4 16,3 51,5 -5,2 -11,3 |
1 |
|
При тиску 1 мм рт. ст.
