- •Теория строения органических соединений а.М. Бутлерова. Изомерия. Гомология.
- •Строение атома углерода в органических соединениях. Виды гибридизации. Классификация органических соединений.
- •Взаимное влияние атомов в молекулах органических соединений. Электронные эффекты. Индуктивный эффект.
- •Алканы. Гомологический ряд. Изомерия. Номенклатура. Конформации алканов.
- •Химические свойства алканов. Применение метана, этана, пропана, бутана, вазелинового масла, парафинов, вазелина, озокерита и др. Представителей алканов.
- •Алкены. Гомологический ряд. Строение двойной связи. Номенклатура. Изомерия: цис- и транс- изомерия.
- •Физические свойства алкенов. Методы получения: промышленные и лабораторные. Пиролиз алканов.
- •Алкены. Химические свойства. Правило Зайцева. Образование карбкатиона. Реакции электрофильного присоединения. Правило Марковникова.
- •Области применения олефинов в органическом и нефтехимическом синтезе. Полимеры. Реакции полимеризации, поликонденсации.
- •Получение полиэтилена, полипропилена, акрилонитрила, фторированного этилена, бутилена и др. Отдельные представители и их применение.
- •Алкадиены. Номенклатура. Строение бутадиена -1,3. Сопряженная система. Делокализация. Изомерия.
- •Физические свойства алкадиенов. Методы получения. Крекинг-процесс нефти и газа. Промышленное производство синтетического бутадиенового каучука по методу с.В. Лебедеву.
- •Алкины. Строение тройной связи. Номенклатура и изомерия.
- •Промышленные методы получения ацетилена и его гомологов на основе нефтегазового сырья. Высокотемпературный крекинг метана. Получение ацетилена из каменного угля.
- •Физические и химические свойства алкинов. Реакции электрофильного присоединения. Гидратация и изомеризация алкинов. Правило а.П. Эльтекова.
- •Галогенопроизводные углеводороды. Галогенопроизводные углеводороды. Определение и классификация. Номенклатура и изомерия.
- •Производные бензола с содержанием двух атомов галогена. Особенности строения. Способы получения.
- •Галогенопроизводные углеводороды. Способы получения: галогенирование алканов, циклоалканов, алкенов и алкинов, аренов.
- •Галогенопроизводные углеводороды. Физические свойства.
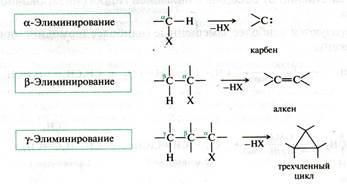
- •Галогенопроизводные углеводороды. Реакции элиминирования в галогеналканах: щелочное дегидрогалогенирование.
- •Реакции ароматических галогенопроизводных: гидролиз хлорбензола, галогенирование бромбензола. Нитрование хлорбензола, сульфирование бромбензола.
- •Физические свойства спиртов одноатомных спиртов. Образование водородных связей.
- •Реакции элиминирования одноатомных спиртов: внутримолекулярная дегидратация спиртов.
- •Реакции окисления одноатомных спиртов в альдегиды и кетоны. Промышленное каталитическое дегидрирование спиртов с образованием альдегидов и кетонов.
- •Двух- и трехатомные спирты. Получение гликолей из галогенпроизводных, гидроксилированием алкенов. Получение глицерина.
- •Двух- и трехатомные спирты. Межмолекулярная дегидратация этиленгликоля с получением диоксана (Метод а.Е. Фаворского).
- •Фенолы. Определение и классификация. Одноатомные, двухатомные, трехоатомные фенолы. Номенклатура и изомерия.
-
Галогенопроизводные углеводороды. Реакции элиминирования в галогеналканах: щелочное дегидрогалогенирование.
Реакции элиминирования сопровождаются отщеплением галоге- новодорода от галогеналкана и приводят к образованию алкенов.
![]()
Поскольку отщепление водорода происходит от β-атома углерода, то такие реакции называются β- или 1,2-элиминированием.
Реакции элиминирования (Е) и нуклеофильного замещения (SN) конкурируют друг с другом, но в определенных условиях каждая из них может стать доминирующей. Отщепление галогеноводорода от галогеналкана становится основным процессом в присутствии нуклеофильных реагентов, обладающих высокой основностью. К ним относятся спиртовые растворы гидроксидов щелочных металлов или алкоголяты щелочных металлов. Элиминированию способствуют также повышение температуры реакционной смеси и концентрации реагентов
![]()

-
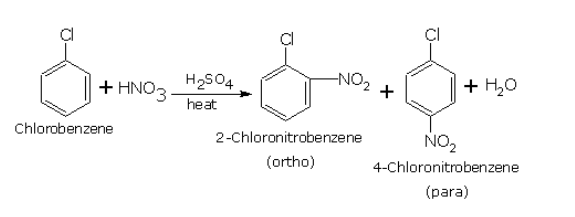
Реакции ароматических галогенопроизводных: гидролиз хлорбензола, галогенирование бромбензола. Нитрование хлорбензола, сульфирование бромбензола.
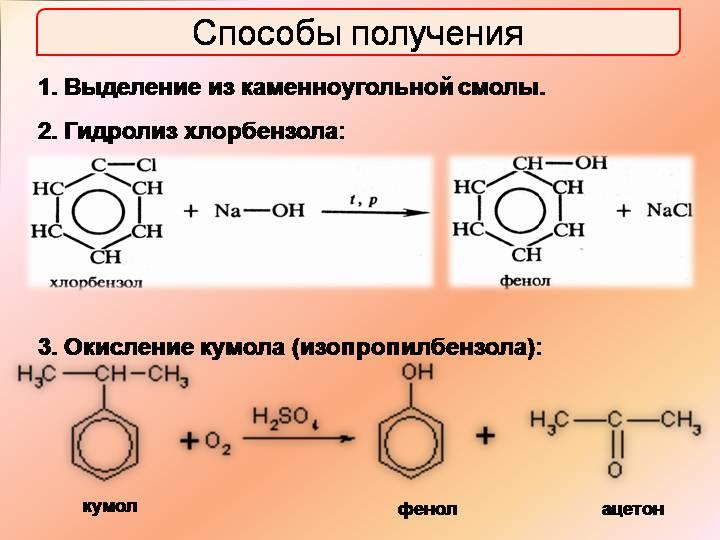
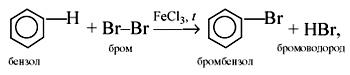
Нитрование хлорбензола
Сульфирование бромбензола C6H5Br + H2SO4 --> п-бромбензолсульфокислота + о-бромбензолсульфокислота + H2O
-
Галогенопроизводные углеводороды. Определение и классификация. Отдельные наиболее важные представители, физические свойства и их применение: этилхлорид, дихлорметан, хлороформ, йодоформ, четыреххлористый углерод, фторотан, дифтордихлорметан, винилхлорид, йодоформ и др.
галогенопроизводные углеводородов. галогенопроизво́дные углеводоро́дов. (галогенсодержащие углеводороды), углеводороды, в молекулах которых один или несколько атомов водорода замещены на атомы галогена.
Классификация галогенопроизводных углеводородов
Галогенопроизводные углеводородов могут быть:
1. по природе радикала :- предельными;- непредельными;- ароматическими.
2. по числу атомов галогена в молекуле: - моно-;- ди-;- полигалогенопроизводные.
3. по природе галогена:- хлор-;- бром-;- йод-;- фторпроизводные.
4. по характеру атома углерода, с которым связан галоген: - первичными;- вторичными;- третичными.
-
Применение вещества Этилхлорид. Кратковременное местное обезболивание при небольших хирургических операциях на кожных покровах.
-
Широкое применение дихлорметана обусловлено его доступной ценой и простотой производства. Его ценят в различных сферах производства за способность к растворению различных жиров и кислот, простое применение и удаление с обрабатываемых поверхностей.
-
Хлороформ используется для наркоза.
-
В медицине иодоформ применяют как антисептик. В частности, используется для полоскания горла. В стоматологии в ряде случаев, йодоформ применяют для тампонады лунки после удаления зуба.
-
Хлористый винил (винилхлорид) – одно из самых широко используемых химических соединений, так как оно является сырьем для производства ПВХ.
-
Фторотан – синтетический медикамент, применяемый для ингаляционной общей анестезии во время проведения различных по сложности и длительности операций.
-
Четыреххлористый углерод Применение: в качестве хладоагентов, как невоспламеняющийся и негорючий растворитель смол, лаков, жиров, восков; как растворитель при проведении многих реакций
-
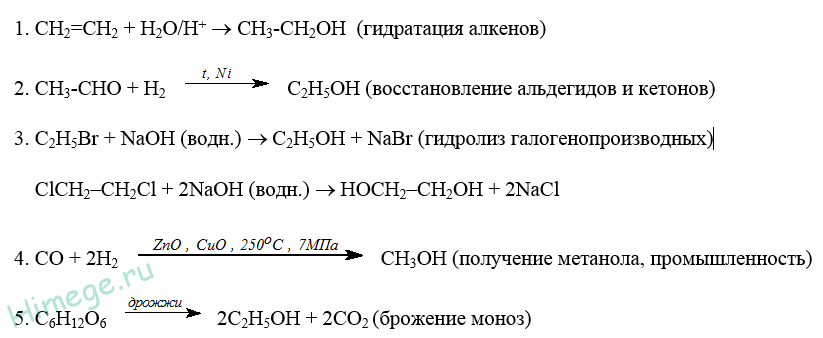
Спирты. Определение, классификация и получение одноатомных спиртов. Правило Марковникова. Способы получения: гидратацией алкенов, щелочным гидролизом галогенопроизводных, каталитическим восстановлением альдегидов и кетонов.
 Классификация
спиртов
Классификация
спиртов
По числу гидроксильных групп (атомности) спирты делятся на:
Одноатомные,
например:
![]()
Двухатомные (гликоли),
например:
![]()
Трехатомные,
например:
![]()
По характеру углеводородного радикала выделяют следующие спирты:
Предельные,
содержащие в молекуле лишь предельные
углеводородные радикалы, например:
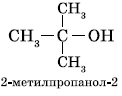
![]()
Непредельные,
содержащие в молекуле кратные (двойные
и тройные) связи между атомами углерода,
например:![]()
Ароматические,
т. е. спирты, содержащие в молекуле
бензольное кольцо и гидроксильную
группу, связанные друг с другом не
непосредственно, а через атомы углерода,
например:![]()
Органические вещества,содержащие в молекуле гидроксильные группы, связанные непосредственно с атомом углерода бензольного кольца, существенно отличаются по химическим свойствам от спиртов и поэтому выделяются в самостоятельный класс органических соединений-фенолы.
Например:
Существуют
и полиатомные (многоатомные
спирты),содержащие более трех гидроксильных
групп в молекуле. Например, простейший
шестиатомный спирт гексаол (сорбит)![]()


Получение: