- •«Посттрансляционная модификация полипептидов»
- •Содержание
- •Введение
- •Основные виды модификаций:
- •Ограниченный протеолиз
- •Ограниченный протеолиз
- •Ковалентная модификация
- •Включение Кофакторов
- •Ассоциация в олигомеры
- •Биохимия: Учеб. Для вузов, Под ред. Е.С. Северина., 2003. 779 с.
- •Биохимия: Учебник для вузов/ в.П. Комов, в.Н. Шведова – м.:Дрофа, 2004. – 640 с.
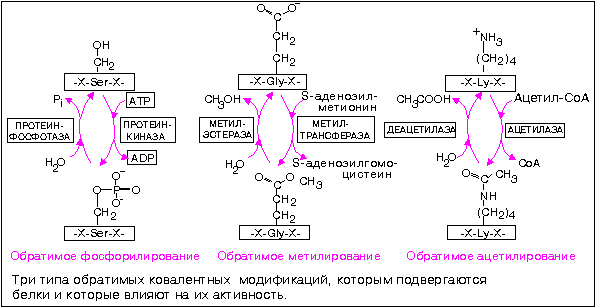
Ковалентная модификация
Структурные белки и ферменты могут активироваться или инактивироваться в результате присоединения различных химических групп: фосфатных, ацильных, метальных, олигосахаридных и некоторых других.
Фосфорилирование белков осуществляется по гидроксильным группам серина, треонина итирозина ферментами из группы протеинкиназ, тогда как дефосфорилирование катализируют гидролитические ферменты фосфопротеинфосфатазы .
Метилирование белка процесс посттрансляционной модификации белка, заключающийся в присоединении метильной группы к аминокислотам полипептида. Метилирование осуществляется главным образом по аминокислотным остаткам лизина, аргинина и гистидина (N-метилирование), а также по остаткам глутаминовой и аспарагиновой кислот (О-метилирование).
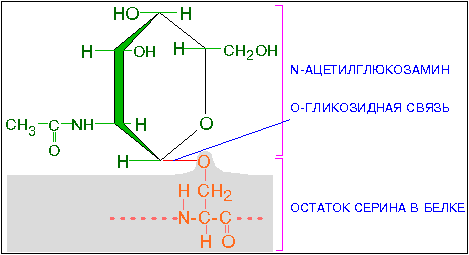
Гликозилированием называют процесс присоединения к полипептидной цепи различных углеводных остатков. Все секретируемые белки эукариот бывают в той или иной степени гликозилированы.
N-гликозилирование осуществляется по аспарагину, расположенному через один аминокислотный остаток от триптофана, и происходит постадийно.

В процессе О-гликозилирования происходит присоединение одного-двух углеводных остатков преимущественно по серину и триптофану. Белки, входящие в состав плазматических мембран или секретирующиеся из клеток, подвергаются гликозилированию. Углеводные цепи присоединяются то гидроксильным группам серина или треонина (О-гликозилирование). Последовательное наращивание углеводного фрагмента происходит в ЭР и аппарате Гольджи.
Включение Кофакторов
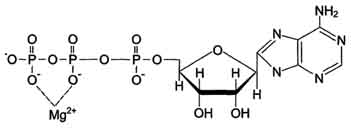
Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой природы и/или в ионах металлов. Более 25% всех ферментов для проявления полной каталитической активности нуждается в ионах металлов. Рассмотрим роль кофакторов в ферментативном катализе.
Кофактор + белковая часть фермента – холофермент.
Кофакторы неорганической природы – ионы металлов.
Функции:
Поддерживают конформацию белковой молекулы
Мостик межу белковой и небелковой частью
Может связывать субстрат и фермент
Может участвовать в катализе
Кофакторы органической природы – витамины, нуклеотиды, витаминоподобные в-ва.
Функции: переносят функциональные группы.
Роль металлов в присоединении субстрата в активном центре фермента
Ионы металла выполняют функцию стабилизаторов молекулы субстрата, активного центра фермента и конформации белковой молекулы фермента, а именно третичной и четвертичной структур.
Ионы металлов - стабилизаторы молекулы субстрата
Для некоторых ферментов субстратом служит комплекс превращаемого вещества с ионом металла. Например, для большинства киназ в качестве одного из субстратов выступает не молекула АТФ, а комплекс Mg2+-ATФ. В этом случае ион Mg2+ не взаимодействует непосредственно с ферментом, а участвует в стабилизации молекулы АТФ и нейтрализации отрицательного заряда субстрата, что облегчает его присоединение к активному центру фермента.