
- •Образования «национально-исследовательский томский политехнический университет»
- •Глава 1. Основы микробиологии
- •1.1. Морфология микроорганизмов .1.1. Систематика и номенклатура микроорганизмов
- •1.1.2. Формы бактерий
- •1.1.3. Структура бактериальной клетки и методы ее исследования
- •Включения Нефотоситезирцющие Основные
- •1.1.4. Морфология микробов-эукариотов: дрожжевых и плесневых грибов
- •Зкзоспоры
- •1.1.5. Методы микроскопического исследования микроорганизмов
- •Электронная микроскопия
- •1.2. Физиология микроорганизмов 1.2.1. Питание бактерий
- •1.2.2. Питательные среды
- •1.2.3. Условия культивирования бактерий
- •1.2.4. Дыхание бактерий
- •1.2.5.Ферменты бактерий
- •1.2.6. Культуральные свойства бактерий
- •1.2.6. Выделение чистых культур микроорганизмов
- •Глава 2. Химические основы жизни
- •2.1. Липиды
- •2.1.1. Жирные кислоты и родственные липиды
- •Глава 7. Сельскохозяйственная биотехнология 360
- •Глава 8. Экологическая биотехнология 368
- •2.1.2. Жирорастворимые витамины, стероиды и другие липиды
- •2.2. Сахара и полисахариды
- •2.2.2. Дисахариды и полисахариды
- •2.3. Белки
- •2.3.1. Биологические функции белков
- •2.3.2. Белковые аминокислоты и полипептиды
- •2.3.3. Структура белков
- •Первичная структура белков
- •Глава 7. Сельскохозяйственная биотехнология 360
- •Глава 8. Экологическая биотехнология 368
- •Глава 7. Сельскохозяйственная биотехнология 360
- •Глава 8. Экологическая биотехнология 368
- •2.4.5. Биосинтез нуклеиновых кислот и белков (матричные биосинтезы)
- •I I аденин
- •Глава 3. Технологические основы биотехнологических производств
- •3.1. Процессы в биотехнологии
- •3.4. Контроль и управление биотехнологическими процессами; моделирование и оптимизация
- •Глава 4. Генная инженерия
- •4.3. Получение фармакологических препаратов с помощью методов генной инженерии
- •4.3.1. Биосинтез инсулина человека в клетках кишечной палочки
- •4.3.2. Биосинтез соматотропина и других гормонов человека
- •4.3.3. Получение интерферонов
- •4.3.4. Получение иммуногенных препаратов и вакцин
- •4.3.5. Другие области применения генной инженерии
- •1. Новые методы диагностики и исследований
- •2. Генная инженерия и белковая инженерия ферментов
- •3. Получение бактерий для деградации токсикантов и ксенобиотиков
- •5. Биоматериалы
- •4.5. Преимущества и опасность генной инженерии
- •4.5. Меры безопасности
- •Глава 5. Промышленная микробиология
- •5.1. Производство первичных метаболитов
- •5.1.1. Производство аминокислот
- •5.1.2. Производство органических кислот
- •5.1.3. Получение витаминов
- •5.2. Производство вторичных метаболитов
- •5.3. Производство белков одноклеточных и многоклеточных
- •5.3.1. Производство белка одноклеточных организмов
- •5.3.2. Производство грибного белка (микопротеина)
- •5.3.3. Производство цианобактерий
- •Глава 6. Инженерная энзимология
- •6.1. Методы получения иммобилизованных ферментов
- •6.1.1. Физические методы иммобилизации
- •6.1.2. Химические методы иммобилизации ферментов
- •Носитель Вставка Фермент Иммобилизованный фермент
- •6.2. Применение иммобилизованных ферментов
- •6.3. Промышленные процессы с использованием иммобилизованных ферментов
- •6.3.1. Разделение рацемических смесей аминокислот
- •6.3.2. Производство кукурузного сиропа с высоким содержанием
- •Глава 7. Сельскохозяйственная биотехнология
- •7.1. Биопестициды
- •7.1.1. Технология получения бактериальных энтомопатогенных
- •7.1.2. Технология получения грибных энтомопатогенных
- •7.1.3. Технология получения вирусных энтомопатогенных препаратов
- •7.2. Биологические удобрения
- •7.2.1. Технология получения сухого нитрагина
- •7.2.2. Технология получения сухого азотобактерина
- •7.2.3. Технология получения фосфоробактерина
- •Глава 8. Экологическая биотехнология
- •8.1. Аэробная биологическая очистка сточных вод
- •8.1.1. Основные характеристики сточных вод
- •8.1.2. Процессы с участием активного ила
- •8.1.3. Аэробная обработка ила
- •8.1.4. Вторичная очистка сточных вод с помощью капельных биологических фильтров
- •8.2. Анаэробная переработка отходов
- •1Связь, a-мальтоза
6.3. Промышленные процессы с использованием иммобилизованных ферментов
В настоящее время лишь несколько процессов с использованием иммобилизованных ферментов имеют крупномасштабное применение. Эти процессы следующие:
Получение 6-аминопенициллановой кислоты с помощью иммобилизованной пенициллинамидазы (Россия, Япония, Финляндия).
Получение глюкозо-фруктозных сиропов с использованием иммобилизованной глюкозоизомеразы (США, Великобритания, Голландия, Финляндия, Дания, Япония).
Разделение рацемических смесей аминокислот с использованием иммобилизованной аминоацилазы (Япония).
Получение безлактозного молока с использованием иммобилизованной лактазы (Чехия, США, Италия).
6.3.1. Разделение рацемических смесей аминокислот
Потребность в L-аминокислотах для производства пищевых продуктов и в медицинских целях постоянно возрастает. В связи с этим большое внимание уделяется разработке как микробиологических, так и химических методов получения L-аминокислот. Недостатком химических методов является рацемическая природа синтетических аминокислот. В общем случае D-аминокислоты не имеют питательной ценности, поэтому желательно получать только физиологически активные L- аминокислоты.
Указанная цель была достигнута в процессе, разработанном фирмой Tanabe Seiyaku Co., Ltd. (Япония), в котором впервые в промышленном масштабе применялись иммобилизованные ферменты. Основой процесса является метод разделения оптических изомеров в соответствии со следующей реакцией, катализируемой ферментом аминоацила- зой:
nhcor
аминоацилаза
dl- r—c—cooh + h2o h
dl-аминокислота
nhcor1 nhcor-i
i 1 i 1 l- r-c-cooh + d- r—c—cooh hh
l-аминокислота d-ациламинокислота
Эту реакцию осуществляют в реакторах колонного типа с иммобилизованной аминоацилазой. Общая схема процесса приведена на рис. 6.4.
Рис.
6.4. Технологическая схема процесса с
применением иммобилизованной
аминоацилазы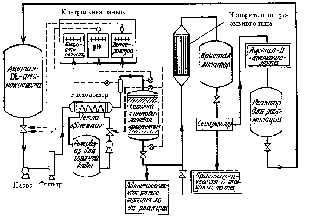
Для разделения смеси рацемическую аминокислоту переводят в ацилированную форму и подвергают действию фермента аминоацила- зы, разрушающего ацильную связь и высвобождающего свободную аминокислоту. Фермент гидролизует амидную связь только L-изомера. В результате получается смесь свободной L-аминокислоты и ацилиро- ванной D-аминокислоты. Эти вещества, как правило, имеют разную растворимость (чаще всего в воде, иногда в других растворителях), поэтому их довольно легко разделить путем дробной кристаллизации. Оставшийся после разделения D-изомер нагревают, в результате чего он рацемизуется, после этого разделение повторяют до тех пор, пока весь изомер не перейдет в L-форму (обычно выходы превосходят 90 %).
Промышленный процесс заключается в следующем. Через колонну, заполненную аминоацилазой, иммобилизованной ионными связями на DEAE-сефадексе, пропускают раствор рацемической модифициро
ванной по аминогруппе аминокислоты. После колонны раствор осторожно упаривают в вакууме: при концентрировании раствора первым выпадает в осадок менее растворимый компонент (как правило, это ацилированный D-изомер). Далее раствор фильтруют и упаривают еще раз для выделения свободной L-аминокислоты. D-Изомер растворяют и нагревают, при этом он рацемизуется, и его возвращают в колонну. В итоге добиваются высокой концентрации L-аминокислоты. Фермент аминоацилаза мало чувствителен к типу аминокислоты, поэтому одна установка с иммобилизованным ферментом может использоваться для получения самых разных аминокислот. Когда активность фермента падает, добавляют порцию свежего катализатора (один раз в несколько лет).
